Фокальная кортикальная дисплазия

Фокальная кортикальная дисплазия (ФКД) является одной из основных причин развития резистентных к терапии фокальных эпилептических приступов.
О резистентности к терапии говорят в тех случаях, когда приступы сохраняются после применения двух базовых, одобренных для данной формы эпилепсии антиэпилептических препаратов (АЭП) в максимально переносимых дозах последовательно (в виде монотерапии) или в комбинации.
Стоит отличать резистентность от «псевдорезистентности», к которой могут привести: неправильно установленный диагноз (например, психогенные приступы), неправильно выбранные АЭП (например, карбамазепин при абсансах или миоклонических приступах), не адекватную возрасту дозировку АЭП, несоблюдение пациентом предписаний врача и др. Термин «фокальная кортикальная дисплазия» был впервые употреблен Дэвидом Тейлором, описавшим 10 больных с резистентной к терапии эпилепсией, у которых были обнаружены нарушения кортикального развития. Сегодня его именем (тейлоровская кортикальная дисплазия) называют дисплазии IІ типа.
В настоящее время ФКД относят к разновидностям обширной группы патологий под названием нарушения кортикального развития (НКР).
 Таблица 1 ❘ Современная классификация ФКД по Barkovich
Таблица 1 ❘ Современная классификация ФКД по Barkovich
Напомним, что в пределах коры наблюдается чередование слоев, содержащих преимущественно тела нервных клеток, со слоями, образованными в основном их аксонами, и поэтому, например, на свежем срезе кора головного мозга выглядит «полосатой». На основании формы и расположения нервных клеток в коре с типичным строением можно выделить шесть слоев, некоторые из них подразделяются на два или более вторичных слоя.
В соответствии со строением коры выделяют следующие основные зоны: новую кору (неокортекс), старую кору (архикортекс), древнюю кору (палеокортекс) и межуточную кору (периархикортикальную и перипалеокортикальную). Неокортекс является наиболее обширной зоной коры и занимает дорсальную и латеральную поверхность больших полушарий, в то время как палеокортекс находится на базальной и медиальной поверхности полушарий.
В неокортексе различают следующие слои:
I. Молекулярный. В этом слое имеется множество волокон, образующих густое тангенциальное (т. е. с направлением волокон по касательной относительно коры) поверхностное сплетение. Клеток незначительное количество, в основном это звездообразные мелкие клетки, которые осуществляют местную интеграцию деятельности эфферентных нейронов.
II. Наружный зернистый. Содержит мелкие нейроны различной формы, которые имеют синаптические связи с нейронами молекулярного слоя на всем поперечнике коры. В глубине располагаются малые пирамидные клетки.
III. Наружный пирамидный. Этот слой состоит из пирамидных клеток малой и средней величины. Некоторые отделы коры в этом слое содержат крупные пирамидные клетки. Часть отростков этих клеток достигает первого слоя, участвуя в формировании тангенциального подслоя, другие погружаются в белое вещество полушарий мозга.
IV. Внутренний зернистый. Характеризуется рыхлым расположением мелких нейронов различной величины и формы с преобладанием звездчатых, имеющих дугообразные возвратные аксоны. Аксоны клеток проникают в выше- и нижележащие слои.
V. Внутренний пирамидный. Состоит в основном из средних и больших пирамидных клеток (клеток Беца). Эти нейроны обладают длинными апикальными дендритами, достигающими молекулярного слоя, а также базальными дендритами, распространяющимися более или менее тангенциально по отношению к поверхности. Эти слои четко выражены в передней центральной извилине и незначительно — в других участках коры. Из этого слоя в основном формируются двигательные произвольные пути (проекционные эфферентные волокна).
VI. Полиморфный. В этом слое расположены преимущественно веретеновидные нейроны с короткими извитыми верхушечными дендритами, заканчивающимися в V и IV слоях коры. Аксоны многих клеток слоя объединяются в возвратные волокна, проникая в V слой. Наиболее глубокая часть этого слоя переходит в белое вещество.
Гистопатология и этиология
Нарушения коркового развития представляют собой различные изменения в строении коры головного мозга в результате патологии внутриутробного развития (конкретнее — нарушения клеточного формирования коры). Они могут быть локальными или диффузными, а также могут сочетаться с другими аномалиями головного мозга (патологиями мозжечка, гиппокампа, сосудистыми мальформациями, опухолями ЦНС и др.). Их этиология до конца неизвестна.
К возможным этиологическим факторам можно отнести генетические изменения, химические мутагены, ионизирующую радиацию, вирусные инфекции. Вид порока зависит не от природы повреждающего агента, а от возраста эмбриона.
Пороки головного мозга могут развиться на всех этапах эмбрионального и частично в фетальном периоде. Если «поломка» происходит во время формирования прозэнцефалона (2–3-й месяц внутриутробного развития), то возникают грубые пороки, например, голопрозэнцефалия, формирующаяся в строго фиксированные для ее развития сроки — 22–24-й дни внутриутробного развития. Наибольший интерес для клинициста представляют пороки развития головного мозга, формирующиеся вследствие аномальных процессов развития мозга с 6-й по 20-ю неделю внутриутробного развития:
- 3‒4-й месяц гестации — процесс пролиферации (начало с 7-й недели);
- 3‒5-й месяц гестации — центробежная миграция (начало с 8-й недели);
- 5-й месяц гестации — нейронная организация.
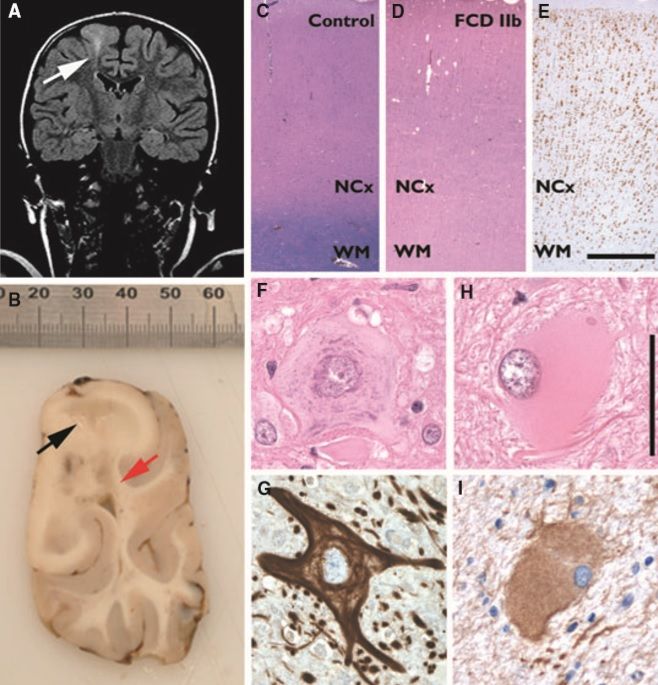
ФКД гистологически проявляется:
- кортикальной дисламинацией, т.е. нарушением нормальной “слоистости” коры и наличием эктопированных нейронов в белом веществе,
- наличием диспластических нейронов,
- наличием баллонных клеток,
- увеличением размеров клеток (цитомегалией) до размеров (или даже больше) гигантских пирамидных клеток.
Кортикальная дисламинация в той или иной степени выражена при всех типах ФКД, однако наиболее выражена она при ФКД I типа, причем может нарушаться как радиальная (горизонтальная) архитектоника, так и тангенциальная, а при Iс типе наблюдаются оба варианта. Также при первом типе может возникать цитомегалия.
Эктопированные нейроны в белом веществе могут встречаться при различных НКР и имеют невысокий эпилептогенный потенциал.
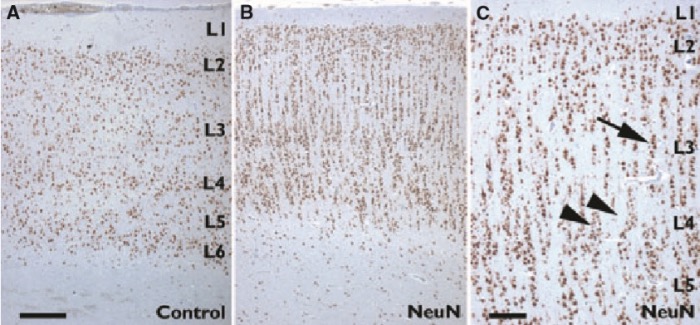
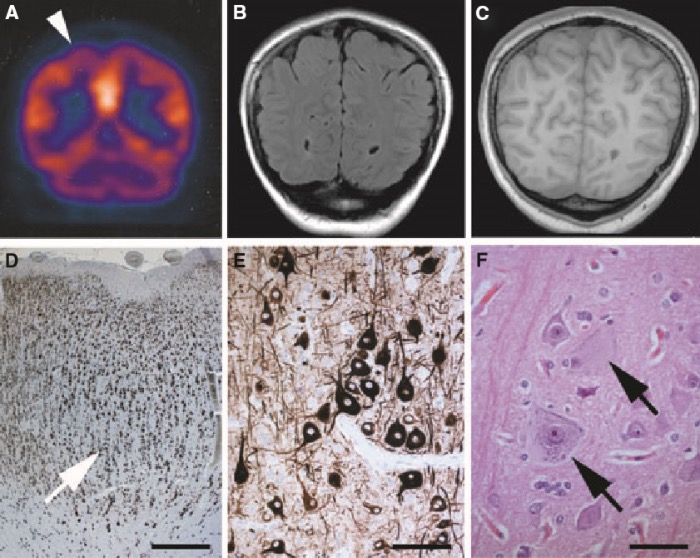
Второй тип ФКД характеризуется (в дополнение к нарушениям цитоархитектоники коры) появлением диспластических нейронов при типе IIa, а при типе IIb — диспластических нейронов и баллонных клеток.
Диспластические нейроны имеют следующие отличия от нормальных нейронов:
- они увеличены в размерах;
- имеют большие клеточные ядра;
- характеризуются аномальным накоплением субстанции Ниссля и расположением ее ближе к мембране,
- а также увеличенным количеством нейрофиламентов в цитоплазме.
Такие дисморфичные нейроны формируют скопления, что приводит к локальному утолщению коры, иногда такие скопления «выпячиваются» в белое вещество.Также стоит заметить, что эти нейроны обладают крайне высоким эпилептогенным потенциалом. В сравнении с неизмененными корковыми клетками эти клетки формируют большее количество синаптических связей при заметном снижении количества «тормозных» ГАМКергических интернейронов.
Скопление диспластических клеток представляет собой патологическую нейрональную сеть, в которой постоянно циркулируют процессы возбуждения. В дополнение к этому у больных с дисплазией IIb типа отмечено нарушение деятельности ГАМКергической системы с изменением количества разных подтипов рецепторов. Этот факт важно учитывать при назначении препаратов, имеющих влияние на ГАМК-рецепторы.
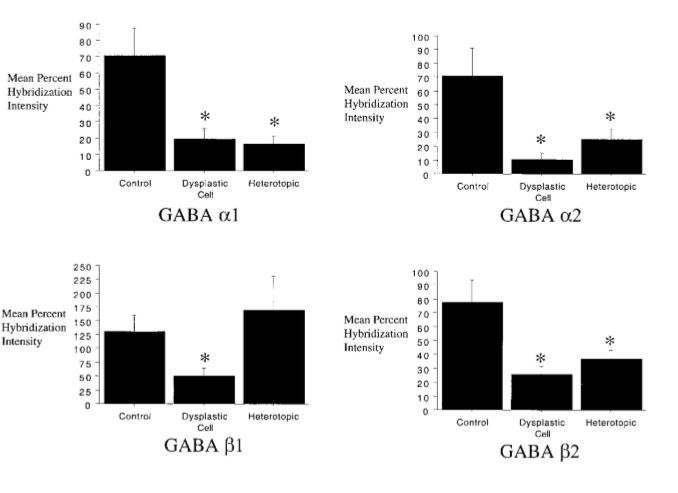 Различие в частоте встречаемости разных подтипов ГАМК-рецепторов в клетках нормальной коры, диспластических нейронах и гетеротопических клетках
Различие в частоте встречаемости разных подтипов ГАМК-рецепторов в клетках нормальной коры, диспластических нейронах и гетеротопических клетках
Баллонные клетки при ФКД встречаются во всех слоях коры (включая первый) и отличаются увеличенными ядрами, часто — несколькими ядрами с «мостиками» между ними, опалесцирующей цитоплазмой и отсутствием субстанции Ниссля. Интересно, что баллонные клетки также можно найти в кортикальных туберах больных туберозным склерозом.
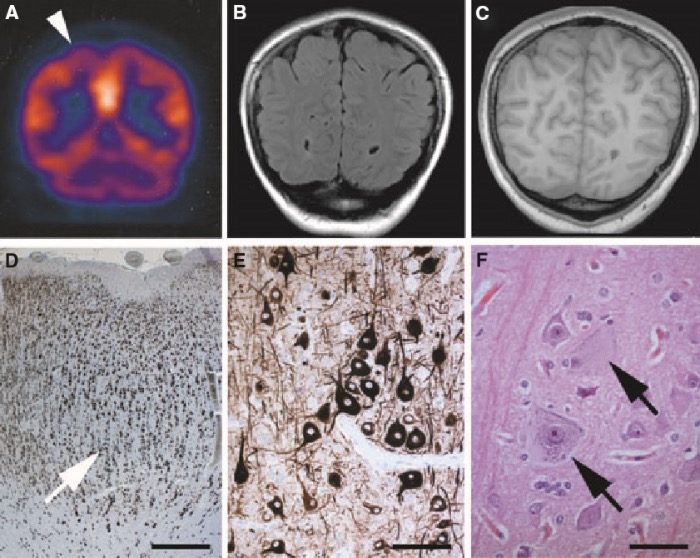
Клиническая картина
ФКД могут быть диагностированы только по данным нейровизуализационного (МРТ) исследования, верифицированы — гистологически. Клиническая картина позволяет заподозрить данное нарушение, однако специфического клинического паттерна у ФКД нет.
Основным проявлением ФКД является эпилепсия. Реже в качестве основного проявления выступают различные двигательные и когнитивные нарушения.
Эпилепсия при ФКД обычно характеризуется резистентностью к терапии и ранним дебютом. Наиболее частый возраст появления клинических проявлений — в интервале от первых месяцев до 4-х лет. ФКД II типа дебютирует достоверно позже, в диапазоне от младенческого до подросткового возраста. Дебют эпилепсии во взрослом возрасте — редкое, но не казуистическое явление. Описаны случаи начала приступов в возрасте после 50 лет. Нет явного превалирования по признаку пола.
ФКД может проявляться практически всеми видами эпилептических приступов, а также эпилептическими энцефалопатиями. Общими чертами приступов являются:
- заметный полиморфизм (один вид приступов со временем сменяется другим, затем возвращается и т. д.),
- наличие фокальных припадков,
- асимметричность приступов,
- частое развитие эпилептической энцефалопатии и органического аутизма (что коррелирует с ранним началом приступов),
- небольшая длительность приступов,
- вторичная генерализация происходит раньше в сравнении с височной эпилепсией,
- необычные, демонстративные двигательные феномены, двигательные автоматизмы,
- «ауры» перед приступами,
- минимальная постприступная спутанность сознания.
ФКД I типа
Довольно характерным проявлением являются инфантильные спазмы. В этиологии 30 % инфантильных спазмов участвует тот или иной тип нарушения кортикального развития.
При ФКД инфантильным спазмам часто предшествуют другие, чаще фокальные «вегетативные» приступы: миоклонические, тонические, окулотонические. Эти приступы иногда можно заметить с первых дней жизни ребенка. Инфантильные спазмы присоединяются после 4‒6 месяцев. Для ФКД более характерны несимметричные спазмы: неравномерное вовлечение конечностей, поворот головы и глаз в сторону, нистагм (очаг располагается контрлатерально быстрому компоненту нистагма).
Характерно нарушение поведения перед приступом, что является проявлениями «ауры»: «замирание» и «сосредотачивание» ребенка, он как будто прислушивается к своим ощущениям; улыбка, смех, реже — внезапный плач, испуг. При локализации очага в затылочной области (наиболее частая локализация Iа типа) аура проявляется зрительными галлюцинациями и иллюзиями, при этом ребенок может закрывать глаза руками, пытаясь избавиться от неприятных ощущений. Дебют любых приступов до 3 месяцев жизни — фактор будущей резистентности и крайне неблагоприятного прогноза.
Периодические спазмы обычно дебютируют в более позднем возрасте. Их характеризует неизменность (приступы не меняют проявлений, не исчезают и не перетекают в другие формы эпилепсии на протяжении многих лет). Приступы возникают серийно, причем каждой серии предшествуют фокальные приступы и нарушения сознания разной степени. Собственно спазмы проявляются серийными приступами с короткими нарушениями аксиальной мускулатуры: кивок, наклон туловища, сведение и разведение рук. Можно заметить ассиметричность спазмов и фокальные проявления в виде наклона глаз и головы в сторону или одностороннего спазма лицевой мускулатуры. Фокальные приступы могут возникать до, после серии спазмов и в серии между «основными» приступами. Длительность серии обычно составляет от 3 до 30 минут.
Среди других проявлений можно отметить фокальные моторные и диалептические приступы, а также вторично-генерализованные приступы. При обширных дисплазиях нередки псевдогенерализованные приступы: атипичные абсансы, эпилептический миоклонус, генерализованные тонические и атонические приступы.
Для ФКД Ia типа характерны: ранний дебют эпилепсии, тяжелая умственная отсталость (что коррелирует с возрастом начала приступов) и врожденные двигательные нарушения (церебральный паралич). Типичная локализация — задневисочно-теменно-затылочная область.
Характерен также феномен распространения эпилептической активности с патологического очага на всю гемисферу или «переброс» на здоровую гемисферу — феномен вторичной билатеральной синхронизации, что обуславливает вторично-генерализованные приступы. Клиническая картина может напоминать синдромы Ленокса-Гасто и Дозе.
Для ФКД Ib типа характерен более поздний дебют и менее тяжелое течение.
ФКД II типа
Заболевание дебютирует, как правило, в более позднем возрасте. Наиболее часто возникают тонические приступы, симметричные или асимметричные, возможно, с дополнительным моторным компонентом. Характерны также приступы, связанные со сном (в т.ч. эпилепсия с электрическим эпилептическим статусом медленного сна).
При вовлечении сенсомоторной коры может развиваться картина Кожевниковской эпилепсии.
Лучевые признаки
Стандартом визуализации ФКД является МРТ. Иногда (чаще в случае предоперационного планирования) используется ПЭТ- и ОФЭКТ-КТ, однако их доступность крайне невысока.
МР-исследование должно проводиться на аппарате с индукцией магнитного поля не менее 1,5 Тесла. Протокол сканирования при подозрении на ФКД должен включать в себя:
- Аксиальные Т2, Т1, FLAIR, DWI,
- Сагиттальные Т2,
- Аксиальные Т2* и/или SWI,
- 3D-T1,
- 3D T2/ FLAIR.
Крайне желательно, чтобы протокол поиска ФКД, как и любой вариант “эпилептического протокола”, включал в себя хотя бы одну из названных последовательностей в режиме тонких срезов (1–2мм).
Режим FLAIR не имеет диагностической ценности для детей до 1 года, пока процессы миелинизации волокон головного мозга не завершены. У различных типов фокальной кортикальной дисплазии существует много схожих черт, а отдельные типы при МРТ могут не иметь выявляемых изменений.
Основные черты фокальной кортикальной дисплазии включают:
- утолщение коры,
- размытость границ серого и белого вещества с аномальной архитектоникой субкортикального слоя,
- гиперинтенсивный МР сигнал от белого вещества на T2/FLAIR взвешенных изображениях с или без признаков трансмантийной дисплазии,
- гиперинтенсивный МР сигнал от серого вещества на T2/FLAIR взвешенных изображениях,
- изменение структуры борозд и извилин.
Трансмантийная дисплазия (трансмантийный признак) — высокая интенсивность сигнала на T2/FLAIR, который простирается от желудочков к коре. Он также связан с другими особенностями фокальной кортикальной дисплазии, такими как утолщение коры, размытие границы между серым и белым веществом и снижение сигнала на Т1-ВИ.
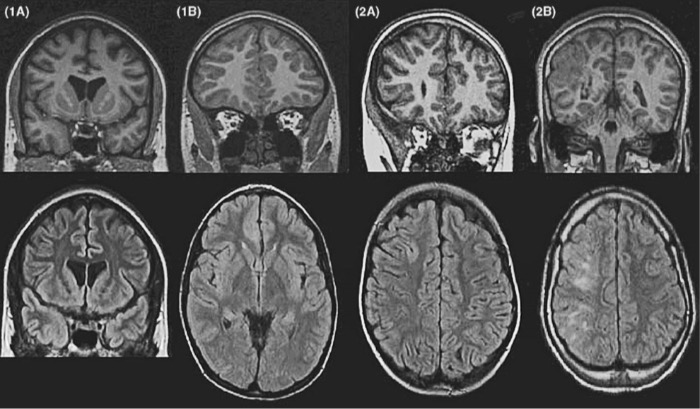
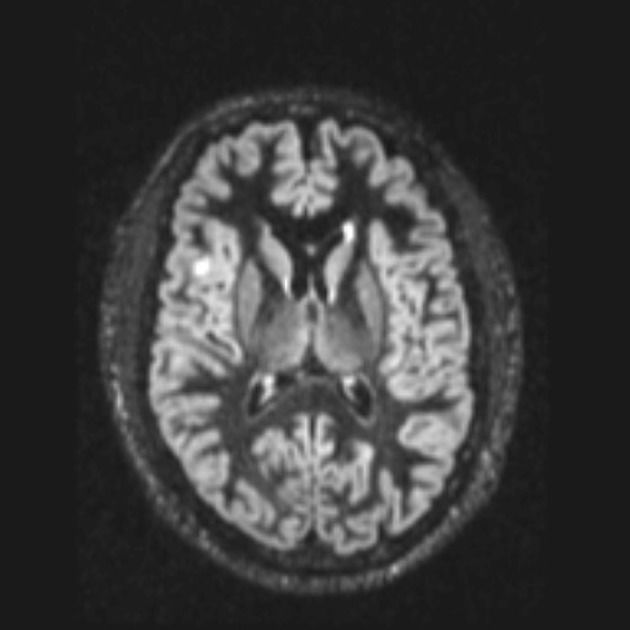
МР-изображение в DIR-последовательности: заметное повышение сигнала и утолщение коркового слоя правой лобной области
В отличие от патологов, использующих классификацию Барковича, радиологи чаще пользуются классификацией фокальной кортикальной дисплазии Blumcke (2011), которая учитывает, в первую очередь, локализацию (так как различить гистологические типы по данным МРТ не представляется возможным):
I тип
Локализация
- Ia тип: локализация обычно ограничена височной долей, в сочетании с атрофией гиппокампа данный тип сейчас относится к IIIa типу по классификации Blumcke.
- Ib тип: чаще встречается за пределами височной доли.
Структура
размытость границ серого и белого вещества (менее выражена, чем при II типе ФКД), выраженная “сегментарная” или долевая атрофия/гипоплазия с локальной потерей объема белого вещества.
МР сигнал
белое вещество: промежуточно повышенный МР сигнал на T2/FLAIR взвешенных изображениях, сниженный МР сигнал на T1 взвешенных изображениях.
II тип
Локализация
часто встречается в лобных долях, менее часто, по сравнению с ФКД I типа, в височных долях.
Структура
изменение структуры борозд и извилин, выраженная размытость границ серого и белого вещества, утолщение коры.
МР сигнал
- белое вещество — промежуточно повышенный МР сигнал на T2/FLAIR взвешенных изображениях, обычно более интенсивный, чем сигнал от прилежащей коры;
сниженный МР сигнал на T1 взвешенных изображения, локально измененный сигнал может распространяться за пределы коры по направлению к желудочкам (трансмантийный признак), что не характерно для I типа; - серое вещество — несколько повышенный МР сигнал на T2 взвешенных изображениях;
кора остается гипоинтенсивной по отношению к повышеному сигналу от белого вещества, на Т2 взвешенных изображениях — более выраженный, чем при I типе
III тип
Фокальная кортикальная дисплазия III типа характеризуется наличием ряда сочетанных нарушений
- IIIa: сочетается с атрофией гиппокампа,
- IIIb: сочетается с глионейрональными опухолями (например, с дисэмбриопластическими нейроэпителиальными опухолями),
- IIIc: с сосудистыми мальформациями,
- IIId: с инсультом раннего детского возраста.
Учитывая наличие разных классификаций, необходимо указывать, какая именно была использована при формировании заключения (например, “ФКД Iа типа по Blumcke”).
Лечение
Лекарственная терапия
Медикаментозное лечение при ФКД часто неэффективно, причем, если после назначения первого АЭП не произошло улучшения, это говорит о высокой вероятности дальнейшей резистентности к терапии.
При эпилептических спазмах у детей младенческого возраста рекомендуется начинать лечение с вигабатрина или кортикостероидов, при фокальных приступах — с карбамазепина, при псевдогенерализованных — с вальпроатов. При эпилептических спазмах (включая периодические спазмы) у больных ФКД стероиды могут работать хуже, чем вигабатрин. При этом предпочтительнее использовать вигабатрин в высоких дозах в комбинированной терапии (обычно с вальпроатом).
При частых приступах и высоком индексе эпилептиформной активности на ЭЭГ у больных ФКД I типа рекомендуют применение фенитоина и вигабатрина. Поскольку у больных ФКД IIb типа нарушено функционирование ГАМКергических систем с незрелостью ГАМК-рецепторов, следует с осторожностью назначать препараты из группы транквилизаторов и другие вещества, влияющие на ГАМК-рецепторы.
К сожалению, даже при эффективности терапии возможно ухудшение состояния больных. У пациентов с ФКД описаны рецидивы приступов после 2–11 лет лекарственной ремиссии.
Хирургическое лечение
У 50–60 % больных ФКД после хирургического вмешательства эпилептические приступы прекращаются, причем исходы по приступам не зависят от возраста оперированных пациентов.
Исходы оперативного вмешательства существенно хуже у больных ФКД I типа, чем у больных ФКД II типа: 50 % и меньше — достижение ремиссии после операции у 1-й категории пациентов, 70–90 % — во 2-й. Наилучшие результаты хирургического лечения достигаются у больных с ФКД IIb типа. Исходы операции при ФКД I типа во многом зависят от объема резекции. При выполнении фокальных кортикальных или мультилобарных резекций ремиссия приступов наступает лишь у 21 % больных ФКД I типа, а при выполнении гемисферэктомии — у 70 % в течение первых 6 месяцев после операции и у 60 % — в течение 5 лет.
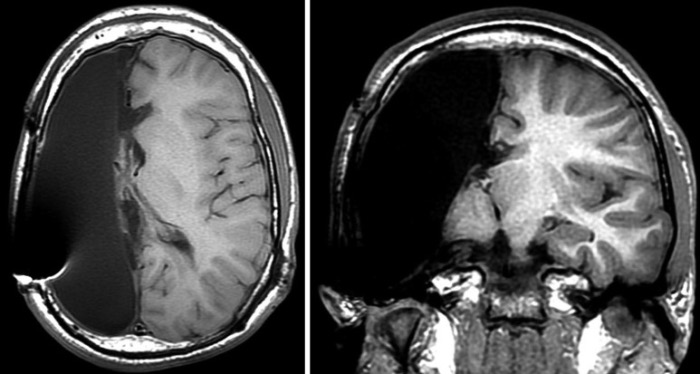 T1 аксиальные и корональные МР-изображения пациента после проведенной анатомической правосторонней гемисферэктомии
T1 аксиальные и корональные МР-изображения пациента после проведенной анатомической правосторонней гемисферэктомии
При обширных ФКД I типа при отсутствии гемипареза у детей возможно проведение операции в объеме «все, кроме двигательной коры» («everything, but motor»): диссекция всего полушария, за исключением моторной коры и ее связей. Это позволяет максимально «изолировать» диспластическую кору и избежать развития гемипареза. При неудаче данной операции и продолжении приступов выполняется уже полная диссекция пораженного полушария.
Источники
1. Мухин К. Ю. Фокальные кортикальные дисплазии: клинико-электро-нейровизуализационные характеристики //Русский журнал детской неврологии. – 2016..2. Шевченко А. А. Врождённые пороки развития центральной нервной системы (ЦНС): клинико-неврологические аспекты и проблемы пренатальной диагностики //Международные обзоры: клиническая практика и здоровье. – 2014.
3. Шевченко А. А. Врождённые пороки развития центральной нервной системы (ЦНС): клинико-неврологические аспекты и проблемы пренатальной диагностики //Международные обзоры: клиническая практика и здоровье. – 2014
4. Crino P. B. Focal cortical dysplasia //Seminars in neurology. – Thieme Medical Publishers, 2015
5. Wong-Kisiel L. C. et al. Double inversion recovery magnetic resonance imaging in identifying focal cortical dysplasia //Pediatric neurology. – 2016.
6. Colombo N. et al. Focal cortical dysplasias: MR imaging, histopathologic, and clinical correlations in surgically treated patients with epilepsy //American Journal of Neuroradiology. – 2003.
7. Widdess-Walsh P. et al. Electro-clinical and imaging characteristics of focal cortical dysplasia: correlation with pathological subtypes //Epilepsy research. – 2005.
8. Barkovich A. J. et al. A developmental and genetic classification for malformations of cortical development //Neurology. – 2005.
9. A.Prof Frank Gaillard et al. Focal cortical dysplasia. Radiopaedia.org (https://radiopaedia.org/articles/focal-cortical-dysplasia)
10. Alami B. et al. Magnetic resonance imaging findings and Spectrum of Etiologies in children epilepsy //European Congress of Radiology. – 2015
11. radiographia.info/article/fokalnaya-kortikalnaya-displaziya
12. 24radiology.ru/golova-i-sheya-2/klassifikatsiya-vrozhdyonnyh-porokov-razvitiya-tsentralnoj-nervnoj-sistemy/
13. Kabat J., Król P. Focal cortical dysplasia–review //Polish journal of radiology. – 2012
