Cиндром Бланда-Уайта-Гарланда
Аномалии коронарных артерий — почти terra incognita для современной кардиологии, в то же время, по разным данным, они обнаруживаются у 0,6 % – 5,64 % кардиологических пациентов, однако есть вероятность, что частота встречаемости намного выше. Недостаточно изучены анатомические варианты коронарных сосудов, их патофизиологическое и клиническое значение, прогноз, вследствие чего нет обоснованных рекомендаций по лечению пациентов, часты ошибки в диагностике и выборе лечения.
В подавляющем большинстве случаев аномалии коронарных артерий обнаруживаются посмертно, не являясь причиной смерти, или случайно при инструментальном исследовании по другому поводу и в течение жизни не вызывают патологических состояний. Таким образом, существуют предпосылки для определения новых «нормальных» вариантов анатомии коронарных сосудов, на что указывает P. Angelini в своих работах, предлагая идентифицировать коронарные сосуды по особенностям их средних и дистальных сегментов или микрососудистого бассейна, а не места отхождения и хода проксимальных сегментов.
Подавляющее большинство аномалий коронарных артерий доброкачественны, но существует группа аномалий, чреватых постоянными или периодическими нарушениями кровоснабжения миокарда и тяжелыми последствиями ишемии без ранней диагностики и лечения. Часто их единственным проявлением становится внезапная сердечная смерть. К этой группе относится синдром Бланда-Уайта-Гарланда.
Аномальное отхождение левой коронарной артерии от легочной артерии (ALCAPA — anomalous origin of the left coronary artery from the pulmonary artery), или синдром Бланда-Уайта-Гарланда (СБУГ), относится к редким врожденным порокам сердца (1 на 300 тысяч новорожденных) и составляет 0,25 % от всех ВПС.
СБУГ относится к гемодинамически значимым («большим») аномалиям коронарных артерий (КА). В 5% случаев сопровождает другие ВПС: открытый артериальный проток, дефект межжелудочковой или межпредсердной перегородки, тетраду Фалло, коарктацию аорты. Без должного лечения прогноз неблагоприятный. Средний возраст появления угрожающих жизни состояний при СБУГ составляет 33 года, а внезапной сердечной смерти — 31 год. Женщины болеют чаще.
Анатомическое описание порока впервые дал в 1911 году русский патологоанатом А.И. Абрикосов, описавший вскрытие 5-месячного ребенка с аневризмой левого желудочка. Исчерпывающее описание синдрома впервые дали E. Bland, P. White и J. Garland, работавшие в Массачусетской больнице общего профиля, в 1933 году.
Они описали случай 3-месячного ребенка с прогрессирующими проблемами с кормлением, кардиомегалией, выявленной при рентгенографии грудной клетки, и ЭКГ-признаками поражения левого желудочка. На вскрытии было обнаружено, что левая коронарная артерия (ЛКА) отходила от легочной артерии (ЛА). Эффективное лечение этой патологии нашлось только в 1960 году, когда Sabiston et al. показали наличие ретроградного тока крови из ЛКА в ЛА. Лигирование аномальной ЛКА в месте отхождения от ЛА спасло жизнь больному ребенку.
Аномальное отхождение ЛКА от ЛА возникает в эмбриогенезе в результате нарушения разделения конотрункуса перегородкой на аорту и ЛА или сочетания персистирования эндокардиальных подушек в легочной артерии и их дефективной инволюции в аорте. Генетические предпосылки заболевания не изучены. Предполагают, что причиной могут служить мутации в генах CFTR (трансмембранный регулятор муковисцидоза), MEN1 (множественная эндокринная неоплазия типа 1) и PKP2 (плакофилин-2).
Клиническая картина СБУГ
Спектр клинических проявлений СБУГ многообразен. Различают инфантильный и взрослый типы заболевания.
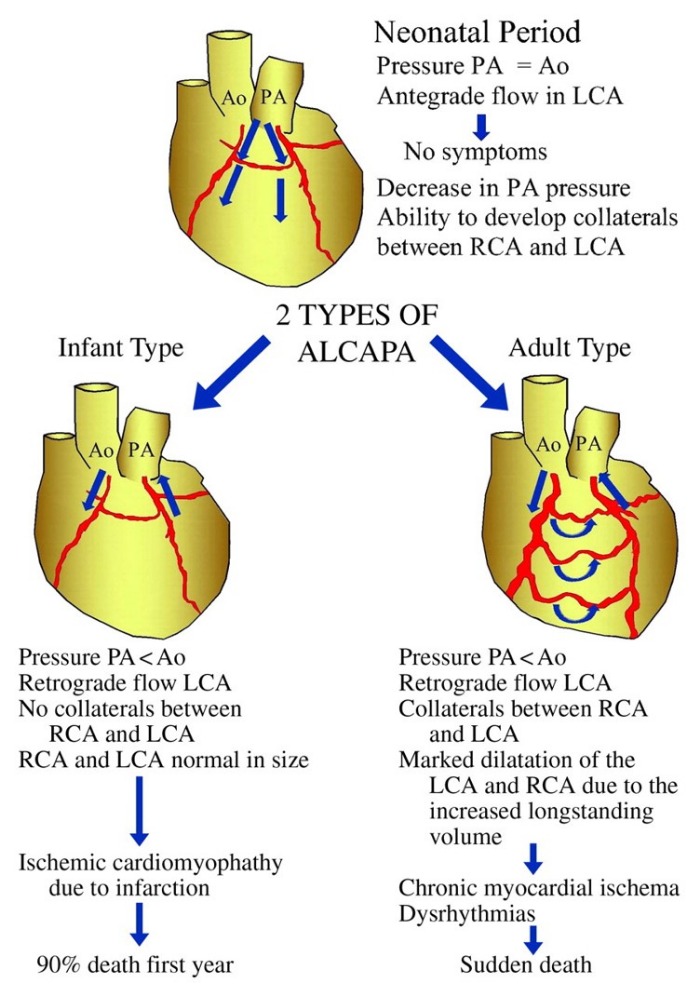 Рисунок 1 | Классификация СБУГ. Источник: Peña E. et al. ALCAPA syndrome: not just a pediatric disease //Radiographics. – 2009
Рисунок 1 | Классификация СБУГ. Источник: Peña E. et al. ALCAPA syndrome: not just a pediatric disease //Radiographics. – 2009
При инфантильном, или летальном, типе СБУГ (85–90 % случаев) симптомы манифестируют обычно на втором месяце жизни. Новорожденные выглядят здоровыми, поскольку относительно высокое сопротивление ЛА пока еще поддерживает антероградный ток крови по аномальной ЛКА, а фетальный гемоглобин обеспечивает миокард кислородом. На 1–2 месяце жизни ребенка сопротивление сосудистого русла легких падает в связи с закрытием артериального протока, что ведет к уменьшению антероградного тока крови и перфузии миокарда.
Классические симптомы (приступы беспокойства, плача, колик, одышки, бледность, цианоз, потливость, срыгивание, сложности с кормлением), описанные Bland et al. в 1933 г., позволяют заподозрить патологию коронарных артерий. Как правило, приступы беспокойства возникают после или во время кормления или плача, когда повышается потребность миокарда в кислороде, и длятся несколько минут. Между приступами ребенок выглядит здоровым. Больные дети отстают в физическом развитии.
При осмотре обнаруживается расширение сердечной тупости, сердечный горб, аускультативно нормальные тоны и отсутствие шумов либо выслуживаются шум митральной регургитации, ритм галопа, изредка, чаще на 2–3 году жизни, мягкий непрерывный шум в верхних отделах по левому краю грудины, напоминающий шум у больных с коронарной фистулой или открытым артериальным протоком, усиление II тона над ЛА при развитии легочной гипертензии, гепатомегалия. Со временем из-за недостаточного развития коллатералей развиваются инфаркты переднебоковой стенки ЛЖ, недостаточность митрального клапана и хроническая сердечная недостаточность.
В ряде случаев регургитация на МК может маскировать проявления основного порока, что может привести к диагностической ошибке и неадекватной хирургической тактике. При отсутствии хирургической коррекции в 90 % случаев смерть наступает в течение первого года жизни.
Если у больного доминирует правый тип кровоснабжения сердца и имеется сеть многочисленных хорошо развитых межсосудистых анастомозов в системе коронарных артерий, симптомы могут отсутствовать или проявляться незначительно, и заболевание переходит во взрослый тип (10–15 % случаев). Некоторые взрослые пациенты с СБУГ не испытывают недомогания, но значительно чаще аномалия проявляет себя одышкой, сердцебиением, обмороками, стенокардией, легочной гипертензией, кардиомиопатией, желудочковыми аритмиями и внезапной сердечной смертью. Симптомы не всегда связаны с физической активностью и могут внезапно возникать в покое, результаты функциональных проб часто ложноотрицательные, что затрудняет диагностику.
Из-за развития большого числа коллатералей происходит шунтирование крови из правой коронарной артерии (ПКА) в ЛКА и ЛА и наблюдается феномен обкрадывания. В отдельных случаях СБУГ не проявляется до более позднего возраста (старше 30 лет), что объясняется адаптацией не только к хронической ишемии участка миокарда, кровоснабжаемого ЛКА, но и к шунтированию крови. Предполагается, что адаптация происходит благодаря:
- обеспечению перфузии ЛЖ из ПКА по коллатералям между ПКА и ЛКА;
- уменьшению территории миокарда, зависящей от ЛКА, в результате доминирования ПКА;
- уменьшения шунтирования крови из артериального в венозное русло из-за появления со временем стеноза устья ЛКА;
- развития коллатералей бронхиальных артерий, обеспечивающих перфузию ишемизированного миокарда.
Однако обычно адаптации не обеспечивают достаточное кровоснабжение ЛЖ и развивается хроническая субэндокардиальная ишемия миокарда, увеличивающая риск возникновения злокачественных желудочковых аритмий. В 80–90 % случаев СБУГ наступает внезапная сердечная смерть. Изначально считалось, что причиной внезапной сердечной смерти является гипоплазия КА, изгиб или перегиб проксимального эктопического сегмента КА (отходящего по касательной от аорты), острый угол отхождения и щелевидная или заслончатая форма устья КА, ход артерии между аортой и легочной артерии, что приводит к сдавлению («ножницы»).
P. Angelini выделяет несколько механизмов стеноза КА:
• Коронарная гипоплазия
Интрамуральный инвагинированный сегмент проксимальной эктопической артерии меньше в окружности, чем более дистальные экстрамуральные сосуды. Автор предлагает в качестве ценного количественного параметра индекс гипоплазии (отношение длин окружностей интрамурального сегмента и более дистального на внутрисосудистом УЗИ). Врожденный ход артерии в медии аорты скорее приводит к ненормальному росту КА до и после рождения.
• Латеральная компрессия
На поперечном разрезе интрамуральный сегмент имеет овоидную, а не круглую форму. Латеральное сдавливание уменьшает площадь по сравнению с площадью сечения круглого на разрезе сосуда с той же длиной окружности. Латеральное сдавливание характеризуется коэффициентом асимметрии (отношение меньшего диаметра к большему при внутрисосудистом УЗИ). В систолу диаметр еще больше уменьшается.
Таким образом, заподозрить у пациента СБУГ можно при наличии необъяснимой кардиомегалии, митральной недостаточности или стойкого систолического шума над областью сердца.
Инструментальная диагностика СБУГ
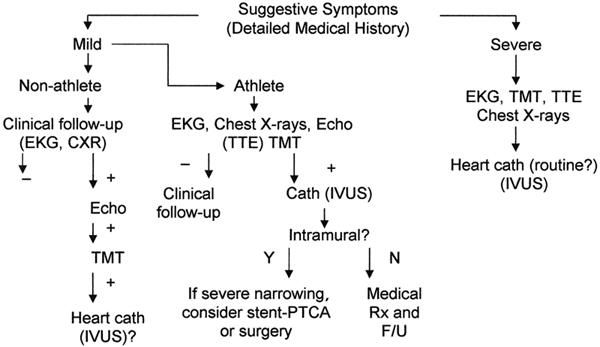
Рисунок 2 | Предлагаемый диагностический протокол для взрослых пациентов с риском развития аномалий коронарных артерий. Источник: Angeline P. Coronary artery anomalies—current clinical issues //Tex Heart Inst J. – 2002
В 80–90 % диагноз СБУГ устанавливается на вскрытии. Наиболее актуальна скрининговая диагностика аномалий коронарных артерий для спортсменов и военнослужащих. Согласно данным Американского Национального регистра внезапной смерти среди спортсменов аномалии КА являются второй по частоте причиной внезапной сердечной смерти (17 %), уступая лишь гипертрофической кардиомиопатии. Сообщается, что функциональные пробы и радионуклидные методы часто не выявляют временную ишемию у спортсменов с аномалиями КА. От 55 % до 93 % пациентов, умерших от внезапной сердечной смерти, вызванной аномалиями КА, не имели ранее кардиологической симптоматики и менее 10 % из них обращались к кардиологу с симптомами, связанными с аномалией.
Прямым указанием на СБУГ служит визуализация ЛКА, отходящей от легочного ствола (чаще всего от его левой нижнелатеральной части сразу за клапаном ЛА). Далее ЛКА следует по межжелудочковой борозде и распадается на левую переднюю нисходящую и огибающую артерии. Косвенными признаками СБУГ являются извитость КА, расширенная ПКА, множественные расширенные коллатерали между ПКА и ЛКА, гипертрофия и дилатация ЛЖ, миксоматозная дегенерация и ишемическая дисфункция папиллярных мышц, гипокинез стенки ЛЖ, расширенные бронхиальные артерии.
Диагностической процедурой выбора для диагностики СБУГ является коронарография с инъекцией в корень аорты, однако из-за анатомических особенностей устья аномальной ЛКА не всегда удается визуализировать ее ход. Аортография используется для лучевой диагностики у детей младше одного года, коронарография – у детей старше 5 лет. Процедура чревата осложнениями, среди которых часто встречаются временные изменения на ЭКГ (11 %), временная брадикардия (2,5 %), сосудистые нарушения (11,6 %) и такие серьезные осложнения, как желудочковая фибрилляция (0,6 %).
Большинство диагнозов СБУГ основаны на данных эхокардиографии с цветовым допплеровским картированием. ЭхоКГ позволяет избежать осложнений коронарографии и оценить дисфункцию МК. Дополнительные исследования проводятся при невозможности установить точный диагноз на ЭхоКГ или для дифференциальной диагностики. Трансторакальная ЭхоКГ используется у детей в связи с наличием хорошего акустического окна (у взрослых более чувствительна чреспищеводная ЭхоКГ).
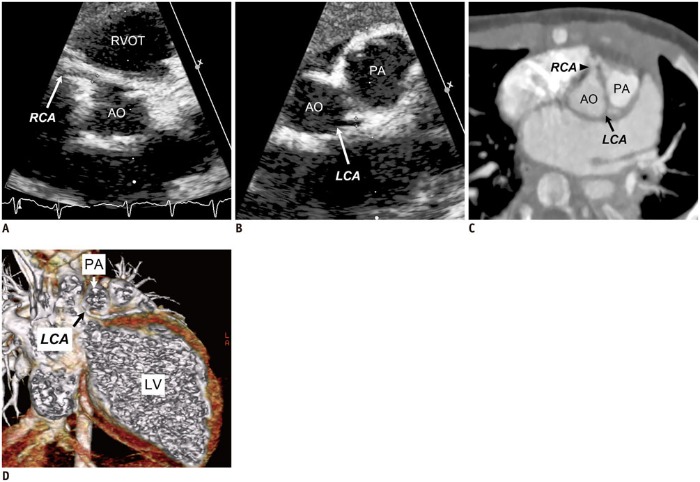
Источник: Goo H. W. Coronary artery imaging in children //Korean journal of radiology. – 2015
МРТ сердца дает дополнительную информацию о направлении тока крови в ЛКА (кино-МРТ с последовательностью SSFP), состоянии клапанов, миокарда, местной сократимости, сопутствующих пороках, которая важна для предоперационной оценки и послеоперационного наблюдения за пациентами. При исследовании пациент не подвергается ионизирующему облучению, что важно в педиатрии. МРТ сердца используется для обнаружения субэндокардиальной ишемии и фиброза миокарда, который может стать субстратом для возникновения летальных аритмий, при этом получают изображения с усилением в отложенную фазу после инъекции гадолиния.
На ЭКГ-синхронизированной МСКТ-ангиографии лучше, чем на МРТ, визуализируется не только аномальная ЛКА, но и расширенная и извитая ПКА, множественные межкоронарные коллатеральные сосуды, расширенные бронхиальные артерии.
Радионуклидные методы визуализации сердца позволяют оценить перфузию миокарда и функциональное значение аномалии КА. К ним относятся нагрузочная сцинтиграфия с таллием, однопротонная эмиссионная компьютерная томография и позитронная эмиссионная томография. Однопротонная эмиссионная КТ (ОПЭКТ)-МРТ и позитронная эмиссионная томография (ПЭТ)-МРТ выявляют ишемию миокарда у асимптоматических пациентов и пациентов с симптомами. При гибридном КТ-коронарография/ОПЭКТ-МРТ исследовании удается обнаружить нарушения кровотока в кровоснабжаемых КА участках даже при отсутствии дефектов перфузии. На решение об оперативном вмешательстве радионуклидные методы в целом не влияют и не используются при обследовании большинства пациентов.
Нередко первым признаком СБУГ являются нарушения ритма, представляющие риск развития внезапной сердечной смерти. Тем не менее, ЭКГ-признаки гипертрофии и перегрузки левых отделов сердца отмечают у всех пациентов с СБУГ. Перспективными в диагностике ишемии миокарда ЛЖ у данной категории больных могут быть поверхностное ЭКГ-картирование и метод 12-канального холтеровского мониторирования, помогающий выявить транзиторные периоды ишемии миокарда, даже при отрицательных результатах других нагрузочных проб.
ЭКГ у младенцев с СБУГ обычно указывает на переднебоковой инфаркт ЛЖ, признаками которого являются аномальные зубцы Q и временные изменения интервала ST в отведениях I, aVL, V5 и V6. У 20–45 % пациентов отсутствуют аномалии зубца Q и на мысль о СБУГ может навести аномальный прирост зубца R в грудных отведениях.
Различают временные, связанные с текущим повреждением, и более длительные, связанные с исчезновением мышечной ткани, изменения на ЭКГ. Первыми признаками повреждения являются заостренные зубцы Т, свидетельствующие о локальной гиперкалиемии, которые исчезают через несколько часов и часто не обнаруживаются. Затем последовательно появляются изменения сегмента ST, элевация точки J с сегментом ST вогнутой формы и дальнейшая элевация точки J с выпучиванием сегмента ST.
Иногда наблюдается реципрокная депрессия сегмента ST в отведениях II, III, aVF и даже V1 и V2. Признаками исчезновения мышечной ткани являются появление зубца Q и уменьшение амплитуды зубца R в затронутых отведениях. В течение последующих двух недель сегмент ST становится изоэлектрическим, зубец Т — инвертированным и симметричным, уменьшается амплитуда зубца R, углубляется зубец Q. Единственными ЭКГ-признаками переднебокового инфаркта после окончания острой фазы являются аномальные зубцы Q и R.
Вышеперечисленные изменения неспецифичны и характерны для острого миокардита и дилатационной кардиомиопатии, однако одновременное наличие следующих четырех ЭКГ-признаков присуще только СБУГ и позволяет провести дифференциальную диагностику:
- зубец Q выше 0.3 мВ (3 мм);
- ширина зубца Q больше 30 мс;
- qR-комплекс по крайней мере в одном из отведений: I, aVL, V5 и V6. Отсутствие зубцов Q во всех нижних отведениях (II, III, aVF).
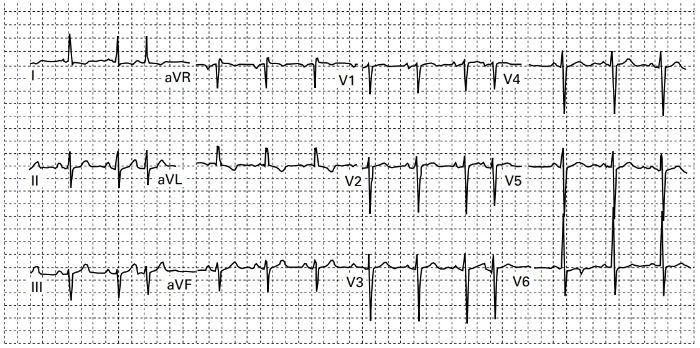 Рисунок 4 | ЭКГ женщины 72-х лет с ALCAPA. Источник: Fierens C. et al. A 72 year old woman with ALCAPA //Heart. – 2000. – Т. 83. – №. 1. – С. e2-e2
Рисунок 4 | ЭКГ женщины 72-х лет с ALCAPA. Источник: Fierens C. et al. A 72 year old woman with ALCAPA //Heart. – 2000. – Т. 83. – №. 1. – С. e2-e2
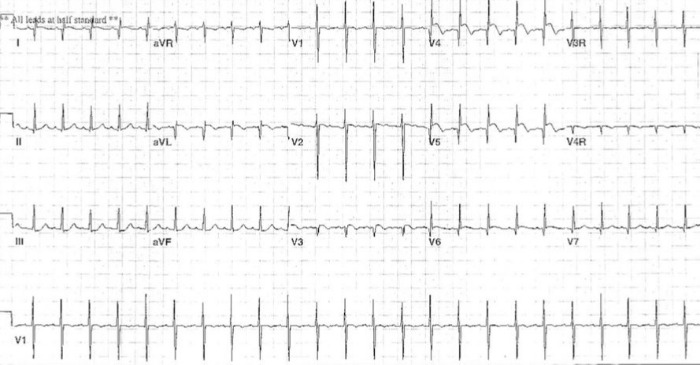
Рисунок 5 | ЭКГ ребенка 3-х месяцев с ALCAPA. Источник: Hoffman J. I. E. Electrocardiogram of anomalous left coronary artery from the pulmonary artery in infants //Pediatric cardiology. – 2013
Данные изменения встречаются в 55–80 % случаев СБУГ. Причины отсутствия аномальных зубцов Q недостаточно ясны, однако у взрослых пациентов оно ассоциировано больше с субэндокардиальным инфарктом, чем с трансмуральным; больше с нижним, чем с передним; больше с мелкоочаговым, чем крупноочаговым. Стоит отметить и новые, но пока не получившие широкого применения, методы диагностики, например внутрисосудистое УЗИ и измерение интракоронарного давления с определением ФРК.
Дифференциальную диагностику СБУГ проводят с миокардитом, болезнью Кавасаки, васкулитами (узелковым полиартериитом или артериитом Такаясу), склеродермией, синдромом Элерса-Данло, наследственной геморрагической телеангиэктазией, дилатационной кардиомиопатией, врожденной недостаточностью МК, стенозом и коарктацией аорты.
Лечение СБУГ
Синдром Бланда-Уайта-Гарланда является абсолютным показанием к хирургическому лечению.
Выживаемость спустя 20 лет после операции, проведенной в младенчестве, составляет 95 %. Скудные данные о хирургическом лечении взрослых пациентов, переживших внезапную сердечную смерть, также выглядят многообещающими, однако до сих пор не проведено рандомизированных контролируемых исследований для оценки долгосрочных результатов разных способов коррекции порока.
В 1960 г. Sabiston et al., сотрудники Johns Hopkins Hospital, описали лечение 2,5-месячного ребенка с СБУГ. У ребенка наблюдались трудности при кормлении, одышка и звуки хрюканья. Рентгенография грудной клетки выявила кардиомегалию, на ЭКГ были признаки свежего повреждения миокарда. Катетеризация сердца выявила дилатацию и дисфункцию ЛЖ, аномальная ЛКА не визуализировалась. После полного обследования было принято решение о хирургическом вмешательстве с целью реваскуляризации ЛЖ. В ходе операции был обнаружен инфаркт миокарда и аномальная ЛКА.
С целью определить направление кровотока по аномальной КА Sabiston et al. измерили систолическое давление в ЛА и ЛКА, которое составило 25 и 30 мм рт.ст. соответственно. При окклюзии аномального сосуда в месте отхождения от ЛА давление в нем возросло до 75 мм рт.ст., обеспечив ретроградный кровоток по коллатералям. Сатурация кислородом в ЛКА составляла 100 %, в ЛА — 76 %, что также свидетельствовало о наличии кровотока по коллатералям. Sabiston et al. рекомендовали наложение лигатуры на аномальную ЛКА как эффективный метод лечения патологии.
В последние десятилетия были предложены несколько способов хирургического лечения СБУГ. Простое наложение лигатуры на аномальную артерию в месте ее отхождения от ЛА, описанное Sabiston et al., при своей эффективности оказалось чревато серьезными ранними и поздними осложнениями по той причине, что после наложение лигатуры коронарное кровоснабжение сердца обеспечивается только ПКА и целиком зависит от степени развития коллатералей. В 1966 г. Cooley et al. сообщили о способе создания двухкоронарной системы кровоснабжения миокарда. Создав с помощью протеза из дакрона сообщение между аортой и ЛКА, они восстановили прямой антероградный кровоток в ЛКА. В последующие годы были предложены другие способы создания двухкоронарной системы — шунтирование подкожной веной, внутренней грудной артерией, левой подключичной артерией.
Доказанными осложнениями перечисленных методов хирургической коррекции являются реканализация аномальной КА, увеличение риска атеросклероза, тяжелая ишемическая митральная регургитация. Более современные методы не несут за собой такие риски.
Современный способ хирургической коррекции СБУГ основан на предложенной в 1974 г. Neches et al. прямой имплантации ЛКА в аорту. Устье аномальной ЛКА выделяется из ЛА вместе с небольшим лоскутом ЛА и подсоединяется к корню аорты с формированием двухкоронарной системы. Описанный способ является операцией выбора при СБУГ. Послеоперационная летальность составляет 0–16 % в зависимости от степени дооперационного повреждения миокарда. Главным осложнением может стать тяжелая кровопотеря из-за разрыва аномальной артерии при пересадке. У взрослых прямая имплантация ЛКА часто невозможна из-за ригидности ткани и большим расстоянием от устья ЛКА до аорты. В этих случаях предпочтительным является шунтирование аномальной ЛКА с использованием артериального и венозного трансплантата. При этом риск стеноза пересаженного сосуда выше при использовании венозного трансплантата. Трансплантат подкожной вены сохраняет проходимость в среднем на 80 % в течение 5–8 лет.
При наличии противопоказаний к прямой имплантации ЛКА в аорту с 1979 г. применяется операция Takeuchi. Она заключается в создании тоннеля внутри ЛА (аортопульмонарного окна), через который аорта сообщается с устьем аномальной ЛКА. Данный метод ассоциирован с высокой частотой надклапанного стеноза легочной артерии и обструкции тоннеля.
Пациентам с необратимым, несмотря на коррекцию с формированием двухкоронарной системы, повреждением миокарда показана трансплантация сердца. У пациентов с высоким риском возникновения желудочковых фибрилляций (пациенты с ишемической кардиомиопатией и низкой фракцией выброса) возможно использование имплантируемого кардиовертера-дефибриллятора.
Источники:
- Yamanaka O., Hobbs R. E. Coronary artery anomalies in 126,595 patients undergoing coronary arteriography //Catheterization and cardiovascular diagnosis. – 1990. – Т. 21. – №. 1. – С. 28-40.
- Angelini P. Coronary artery anomalies: an entity in search of an identity //Circulation. – 2007. – Т. 115. – №. 10. – С. 1296-1305.
- Angelini P. Coronary artery anomalies—current clinical issues //Tex Heart Inst J. – 2002. – Т. 29. – С. 271-278.
- Клинические рекомендации по ведению детей с врожденными пороками сердца / Под ред. Бокерия Л.А. — М.: НЦССХ им. А.Н. Бакулева; 2014. — 342 с.
- Peña E. et al. ALCAPA syndrome: not just a pediatric disease //Radiographics. – 2009. – Т. 29. – №. 2. – С. 553-565.
- Quah J. X. et al. The management of the older adult patient with anomalous left coronary artery from the pulmonary artery syndrome: a presentation of two cases and review of the literature //Congenital heart disease. – 2014. – Т. 9. – №. 6. – С. E185-E194.
- Alsara O. et al. Surviving sudden cardiac death secondary to anomalous left coronary artery from the pulmonary artery: a case report and literature review //Heart & Lung: The Journal of Acute and Critical Care. – 2014. – Т. 43. – №. 5. – С. 476-480.
- Cowles R. A., Berdon W. E. Bland-White-Garland syndrome of anomalous left coronary artery arising from the pulmonary artery (ALCAPA): a historical review //Pediatric radiology. – 2007. – Т. 37. – №. 9. – С. 890-895.
- Hoffman J. I. E. Electrocardiogram of anomalous left coronary artery from the pulmonary artery in infants //Pediatric cardiology. – 2013. – Т. 34. – №. 3. – С. 489-491.
- Hekim N. et al. Whole exome sequencing in a rare disease: A patient with anomalous left coronary artery from the pulmonary artery (Bland-White-Garland Syndrome) //Omics: a journal of integrative biology. – 2016. – Т. 20. – №. 5. – С. 325-327.
- ВКонтакте
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
- Telegram
