Вопрос цены: противоопухолевые препараты
Противоопухолевые препараты неприлично дороги, но этой проблемой занимаются.
В Соединенных Штатах 2011 год стал переломным для лечения рака. В течение пяти месяцев FDA одобрило первую иммунотерапию на основе ингибитора контрольных точек, первый метод лечения агрессивной формы рака щитовидной железы, первый персонализированный препарат против меланомы, первый препарат из инновационного класса препаратов направленного действия для лечения рака легких, и «убийственную» терапию лимфомы антителами, при которой препарат доставляется непосредственно к опухолевым клеткам.
Потенциальные возможности, сложность и инновационный характер этих методов лечения, несомненно, заслуживали внимания. Как и цена. Годичный курс каждого из препаратов обходился более чем в $100 000 (6,5 млн. ₽) на человека — в то время редкость для онкологических препаратов.
Цены ошеломляли как врачей и пациентов, так и администрацию медицинских учреждений. Однако вскоре подобные расценки стали нормой. К 2014 году средняя стоимость нового перорального противоопухолевого препарата составила $135 000 (8,8 млн. ₽) за годичный курс, что почти в шесть раз превышало стоимость аналогичных препаратов, одобренных в начале 2000-х годов (с поправкой на инфляцию) [1]. В 2017 году был установлен самый умопомрачительный «рекорд» стоимости препарата в онкологии: стоимость одного курса персонализированной клеточной терапии на одного ребенка, больного лейкозом, составила $475 000 (31 млн. ₽).

Новое поколение лекарств обещает изменить лечение рака, обеспечив большую частоту полного излечения и долговременной ремиссии, чем прежде. Но, хотя ученые разрабатывают все более эффективные методы борьбы с опухолями, докторам не всегда удается обеспечить доступность этих благ.
Если в ближайшее время не будет обеспечена доступность лекарств, многие пациенты с онкологическими заболеваниями не смогут воспользоваться передовыми методами лечения. «При нынешних ценах противоопухолевая терапия становится неподъемной», — говорит Амит Сарпатвари (Ameet Sarpatwari), эпидемиолог и юрист, изучающий ценообразование рынка лекарств, из женской больницы имени Брайама в Бостоне, штат Массачусетс.
«Это действительно серьезная проблема», — утверждает Сабина Фоглер (Sabine Vogler), экономист в сфере здравоохранения из Австрийского института общественного здоровья в Вене. Во многих регионах препараты стоят слишком дорого [2]. «Мы должны спросить себя, — говорит Фоглер, — как долго еще мы сможем платить такую высокую цену?»
Стратегии сдерживания
В области терапии рака дорожают не только новые лекарства. Цена на лечение связана с заработной платой докторов, стоимостью диагностики, радиотерапии и хирургии — а они только растут, утверждает Дариус Лейкдеуолла (Darius Lakdawalla), экономист в сфере здравоохранения из Университета Южной Калифорнии в Лос-Анджелесе. Вместе взятые, они продолжают обуславливать львиную долю стоимости лечения от рака. «Это системная проблема», — говорит эксперт.
Так же считает и Даниэль Голдштейн, онколог и экономист в сфере здравоохранения из Медицинского центра имени Ицхака Рабина в Петах-Тиква, Израиль. Его коллеги в прошлом году сообщили о резком росте стоимости уже существующих противоопухолевых препаратов, намного превышающем уровень инфляции и значительно более быстром по сравнению с другими показателями в области здравоохранения [3]. Такой «разгон цен», как его называет Голдштейн, вредит пациентам, поскольку многие из них откладывают неподъемное лечение или вовсе отказываются от него. Это лишь увеличивает общую стоимость лечения, говорит Сарпатвари, поскольку больным, которые не принимают лекарства по установленному расписанию, с большей вероятностью потребуется госпитализация на поздних стадиях заболевания. По его словам, «если люди в состоянии приобрести себе лекарство, это может уменьшить последующие расходы».
Ускорение роста цен началось с Соединенных Штатов, где стоимость препарата «не обусловлена соображениями целесообразности», утверждает Винай Прасад, онколог из Орегонского университета науки и здоровья в Портленде. Он предполагает, что это позволяет фармацевтическим компаниям взимать непомерные суммы за новые методы лечения, которые часто не намного лучше более старых и более дешевых вариантов. И хотя другие страны обычно могут договориться о скидке, стоимость, в которую обходится препарат, все равно зависит от его цены в США. «То, что происходит в Америке, действительно влияет на остальной мир», — говорит Гольдштейн.
Один из способов снижения цен — связать их уровень с получаемым клиническим результатом. Питер Бах (Peter Bach), терапевт и специалист в области ценообразования противоопухолевых препаратов из Мемориального онкологического центра имени Слоуна-Кеттеринга в Нью-Йорке, разработал калькулятор для расчета цены на препарат сообразно его эффективности: DrugAbacus. Этот онлайн-инструмент позволяет пользователям рассчитать цену на препарат на основе собственных взглядов на относительную важность таких факторов, как переносимость, новые механизмы действия, затраты на исследования и разработки, редкость болезни, а также на основе предполагаемой оценки года жизни в денежном эквиваленте. При разумных экономических предположениях DrugAbacus показывает, что в Соединенных Штатах цены завышены на 80–85 % онкологических препаратов (см. «Втридорога»).
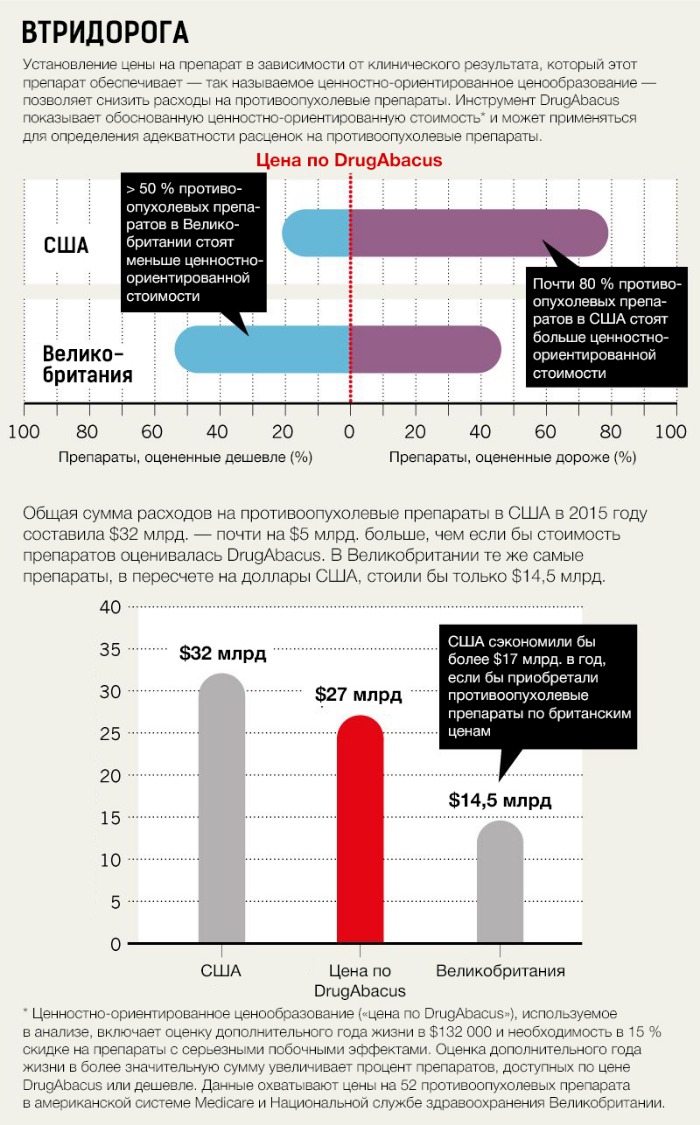
В большинстве стран с государственной системой здравоохранения уже существует система ценностно-ориентированного ценообразования, но даже в этом случае имеются лазейки. Например, в Англии в период с 2010 по 2016 год Национальная служба здравоохранения вложила почти £1,3 млрд. ($1,8 млрд., 117 млрд. ₽) в Фонд по борьбе с раковыми заболеваниями, созданный для улучшения доступа к инновационным методам лечения. Вся эта уйма денег в конечном итоге была использована для оплаты медикаментов, которые не счел рентабельными страж цен на препараты — Национальный институт здравоохранения и совершенствования медицинской помощи (National Institute for Health and Care Excellence, NICE).
Анализ [4], проведенный в 2017 году Ричардом Салливаном (Richard Sullivan), директором Института по вопросам рака в Королевском колледже Лондона, и его коллегами, показал, что фонд «не принес значимой пользы пациентам или обществу». С тех пор оплата лекарств, отклоненных NICE, прекратилась, хотя она по-прежнему покрывает препараты, для которых оценка Института была неубедительна и требовала дальнейшего получения данных.
Альтернативное предложение по сокращению затрат заключается в гарантии возврата денег. При таких условиях за препарат должны платить только те пациенты, которым он помог. Такая «плата за успех» может исключить избыточные расходы на лекарства, не помогающие многим людям. Однако на практике этот метод пока мало применялся.
Лучшие данные по такой схеме получены от AIFA, итальянского агентства по лекарственным средствам, которое в 2006 году ввело возмещение стоимости 25 противоопухолевых препаратов. Два независимых анализа [5, 6] показали, что данная схема приносит весьма небольшую выгоду. Однако гарантии возврата денег «все еще существуют, несмотря на их низкую результативность», — говорит Ливио Гараттини (Livio Garattini), экономист в сфере здравоохранения из Института фармакологических исследований Марио Негри в Бергамо, Италия.
Некоторые фармацевтические компании также начинают предлагать такую гарантию на добровольной основе. Например, «Novartis» из Базеля, Швейцария, гарантирует, что люди, принимающие тисагенлеклейсел, продаваемый под названием «Kymriah» (читается как «Кимрайя» — прим.перев.) — препарат от лейкемии стоимостью $475 000 (31 млн. ₽), — могут получить полный возврат средств при отсутствии улучшения в первые 30 дней после лечения.
«Мы с гордостью предлагаем этот подход, поскольку исходы терапии препаратом „Kymriah“ беспрецедентны для этого типа заболеваний», — говорит Эрик Альтхофф (Eric Althoff), глава отдела по связям со СМИ в компании «Novartis». Он цитирует независимые анализы NICE и Института клинико-экономической экспертизы в Бостоне, а также данные экономистов «Novartis», чтобы показать, экономическую эффективность цены (даже без скидки!) для систем здравоохранения. «Мы признаем нашу ответственность за обеспечение доступа пациентов к препарату, а также необходимость целостного, доказательного подхода, который включает результаты клинических исследований, опыт пациентов, выгоду для системы здравоохранения и ценность для общества», — говорит Альтхофф.
Однако Голдштейн не придает значения подобным гарантиям и расценивает их как рекламный трюк, а не как реальный способ сокращения расходов. Он указывает на то, что лечение не дает результаты в первый месяц примерно у 20 % пациентов и это приводит к тому, что средняя стоимость препарата на одного человека после возмещения составляет около $380 000 (25 млн. ₽). Это сопоставимо с ценой на препарат со сравнимой эффективностью от «Gilead Sciences» в Фостер-Сити, Калифорния, который был одобрен в Соединенных Штатах через несколько недель после «Kymriah» и на момент публикации стоит $373 000 (24 млн. ₽) на одного пациента, но без гарантии возврата денег.
«Это становится упражнением в математике», — говорит Гольдштейн. «Стоимость гарантии включается в общий чек. В общем, это всего лишь трюк».
Государственное вмешательство
Чтобы снизить цены на лекарства, можно было бы предпринять более радикальные шаги, даже в Соединенных Штатах, где здравоохранение — сфера преимущественно частная и децентрализованная. Согласно федеральному закону, правительство США имеет право приобретать непатентованные версии препаратов (т. н. «дженерики») в обмен на «разумные» отчисления в качестве компенсации патентообладателям.
Согласно анализу [7], проведенному в 2017 году Ханной Бреннан (Hannah Brennan) и ее коллегами из Юридической школы Йельского университета в Нью-Хейвене, штат Коннектикут, в 1960-х и начале 1970-х годов Министерство обороны США использовало данный закон для получения антибиотиков и других препаратов со значительными скидками. И одной угрозы повторения подобной ситуации оказалось достаточно, чтобы обуздать чрезмерное ценообразование на препараты: при угрозе распространения сибирской язвы в 2001 году фармацевтическая компания избежала государственного вмешательства, вдвое снизив цены на препарат против этой инфекции.
«Пришло время пересмотреть вопрос о том, каким образом правительство предоставляет лекарства», — говорит Бреннан, в данный момент юрист в фирме по защите прав потребителей «Hagens Berman Sobol Shapiro» в Кембридже, штат Массачусетс. «Если фармацевтические компании намерены продолжать формировать ценник и полностью отказывать государству в любом вмешательстве», — добавляет она, — «тогда это правильный и пропорциональный ответ».
Правительства стран Европейского Союза могут вести переговоры с фармацевтическими компаниями об установлении цен, но они, как правило, делают это изолированно, «что ослабляет покупательную способность», — говорит Фоглер. Для решения этой проблемы некоторые страны ЕС объединились в единый фронт, противостоящий фармацевтическим компаниям. Один из таких союзов сформировали Нидерланды, Бельгия, Австрия и Люксембург. Полдесятка средиземноморских стран надеются сделать то же самое.
Но даже когда фармацевтические компании предлагают большие скидки, во многих уголках планеты противоопухолевые препараты остаются недоступными. Например, в некоторых регионах Африки швейцарский фармацевтический гигант Roche сотрудничает с правительствами и группами пациентов с целью предоставлять препарат трастузумаб (Герцептин) для лечения рака молочной железы со скидкой 50 %. Такая скидка оказалась достаточной для того, чтобы в 2016 году правительство Кении согласилось обеспечить препаратом небольшую группу людей. В прошлом году министерство здравоохранения страны выделило на лечение от рака около 20 миллионов кенийских шиллингов ($195 000, 12,5 млн. ₽).
Однако цены все еще оставались слишком высокими для правительства гораздо более бедной Руанды. Даже после 50 % уступки цена «все еще выходит за рамки того, что они могут себе позволить», — говорит Лоуренс Шульман (Lawrence Shulman), директор Центра мировой онкологической медицины в Онкологическом центре Абрамсона Университета Пенсильвании в Филадельфии, работающий в странах Восточной Африки.
Стремясь оказать давление на фармацевтические компании с целью обеспечения доступности дорогостоящих лекарств для всех людей в странах с низким и средним уровнем дохода — как это произошло с препаратами против ВИЧ в 2000-х годах, — Шульман и международная команда ведущих исследователей-онкологов в сотрудничестве со Всемирной организацией здравоохранения (ВОЗ) в 2015 году расширили список лекарственных препаратов первой необходимости [8]. Это помогло в июне 2017 подтолкнуть две крупные фармацевтические компании — «Pfizer» из Нью-Йорка и «Cipla» из Мумбаи, Индия, — к договоренности о поставке по предельно низким ценам 16 лекарств, большинство из которых включены в список ВОЗ, а некоторые — поддержаны группой Шульмана, больным в Руанде, Кении и четырех других малообеспеченных африканских странах.
Однако эти препараты — главные элементы химиотерапии и для них доступны непатентованные аналоги. Скидки не предоставлялись ни на трастузумаб, ни на какой-либо другой фирменный препарат из списка. Новейшая терапия по-прежнему ускользает от нуждающихся в ней жителей развивающихся стран, где диагноз «рак» для большинства больных означает мучительную смерть (см. «Дифференциальность диагноза»).
В 2015 году в странах с низким и средним уровнем дохода рак унес жизни 6 миллионов человек — больше, чем ВИЧ, туберкулез и малярия. Ограничение доступа к спасительным препаратам по доступной цене способствует осложнениям и смертности. Но даже если онкологи в этих странах смогут назначать те же препараты, что и их лучше финансируемые западные коллеги, не факт, что это приведет к значительному снижению уровня смертности.
Такая ситуация связана с тем, что, в отличие от жителей более богатых стран, многие больные раком, например, в странах Южной Африки, обращаются за медицинской помощью только после того, как их опухоли метастазируют и, следовательно, прогноз становится плохим независимо от методов лечения. Как считает Дэвид Керр (David Kerr), исследователь в области онкологии из Оксфордского университета в Великобритании, «если мы не можем диагностировать у пациента заболевание на более ранней стадии, любые новые и „крутые“ лекарства будут неэффективны».
Однако раннее выявление заболевания также окажется бесполезным при отсутствии обученных специалистов-онкологов, отмечает Лоренс Шульман, директор Центра мировой онкологической медицины в Онкологическом центре Абрамсона Университета Пенсильвании в Филадельфии — во многих развивающихся странах имеется лишь небольшое число специалистов по лечению рака, если таковые вообще есть.
Чтобы нарастить такой потенциал, Шульман с 2011 года работает с некоммерческой организацией «Partners In Health», базирующейся в Бостоне, штат Массачусетс, для разработки программ лечения рака в Руанде и на Гаити. Также он занимался аналогичной работой в Ботсване.
«Нужны хорошо обученные медсестры. Нужен опытный врач», — говорит Шульман. «Вам нужно получить определенные знания, прежде чем вы сможете стартовать и двигаться вперед».
Требование повышать квалификацию актуально не только в странах с низким уровнем ресурсов. Возрастающая сложность лечения рака означает, что даже в наиболее богатых странах онкологи вынуждены разбираться во многих смежных специальностях, чтобы обеспечить оптимальный исход для пациентов. Вот почему в 2017 году Экспертная группа Европейской комиссии по борьбе с раком (European Commission’s Expert Group on Cancer Control) одобрила рекомендацию о том, что все врачи, участвующие в лечении рака, должны пройти период междисциплинарного обучения.
Терапевты-онкологи, лучевые терапевты и онкологи-хирурги уже сотрудничают в повседневном лечении пациентов. Показано, что работа в таких междисциплинарных командах
повышает точность диагностики и улучшает уход за пациентами.
Однако Йеспер Эриксен (Jesper Eriksen), онколог в больнице Орхусского университета в Дании, возглавлявший группу, давшую европейские рекомендации [11], считает, что возможны еще более значительные улучшения. Он призвал врачей проходить полную подготовку по другим дисциплинам, чтобы повысить результативность встреч с другими специалистами. «Надеюсь, это приведет к сокращению времени между постановкой диагноза и началом лечения», — говорит он.
Одним примечательным исключением является иматиниб (Glivec). Начиная с 2001 года, практически одновременно с одобрением препарата для использования при хроническом миелоидном лейкозе (ХМЛ), «Novartis» предоставляет бесплатное лечение для самых бедных пациентов из развивающихся стран через международную программу «Glivec International Patient Assistance Program». «Этот препарат возвращает людям нормальную жизнь», — говорит Дэвид Эпштейн (David Epstein), бывший исполнительный директор «Novartis», ныне работающий в венчурной фирме «Flagship Pioneering», находящейся в Кембридже, штат Массачусетс.
«Мы чувствовали, что обязаны попытаться обеспечить препаратом всех людей, кому он необходим», — говорит он. По данной программе более чем 50 000 пациентов в 80 странах получили около 2,3 миллиона ежемесячных доз препарата [9].
Основываясь на этом успехе, «Max Foundation» — некоммерческая организация в Сиэтле, штат Вашингтон, которая запускает программу доступа к иматинибу в партнерстве с Novartis — приступила к сотрудничеству с тремя другими производителями ради обеспечения доступа ко всем пяти выпущенным на рынок препаратам против ХМЛ. «Сегодня, если вы живете в наибеднейшей стране мира и у вас диагностирован ХМЛ, вы можете получить доступ к любому лекарству, которое вам нужно», — говорит Пэт Гарсиа-Гонсалес (Pat Garcia-Gonzalez), исполнительный директор фонда.
 Непалец получает противоопухолевые препараты, предоставляемые по программе доступа.
Непалец получает противоопухолевые препараты, предоставляемые по программе доступа.«Моя следующая цель, — добавляет Гарсиа-Гонсалес, — сделать то же самое для всех препаратов в сфере онкологии». Однако на данный момент помощь фонда распространяется только на таргетные методы лечения миеломной болезни и нескольких типов солидных опухолей.
Завтрак съешь сам
Несмотря на то, что большинство предлагаемых поправок в вопросе цены на противоопухолевые препараты были сосредоточены на крупномасштабных системных изменениях, нередко требующих участия правительств, фармацевтической промышленности, врачей и групп пациентов, даже небольшие вмешательства могут привести к значительным изменениям.
Идея, которую выдвинул Марк Ратен (Mark Ratain), директор Центра персонализированной терапии Университета Чикаго, штат Иллинойс, заключается в том, чтобы назначать прием дорогих противоопухолевых препаратов во время еды, а не на пустой желудок, как это показано сейчас. Такая мера, как он надеется, улучшит абсорбцию лекарств, позволяя снизить необходимую дозу и, следовательно, уменьшить стоимость лечения.
Тот факт, что пища способствует поступлению большей дозы препарата в кровоток, установлен для нескольких часто назначаемых противоопухолевых препаратов, включая эрлотиниб, препарат против рака легких, и вемурафениб — против меланомы. Однако на данный момент Ратен проверил свою идею только на абиратероне, препарате против рака предстательной железы.
В ходе разработки абиратерона испытания показали различия концентрации и кинетики препарата между людьми, принимавшими его с пищей, и теми, кто принимал препарат независимо от еды. Затем компания-разработчик препарата Janssen Biotech решила проводить дальнейшие клинические испытания только в условии отсутствия пищи, чтобы минимизировать вариабельность у участников исследования и снизить риск развития осложнений, связанных с диетой.
Такое решение отразилось в рекомендациях по приему абиратерона, который продается под торговым названием Зитига (Zytiga). «Принимайте Зитигу натощак», — говорится в них. «Прием Зитиги с пищей может привести к поступлению в организм большего количества препарата, чем это необходимо, что может вызвать побочные эффекты».
В экспериментальном исследовании [10], в котором приняли участие 72 человека, Ратен и его коллега Рассел Шмулевиц, (Russell Szmulewitz) онколог из Чикагского университета, доказали обоснованность этого предупреждения, продемонстрировав, что в случае приема низких доз препарата одновременно с нежирным завтраком, поглощается такое же количество препарата, как и при приеме полной дозы натощак. Таким образом, участники исследования могли принимать одну четверть нормальной дозы и через 12 недель лечения получить тот же противоопухолевый эффект, который оценивался по изменениям уровня простатспецифического антигена, приблизительного показателя опухолевой нагрузки.
Если результаты будут тщательно проверены, пациенты, принимающие абиратерон, смогут распределять месячный курс препарата, стоимость которого составляет около $9000 (585 тыс. ₽), на четыре месяца. Это может снизить расходы на здравоохранение в США на целых $20 млрд. (1,3 трлн. ₽) в следующем десятилетии, считает Аллен Лихтер (Allen Lichter), бывший исполнительный директор Американского общества клинической онкологии. «Экономия, которую даст всего лишь прием препарата во время завтрака, довольно убедительна», — говорит он.
В прошлом году, вместе с Ратеном и другими учеными, Лихтер стал одним из основателей некоммерческой организации под названием «Value in Cancer Care Consortium» («Консорциум по оценке онкологической помощи»), целью которой является поиск лучших и более дешевых способов применения существующих лекарств. Ученые надеются начать с проведения более крупного исследования, подтверждающего клинические испытания абиратерона, проведенные Ратеном. Однако, по словам Лихтера, консорциум пока пытается собрать $5 млн. (325 млн. ₽), необходимых для обеспечения участия 300 пациентов.
«Между тем существует просто огромное различие между тем, что люди говорят, и тем, что они готовы сделать для того, чтобы добиться успеха», — отмечает Лихтер. «Даже если мы сможем вывести миллиарды долларов из уравнения, это не может не помочь больным раком и системам здравоохранения по всему миру». Он сетует: «Не так много людей ориентированы на клиническую эффективность».
