Гестационная трофобластическая болезнь
Гестационная трофобластическая болезнь (ГТБ) — патология, которая включает в себя пузырный занос (полный и частичный), инвазивный пузырный занос, хориокарционому, трофобластическую опухоль плацентарного ложа и эпителиоидную трофобластическую опухоль. Данные заболевания встречаются не очень часто, однако представляют большую угрозу здоровью и жизни пациенток. В недалеком прошлом летальность от различных форм ГТБ могла достигать практически 100 % (например, в случаях с метастазировавшей хориокарциномой) [1]. И, не смотря на успехи, достигнутые в терапии данного заболевания, необходимо иметь настороженность в отношении ГТБ.
Частичный и полный пузырный занос
Предположительно, данная патология была описана еще в 400 году до н.э. Гиппократом. Но лишь в 1895 году пузырный занос связали с беременностью. Сейчас мы рассматриваем пузырный занос как аномалию беременности, при которой происходит пролиферация трофобласта (и цито-, и синцитиотрофобласта); ворсины хориона разрастаются в виде «пузырьков», и все это сочетается с отсутствием эмбриона/плода. Выделяют две формы пузырного заноса: полный и частичный [2].
Для полного пузырного заноса характерна невозможность определения эмбриона; наблюдается гиперплазия трофобласта с различным уровнем атипии, ворсины лишены сосудов. Формирование «пузырьков» носит генерализованный характер. Практически в 90 % случаев аномальная ткань имеет хромосомный набор 46ХХ, полученный путем дупликации ДНК гаплоидного сперматозоида. Генетический аппарат яйцеклетки дефектен либо неактивен либо вовсе отсутствует. Таким образом, весь генетический материал получен от отца (разумеется, кроме митохондриальной ДНК). В остальных случаях (≈ 10 %) клетки имеют набор 46XY или 46ХХ, который формируется путем слияния двух спермиев [1], [3].
Частичный пузырный занос — патология несколько иного рода. В этом случае возможно обнаружить некоторые ткани эмбриона; ворсины хориона отечны и варьируют по размеру и форме. Ворсины имеют фестончатую форму, из трофобласта образуются выступающие «включения», в ворсинах сохраняется кровоток. Одно из основных отличий частичного пузырного заноса от полного: гиперплазия и образование «пузырьков» носит фокальный характер, атипизм выражен крайне слабо. При этом хромосомный набор — триплоидный, зачастую 69XXY, который формируется путем слияния практически нормальной яйцеклетки и двух спермиев [1], [3].
Важно заметить: после полного пузырного заноса в 15-20 % случаев развивается трофобластическая неоплазия (инвазивный занос или хориокарцинома, см. ниже), тогда как при частичном заносе неоплазии развиваются менее, чем в 5 % случаев [1].
.

Рисунок 1. Полный пузырный занос
Клиническая картина при полном пузырном заносе носит неспецифический характер, симптомы у различных пациенток могут довольно сильно варьировать. Среди наиболее часто встречающихся проявлений следует выделить чрезмерное увеличение матки, анемию, токсемию, гипертиреоидизм и дыхательную недостаточность. Благодаря УЗИ и анализу на ХГЧ, диагностика полного пузырного заноса стала возможной уже в первом триместре, как правило, задолго до появления первых симптомов.
Клиника частичного пузырного заноса «мимикрирует» под картину неразвивающейся беременности. Может наблюдаться маточное кровотечение, при этом размеры матки находятся в пределах нормы [3].
Диагностика осуществляется в основном с помощью УЗИ и анализа на ХГЧ. При полном пузырном заносе хорошо заметна генерализованная гиперплазия, а повышение уровня ХГЧ помогает отличить пузырный занос от замершей беременности. В случае частичного пузырного заноса наиболее специфичными будут фокальные кистозные изменения в плаценте, а также увеличение гестационного мешка в полтора раза (это может свидетельствовать о триплоидии). Сочетание этих двух признаков дает достаточно высокую точность результата.
Уровень хорионического гонадотропина закономерно увеличивается при гиперплазии трофобласта. В случае полного пузырного заноса уровень ХГЧ может достигать 100 000 мЕД/мл и выше; при частичном такие цифры встречаются реже, однако увеличение, тем не менее, определяется также отчетливо [3].
Следует заметить, что окончательно диагностировать полный или частичный пузырный занос может только патологоанатом после гистологической верификации.
Лечение полного и частичного пузырного заносов заключается в удалении аномальной ткани из матки; наиболее оптимальным методом является вакуумная аспирация. Женщинам, которые более не планируют беременность, можно посоветовать гистерэктомию (особенно это оправданно в случае полного заноса) [3].
Однако пузырный занос сам по себе не представляет такой опасности, как возможные неопластические процессы, нередко развивающиеся впоследствии. Как мы помним, после полного пузырного заноса (а иногда и после частичного) могут развиваться хориокарцинома, инвазивный пузырный занос и другие патологические состояния, которые объединяют в группу гестационных трофобластических неоплазий (ГТН).
Для профилактики ГТН ранее даже рекомендовалась химиотерапия. Однако в сейчас такой подход считается неоправданным [4]. Доказательная база у профилактической противоопухолевой терапии достаточно низка, а гипотетическая польза в предотвращении ГТН так и остается лишь гипотетической, тогда как вред — вполне реальным. Потому пациентам с диагностированным пузырным заносом требуется систематическое наблюдение и постоянный мониторинг уровня ХГЧ (его резкое повышение, или «плато» (постоянно высокий уровень гормона) могут свидетельствовать о развитии осложнений в виде гестационных трофобластических неоплазий).
Следует заметить, что в дальнейшем беременность не противопоказана: женщина может зачать и выносить здорового ребенка. Однако нужно помнить, что риск повторного пузырного заноса увеличивается. Вероятность второго пузырного заноса составляет ≈ 1 %, третьего — ≈ 15–18 % [3].
Гестационная трофобластическая неоплазия
Гестационная трофобластическая неоплазия (ГТН) — термин, который объединяет четыре патологических состояния: инвазивный пузырный занос, хориокарциному, трофобластическую опухоль плацентарного ложа и эпителиоидную трофобластическую опухоль. ГТН — серьезное состояние, которое требует лечения химиотерапией. Но прежде, чем рассматривать неоплазии более предметно, следует заметить, что благодаря современным методам — мониторингу ХГЧ, систематическому наблюдению и химиотерапии — более 90 % случаев оканчиваются благоприятно [5].
Около 50 % ГТН — следствие полного или частичного пузырного заноса, 25 % из них развиваются после эктопической беременности и еще 25 % — вследствие преждевременных родов.
Клиническая картина разнится, наиболее общие симптомы — кровотечение, увеличение матки, текалютеиновые кисты. Но в половине случаев заболевание может не иметь каких-либо симптомов. Основной диагностический критерий ГТН — повышение уровня ХГЧ [6].
Международная федерация гинекологии и акушерства (FIGO) приводит следующую стадийность ГТН [7]:
1 стадия: заболевание развивается в пределах матки;
2 стадия: неоплазия распространилась за пределы матки, но ограничена другими генитальными структурами (влагалищем, широкой связкой);
3 стадия: ГТН метастазирует в легкие;
4 стадия: метастазирование в другие органы.
Лечение любой ГТН заключается в химиотерапии; зачастую достаточно какого-то одного препарата; на 4 стадии рекомендована комбинация терапевтических средств. Наиболее часто используются метотрексат и дактиномицин [6]. При толерантности к препаратам или рецидиве заболевания может быть рекомендован паклитаксел [8].
Также для ГТН с высоким риском метастазирования используется комбинация EMA/CO: этопозид, метотрексат, актиномицин-D (дактиномицин), циклофосфамид и винкристин [9].
Инвазивный пузырный занос
Инвазивным называется пузырный занос, который проникает в миометрий путем прямой «экспансии» в ткань или через вены. Примерно 10-17 % пузырных заносов будут инвазивными, и из них около 15 % — метастазируют (чаще всего в легкие или влагалище) [1].
.
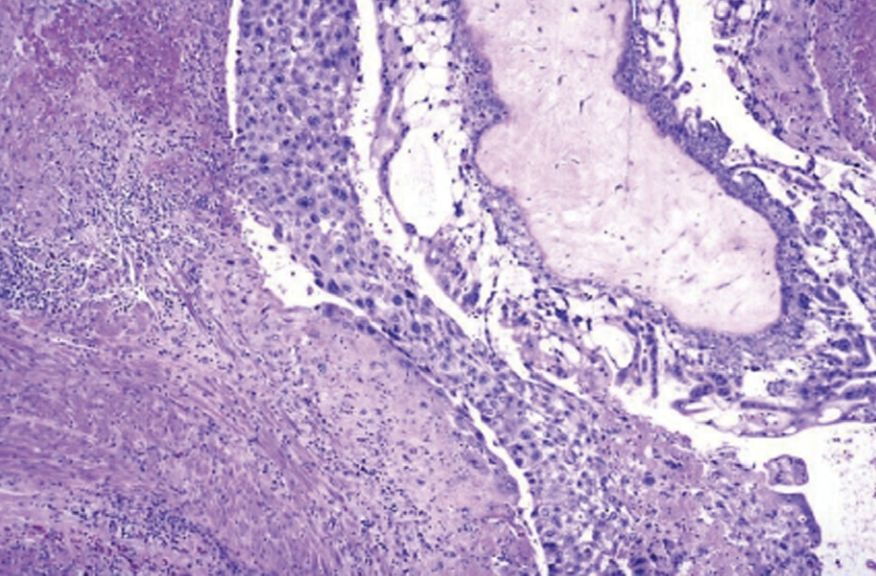
Рисунок 2. Инвазивный пузырный занос
Инвазивный пузырный занос часто диагностируется клинически, так как инвазия в миометрий сопровождается кровотечением, болевым синдромом, а измерение уровня ХГЧ позволяет удостовериться в правильности диагноза. Поэтому терапию инвазивного заноса начинают даже без гистологической верификации [1].
Следует заметить, что данная патология может проявлять себя крайне необычно. Известны случаи внезапной смерти первородящей женщины [10], спонтанное почечное кровотечение [11], развитие инвазивного пузырного заноса с метастазами вследствие ятрогенной перфорации матки [12] и т.п.
Хориокарцинома
Примерно 2-3 % пузырных заносов трансформируются в хориокарциному — злокачественную опухоль, для которой характерна прямая инвазия в миометрий, аномальная гиперплазия и анаплазия трофобласта. Ворсины хориона отсутствуют, в ткани — обширные некрозы; нередки кровотечения [1].
.
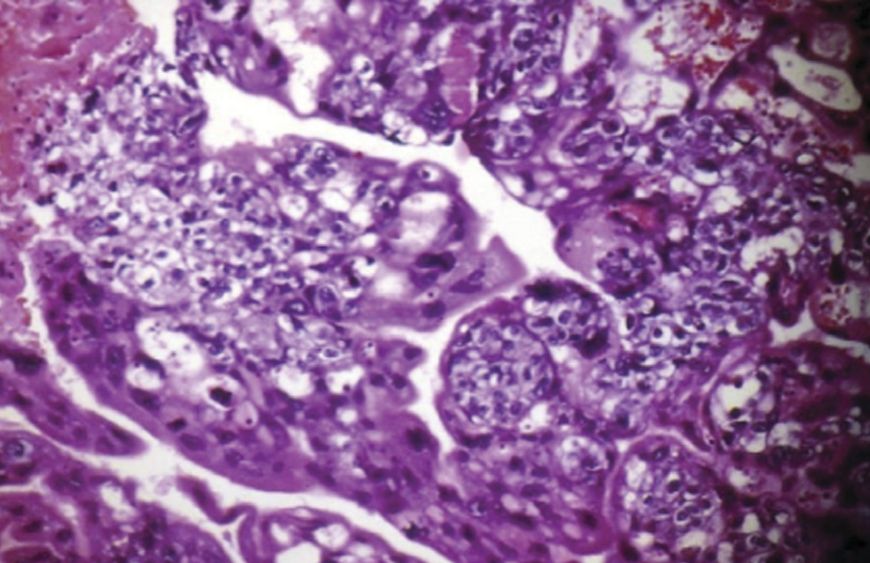
Рисунок 3. Хориокарцинома
Хориокарцинома также имеет множество форм, и, пожалуй, заслуживает отдельного обсуждения. Следует только заметить, что метастазирует данная опухоль практически в любой орган и любую ткань [13].
Трофобластическая опухоль плацентарного ложа и эпителиоидная трофобластическая опухоль
Трофобластическая опухоль плацентарного ложа (ТОПЛ) — крайне редкое злокачественное заболевание. Оно возникает, когда в месте имплантации клетки трофобласта начинают делиться и проникать в миометрий между его мышечными волокнами [1].
.
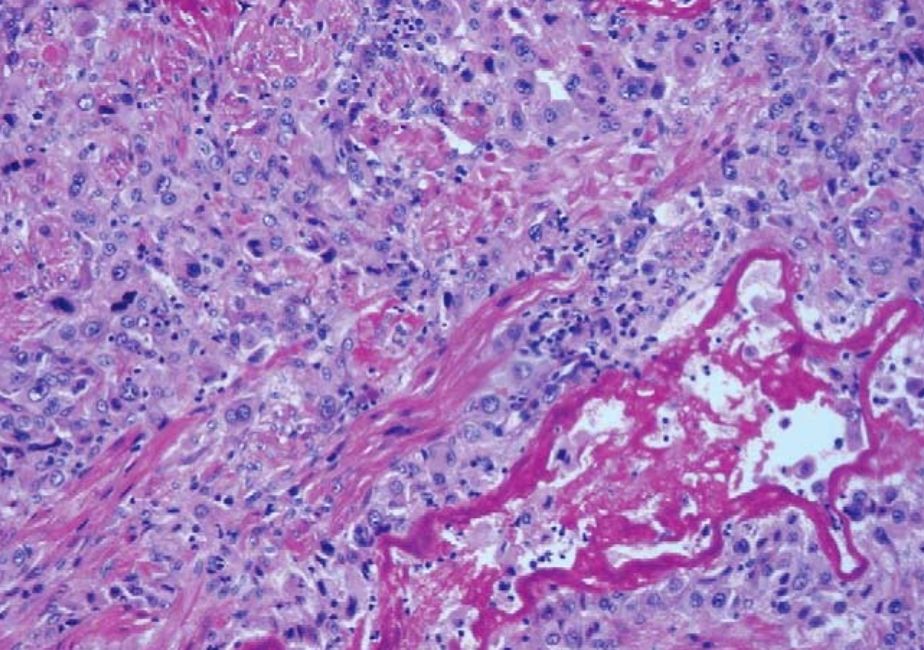
Рисунок 4. Опухоль плацентарного ложа. Клетки опухоли проникают в ткань между мышечными волокнами миометрия [14].
Обычно подобная опухоль имеет форму полиповидного или узелкового плотного образования небольшого размера (≈ 5 см). Сама опухоль гомогенна, состоит из полигональных клеток с выраженным атипизмом; зачастую проникает глубоко в ткань [14], [15]. Как ни странно, ТОПЛ крайне хорошо реагирует на химиотерапию. В случае, если у пациентки нет метастазов — рекомендуется хирургическое лечение.
Эпителиоидная трофобластическая опухоль (ЭТ) — это еще более редкая форма ТОПЛ, которая несколько схожа с хориокарциномой. Представляет собой множество пролиферирующих одноядерных клеток трофобласта. В ряде случаев опухоль может частично заместить собой эпителий эндоцервикса.
Существенной разницы в лечении ТОПЛ и ЭТ нет, однако важно заметить, что эпителиоидная трофобластическая опухоль может возникнуть спустя годы после беременности [1], [16].
Источники:
- J. R. Lurain, ‘Gestational trophoblastic disease I: Epidemiology, pathology, clinical presentation and diagnosis of gestational trophoblastic disease, and management of hydatidiform mole’, Am. J. Obstet. Gynecol., vol. 203, no. 6, pp. 531–539, 2010.
- M. J. Seckl, N. J. Sebire, and R. S. Berkowitz, ‘Gestational trophoblastic disease’, Lancet, vol. 6736, no. 10, pp. 1–13, 2010.
- E. R. M. Jauniaux and J. Johns, ‘Molar pregnancy’, Early Pregnancy, pp. 67–74, 2010.
- Q. Wang et al., ‘Prophylactic chemotherapy for hydatidiform mole to prevent gestational trophoblastic neoplasia’, Cochrane Database Syst. Rev., vol. 2017, no. 9, 2017.
- J. R. Lurain, ‘Gestational trophoblastic disease II: Classification and management of gestational trophoblastic neoplasia’, Am. J. Obstet. Gynecol., vol. 204, no. 1, pp. 11–18, 2011.
- A. Biscaro, A. Braga, and R. S. Berkowitz, ‘Diagnosis, classification and treatment of gestational trophoblastic neoplasia’, Rev. Bras. Ginecol. e Obs., vol. 37, no. 1, pp. 42–51, 2015.
- H. Y. S. Ngan, H. Bender, J. L. Benedet, H. Jones, G. C. Montruccoli, and S. Pecorelli, ‘Gestational trophoblastic neoplasia, FIGO 2000 staging and classification’, Int. J. Gynecol. Obstet., vol. 83, no. SUPPL. 1, pp. 175–177, 2003.
- J. M. Morgan and J. R. Lurain, ‘Gestational trophoblastic neoplasia: An update’, Curr. Oncol. Rep., vol. 10, no. 6, pp. 497–504, 2008.
- L. Deng, J. Zhang, T. Wu, and T. A. Lawrie, ‘Combination chemotherapy for primary treatment of high-risk gestational trophoblastic tumour’, Cochrane Database Syst. Rev., vol. 2013, no. 1, pp. 1–3, 2013.
- M. Chauhan, C. Behera, S. Madireddi, S. Mandal, and S. K. Khanna, ‘Sudden death due to an invasive mole in a young primigravida: Precipitous presentation masquerading the natural manner’, Med. Sci. Law, vol. 58, no. 3, pp. 189–193, 2018.
- S. Xiao, Q. Mu, Y. Wan, and M. Xue, Spontaneous renal hemorrhage caused by invasive mole: a case report, vol. 37, no. 3. 2016.
- Y. Shen, X. Wan, and X. Xie, ‘A metastatic invasive mole arising from iatrogenic uterus perforation’, BMC Cancer, vol. 17, no. 1, pp. 2–5, 2017.
- L. Jiao, E. Ghorani, N. J. Sebire, and M. J. Seckl, ‘Intraplacental choriocarcinoma: Systematic review and management guidance’, Gynecol. Oncol., vol. 141, no. 3, pp. 624–631, 2016.
- R. N. Baergen, J. L. Rutgers, R. H. Young, K. Osann, and R. E. Scully, ‘Placental site trophoblastic tumor: A study of 55 cases and review of the literature emphasizing factors of prognostic significance’, Gynecol. Oncol., vol. 100, no. 3, pp. 511–520, 2006.
- C. M. Feltmate, D. R. Genest, L. Wise, M. R. Bernstein, D. P. Goldstein, and R. S. Berkowitz, ‘Placental site trophoblastic tumor: A 17-year experience at the New England Trophoblastic Disease Center’, Gynecol. Oncol., vol. 82, no. 3, pp. 415–419, 2001.
- O. Fadare, V. Parkash, M. L. Carcangiu, and P. Hui, ‘Epithelioid trophoblastic tumor: Clinicopathological features with an emphasis on uterine cervical involvement’, Mod. Pathol., vol. 19, no. 1, pp. 75–82, 2006.
- ВКонтакте
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
- Telegram
