Некомпактный миокард
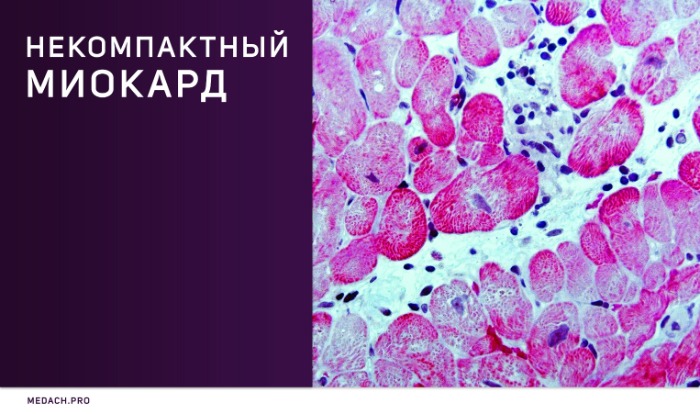
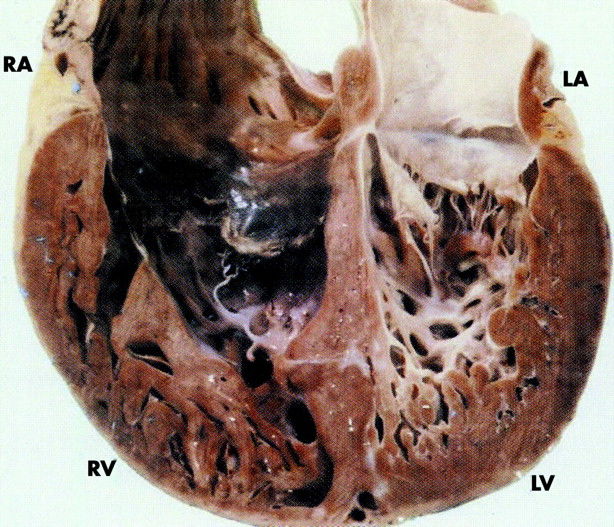
Некомпактный миокард левого желудочка (синонимы: губчатый миокард, эмбриональный миокард, персистирующие синусоиды) — генетически детерминированная кардиомиопатия, которая характеризуется патологической трабекулярностью миокарда левого желудочка в результате нарушения нормального эмбриогенеза сердца с формированием двух слоев миокарда: толстого некомпактного (эндокардиального) и тонкого нормального (компактного, эпикардиального).
Код по МКБ-11
BC44 Noncompaction cardiomyopathy
Историческая справка
Первые упоминания губчатого миокарда описаны американским хирургом Самуэлем Беллетом в 1932 году: в миокарде левого желудочка новорожденного с цианотическим врожденным пороком сердца отмечались глубокие лакуны и трабекулы, выявленные при аутопсии. Далее, лишь с развитием и внедрением эхокардиографии (далее ЭхоКГ), в 1984 году немецкие ученые Рольф Энгбердинг и Франц Бендер описали наличие синусоид миокарда у пациента, характерные лишь для эмбрионального этапа развития сердца. В 1990 году детский кардиолог и американский профессор кафедры педиатрии вместе с соавторами предложил термин «изолированная некомпактность миокарда левого желудочка». Учитывая все большее внедрение в практику ЭхоКГ, описывалось множество случаев данной нозологии, и в 1995 году Всемирная организация здравоохранения включила данное заболевание в группу неклассифицируемых кардиомиопатий. Затем, в 2006 году, Американская ассоциация сердца отнесла данную патологию к первичным генетическим кардиомиопатиям. С 2008 года заболевание включено в группу неклассифицируемых кардиомиопатий согласно классификации Европейского общества кардиологов.
Эпидемиология
Распространенность заболевания среди взрослого населения составляет 0,014%. Встречается: у 0,01-0,27% всех взрослых пациентов, направленных на ЭхоКГ; у 3% больных из 960 с признаками ХСН; у 100 пациентов из 36933, перенесших ЭхоКГ (в период с 1994-2006 гг). По данным разных ученых, заболевание чаще встречается у мужчин (56–82 %). В детской практике из всех случаев кардиомиопатий некомпактный миокард встречается в 9,2%, занимая третье место после гипертрофической КМП и дилатационной КМП.
Эмбриональное развитие миокарда
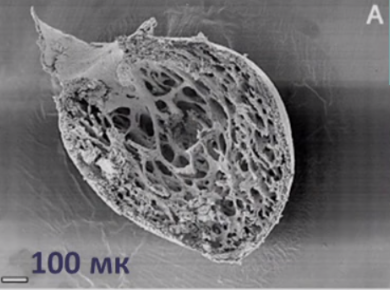
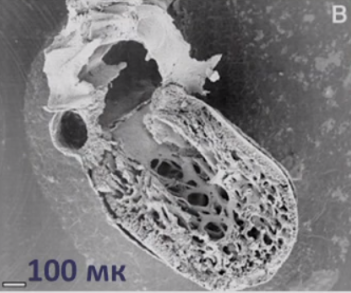
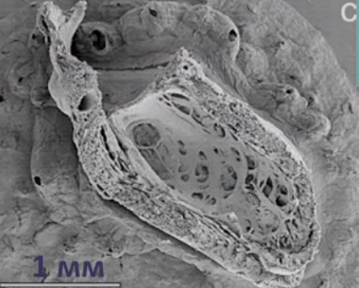
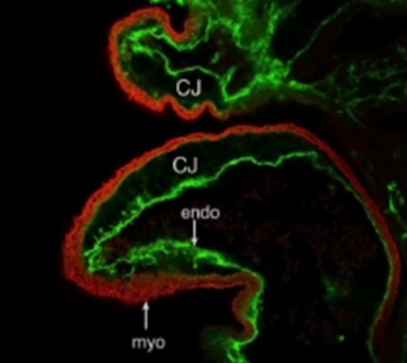
Для наиболее точного понимания механизма образования некомпактного слоя миокарда обратимся к эмбриологии. Миокард развивается из миоэпикардиальной пластинки спланхнотома мезодермы, представляя собой сеть волокон, разделенных широкими полостями. С 5-й недели эмбрионального развития происходит уплотнение сети волокон, сужение межтрабекулярных лакун, формируется коронарный кровоток, происходит процесс уменьшения межтрабекулярных пространств до размеров капилляров. Миокард «компануется» от основания к верхушке, от эпикарда к эндокарду (рис. 1, 2, 3, 4). При нарушении данного процесса, чаще всего в результате генетической мутации в генах, кодирующих белок таффазин, альфадистробеверин, гетерозиготные мутации в генах, кодирующих MYH7, ACTC, TNNT2, в сердце остаются зоны некомпактного миокарда с глубокими межтрабекулярными пространствами.
2009 July 2
Классификация
Большинство ученых выделяют следующие формы некомпактного миокарда:
– изолированный;
– в сочетании с врожденными пороками сердца;
– в сочетании с нейромышечными заболеваниями (метаболическая миопатия, синдром Barth, синдром Roifman, синдром Ohtahara, синдром Noonan, мышечная дистрофия Emery–Dreifuss, мышечная дистрофия Becker, синдром Melnick–Needles).
По форме возникновения:
– спорадическая;
– семейная (30%).
По анатомическим формам выделяют:
– левожелудочковая;
– правожелудочковая;
– бивентрикулярная.
По морфологическим типам:
– лакунарный;
– губчатый;
– смешанный.
По степени некомпактности миокарда (по отношению толщины слоя некомпактного миокарда к толщине всей стенки сердца на уровне верхушки левого желудочка):
– мягкая (0,33–0,26)
– умеренная (0,25–0,20)
– тяжелая (менее 0,2)
Патогенез и клиника
Патогенез складывается из сердечной недостаточности, синдрома нарушений ритма, тромбоэмболического синдрома.
Сердечная недостаточность выходит на ведущее место в клинике данного заболевания. Из-за нарушенной архитектоники строения миокарда происходит нарушение его сократительной способности. При тяжелой степени некомпактности клиническая картина данного синдрома наиболее выражена с преобладанием недостаточности по обоим кругам кровообращения и с выраженным снижением общей сократительной способности миокарда. Как правило, у некоторых пациентов клиника заболевания может манифестировать в результате запуска воспалительного процесса в миокарде, а в ряде случаев, при благоприятном течении, некомпактный миокард можно выявить впервые у лиц пожилого возраста. В клинической картине заболевания на первое место может выходить болевой синдром, который выражается приступами стенокардии. Это объясняется большей потребностью в кислороде некомпактного слоя миокарда, который не кровоснабжается основными ветвями коронарных артерий, а кровоснабжение его происходит непосредственно из полости левого желудочка.
Синдром нарушений ритма проявляется чаще всего желудочковыми нарушениями ритма — более чем в половине случаев (экстрасистолия, нередко и высоких градаций). В четверти случаев наблюдается фибрилляция предсердий. Также, вследствие эндомиокардиального фиброза с захватом проводящей системы сердца наблюдаются нарушения проводимости по типу АВ, СА-блокад.
Конечно же, нарушение глобальной систолической функции, наличие нарушений ритма сердца, а в частности фибрилляции предсердий, наличие глубоких лакун предрасполагает к образованию тромбов в полости левого желудочка, а отсюда и тромбоэмболических осложнений (кардиоэмболические инсульты, ТИА, мезентериальный тромбоз).
Диагностика
Клиника при данном заболевании неспецифична, она может маскировать и дебют ИБС, и прочие кардиомиопатии. В данном случае нам помогает ЭхоКГ и МРТ с контрастированием гадолинием, помимо стандартной ЭКГ и суточного мониторирования ЭКГ.
Выделяют следующие эхокардиографические критерии некомпактного миокарда:
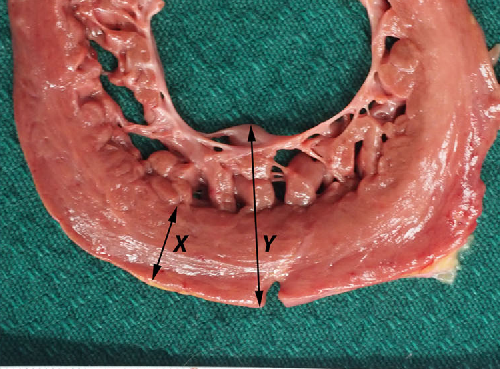
- Критерий Chin, 1990. Отношение компактной (X) части миокарда к общей толще миокарда (Y) ≤ 0,5.(рис.6) Измерение проводится в конце диастолы из парастернальной проекции по короткой оси и верхушечной проекции;
- Критерий Jenni, 2001. Измеряется в конце систолы из парастернальной позиции по короткой оси левого желудочка. Отмечается отношение некомпактной части миокарда к компактной более 2; визуализируются многочисленные выступающие трабекулы с глубокими межтрабекулярными пространствами, между которыми при цветовом доплере выявляется кровоток;
- Критерий Stollberger, 2007. Наличие более 3 трабекул в левом желудочке в направлении от верхушки к папиллярным мышцам, визуализирующиеся одновременно в одной эхокардиографической позиции; выявление кровотока в межтрабекулярных пространствах при цветном доплере;
Так же проводится оценка всех стандартных параметров при ЭхоКГ (размеры полостей, наличие изменений сократительной способности, клапанная недостаточность, оценка фракции выброса).
МРТ проводится с контрастным усилением редкоземельного металла гадолиния, оценивается: ФВ ЛЖ, индексированная масса миокарда (компактного, некомпактного); число некомпактных сегментов; критерий некомпактности (чувствительность 86%, специфичность 99%: соотношение компактного и некомпактного слоя миокарда в диастолу более 1:2); индекс ремоделирования левого желудочка.
И, конечно же, не стоит забывать о генетическом картировании и биопсии миокарда.
Принципы и тактика лечения.
Пациентам с бессимптомным течением специфической терапии не требуется, им нужно лишь динамическое наблюдение у врача кардиолога. При наличии клиники лечение должно складываться из следующих составляющих: стандартная терапия ХСН; назначение антикоагулянтной терапии при необходимости (снижение ФВ, ТЭ в анамнезе, тромбоз полостей сердца); назначение, при необходимости, антиаритмической терапии; назначение иммуносупрессивной терапии при доказанности аутоиммунного повреждения миокарда. Так же, в отдельных случаях, могут рассматриваться варианты установки ЭКС (при наличии блокад высоких градаций с эпизодами синкопе); установки кардиовертера-дефибриллятора (при плохом терапевтическом ответе на антиаритмики); трансплантации сердца.
Источники
- Диагноз при сердечно-сосудистых заболеваниях (формулировка, классификация) / С.Г. Горохова. – 4-е изд., перераб. и доп. – М.: ГЭОТАР-Медиа, 2018.-стр. 192-193
- Басаргина Е. Н., Гасанов А. Г. Некомпактный миокард левого желудочка у детей-редкая кардиомиопатия? //Российский вестник перинатологии и педиатрии. – 2010. – Т. 55. – №. 4.
- Голухова Е. З., Шомахов Р. А. Некомпактный миокард левого желудочка //Креативная кардиология. – 2013. – №. 1. – С. 35-45.
- ICD-11 (Mortality and Morbidity Statistics). https://icd.who.int/browse11/l-m/en