Оптогенетика как возможный метод лечения эпилепсии

Оптогенетика — использование света для стимуляции или ингибирования нейронных связей посредством вирусной трансдукции генов белковых каналов, — стала возможным методом лечения эпилепсии. Путем введения вирусных векторов, несущих катионные или анионные каналы, полученные из водорослей, известные как опсины, нейроны, которые инициируют или распространяют судорожный синдром, могут быть отключены.
Вступление
Эпилепсией страдают более 50 миллионов человек во всем мире, или примерно 1 % населения, с частотой от 4 до 10 на 1000 человек в год. Лечение противоэпилептическими препаратами часто связано с плохо переносимыми побочными эффектами, более того, болезнь резистентная к лечению более чем у 20 % пациентов. Было обнаружено, что резекция частей височной доли, миндалины и гиппокампа является отличным вариантом лечения для небольшой доли пациентов, страдающих височными припадками, причём 86–90 % пациентов освобождаются от приступов в течение двух лет.
Однако даже среди тех пациентов, у которых эпилептический очаг расположен в медиальной части височной доли, не все подходят для резекции. Поэтому существует постоянная потребность в терапии, которая затрагивает фокальные эпилепсии, не поддающиеся существующим методам лечения.
Существует два основных подхода к борьбе с эпилепсией. Первый подход, который лежит в основе действия большинства противоэпилептических препаратов, заключается в изменении возбудимости нейронной сети, чтобы предотвратить появление припадка. Этот фармакологический подход привел к появлению многих новых противоэпилептических препаратов за последние 5 десятилетий, но уровень трудноизлечимых припадков оставался стабильным. Второй подход для лечения резистентных припадков заключается в том, чтобы прервать их в самом начальном этапе, что привело к поиску медицинских устройств, которые могут остановить припадок «по требованию».
Такие устройства, подобно имплантируемым дефибрилляторам, должны работать по принципу «закрытой петли»: подтвердить наличие пароксизма и среагировать в течение миллисекунд после начала приступа, исправляя активность больных нейронов и оставляя нормальные нейроны незатронутыми. У устройств с замкнутым контуром преимущество состоит в том, что период их работы ограничен началом припадка, что позволяет оставить функционирование нейронов и глии без вмешательств в периоды между припадками.
В последнее десятилетие значительное внимание уделяется глубокой и субдуральной электрической стимуляции эпилептических очагов. Два последних рандомизированных контролируемых исследования показали значительное снижение частоты приступов при применении стимуляции. Хотя результаты являются многообещающими, электростимуляция неспецифична в отношении определенных типов клеток.
Оптогенетика использует оптические системы для стимуляции или ингибирования определенной подгруппы нейронов путем введения генов светочувствительных каналов. Этот мощный инструмент для включения и выключения интересующих нейронных связей исследуется в отношении различных неврологических и некоторых других заболеваниях, включая исследование физиологии миоцитов.
Оптогенетические инструменты
Оптогенетика — это новое молекулярное вмешательство, основанное на использовании опсинов — светочувствительных ионных каналов, — впервые обнаруженных в начале 1970-х годов. Ионный канал бактериородопсина, найденный в плазматической мембране Halobacterium halobium, подвергается конформационному изменению в ответ на поглощение света определенной длины волны, что приводит к оттоку протонов. Этот отток ионов генерирует продолжительный трансмембранный градиент и электрический потенциал, который бактериальная клетка затем использует для синтеза АТФ.
В то время, когда изучались тонкости хемиосмотической теории, опсины обеспечивали понимание распространенного биохимического механизма. Однако эти каналы оставались «нетронутыми» в нейробиологии почти 3 десятилетия. В 2004 году исследователи эффективно включили протонный канал (channelrhodopsin-1) и катионный канал (channelrhodopsin-2) в нейроны млекопитающих.
Эти опсины реагировали на вспышки света в течение миллисекунд, что приводило к деполяризации нейронов. Кроме того, были идентифицированы опсины, которые создавали деполяризующий трансмембранный поток ионов при освещении видимым светом красного спектра, важные для нейробиологических исследований, поскольку красный свет лучше проникает сквозь ткани.
После того, как исследователи научились активировать нейронные цепи, их усилия были сосредоточены на идентификации канала для их ингибирования, что было достигнуто с помощью гиперполяризующего опсина из галофильной архебактерии Natronomonas pharaonis. Конформация галородопсина — белка с семью трансмембранными спиральными доменами, — меняется с транс-ретинальной на 13-цис-ретинальную, обменивая 1 фотон на 1 ион хлора. C добавлением С-концевой эндоплазматической транспортной последовательности к галогенродопсину его закрепление в мембране улучшилось, а дальнейшая оптимизация увеличила амплитуду генерируемого тока.
Было продемонстрировано, что эта версия канала, названная eNpHR3.0, безопасно и надежно экспрессируется в клетках подвижных животных. Дальнейшие модификации позволили получить множество генно-инженерных опсинов, и недавно была создана тандемная конструкция, которая позволит доставлять как возбуждающий канал родопсин, так и ингибирующий галогенродопсин в одном векторе 1e. Количество доступных опсинов продолжает расти и, вероятно, будет продолжаться их оптимизация для экспериментального и терапевтического применения.
На рисунке 1 показаны функции этих каналов.
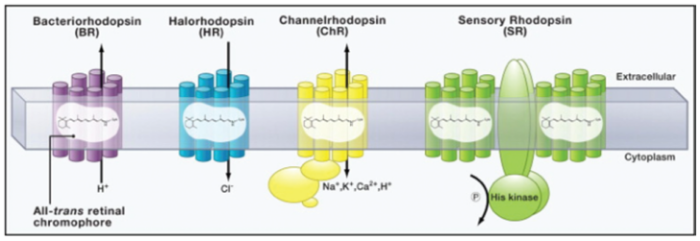
Рис. 1
Опсины доставляются к интересующим клеткам с помощью различных методов. В настоящее время инъекция вирусных векторов в различные участки может быть наиболее применимой к клиническим сценариям. Подгруппы клеток в пределах зоны выбираются с использованием клеточных иммунных промоторов, и некоторые из этих типов клеток участвуют в формировании эпилепсии.
Гены опсинов переносятся в вирусных векторах, как правило, аденоассоциированным вирусом или лентивирусом. Другой способ введения включает в себя скрещивание животных с активной Cre-рекомбиназой, экспрессирующих Cre в специальных нейронах с животными, трансфицированными интересующим геном. Это приводит к появлению канала опсина только в тех нейронах, которые экспрессируют Cre-рекомбиназу.
Пример гена показан на рисунке 2, включая сам ген опсина и области, необходимые для эффективной транслокации.
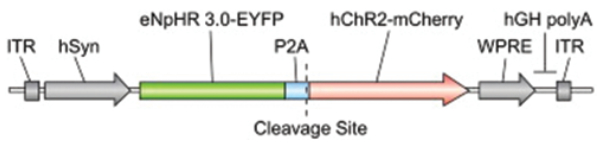
Рис. 2
Подача света для активации oпсинов — еще одна область исследований, в которой испытываются различные системы. Тонкие цилиндрические «оптроны» с наконечником, содержащим оптическое волокно и регистрирующий электрод, напоминают электроды для глубокой стимуляции мозга. Другие версии используют оптрон, имплантированный в 1 область, с отдельной микро-светодиодной матрицей для записи. Перед использованием на человеке эти системы должны быть приведены в соответствие стандартам, применяемым в настоящее время для других имплантируемых устройств, с изменениями, сделанными для обеспечения хорошей переносимости и безопасности пациентов.
Оптогенетика сегодня применяется при лечении многих неврологических заболеваний, а также в отношении некоторых других болезней, включая стимуляцию сердечной мышцы. К другим типам таргетных клеток относятся срединные шипиковые нейроны в базальных ганглиях для изучения болезни Паркинсона, дофаминергические нейроны вентральной области покрышки среднего мозга в моделях депрессии и дофаминовые D1-экспрессирующие нейроны префронтальной коры для исследования схемы, лежащей в основе временного контроля за поведением. Исследование различных физиологических механизмов также стало фокусом оптогенетической манипуляции, с недавними исследованиями, разъясняющими роль астроцитов вентральной поверхности в контроле над дыханием.
Эпилепсия представляет собой сложное явление для изучения из-за большого числа нейронных сетей, которые инициируют или распространяют пароксизм. Тем не менее, есть несколько недавних исследований, целью которых является усиление избирательности оптико-электронной системы для анализа и контроля динамики сети на нескольких моделях судорог на животных.
Эпилепсия характеризуется гиперактивностью различных нейронов, и, следовательно, многие из текущих исследований были сосредоточены на способах замораживания или ингибирования сверхактивных цепей. Способность избирательно нацеливаться на нейроны гиппокампа млекопитающих была первым шагом на пути к исследованию этого пути заболевания и была достигнута с использованием ингибирующего галоордопсина опсина в органотипических культурах гиппокампа мыши.
После этого достижения, галородопсин был использован в отдельных основных глутаматергических нейронов в гиппокампе. В этой модели мыши инъекция лентивирусного вектора в пирамидальные клетки CA1 и CA3 приводила к гиперполяризации в ответ на оранжевый свет (длина волны 573-613 нм). Потенциалы действия были ослаблены, а пароксизмальные деполяризующие сдвиги были ограничены, подавляя эпилептиформную активность.
Важно отметить, что присутствие вирусно- трансфецированных опсинов в нейроны не влияло на нормальные физиологические свойства клеток. Чтобы проверить это, органотипические срезы гиппокампа были подвергнуты полной темноте, и были проверены различные свойства клеток. Параметры, в том числе входное сопротивление, потенциал покоя мембраны, порог и длительность потенциала действия, амплитуды в ответ на гиперполяризующие и деполяризующие импульсы, а также размещение клеток в потенциалах действия были сходными в нейронах галогенодопсина по сравнению с контрольными.
Будущие направления
Эти исследования лежат в основе нашего понимания того, как использовать светочувствительные каналы в качестве терапевтического варианта контроля захвата. Многое еще предстоит узнать из использования опсинов и световой доставки, и многие технические аспекты все равно должны быть оптимизированы до применения к людям, некоторые из которых могут оказаться существенными проблемами. Среди этих аспектов - исследование иммунного ответа человека на эти чужеродные белки, устойчивость вирусных векторов в нервной ткани и оптимизация доставки света с помощью хронически имплантированных устройств. До сих пор применение этого мощного инструмента было успешным для выяснения нормальных и патологических механизмов, и был сделан ряд исследований в области терапевтических применений, включая представленные здесь в отношении эпилепсии. Разработка модели нечеловеческого примата - это одно недавнее достижение, которое может улучшить понимание того, как оптогенетика может применяться к людям.
Источник:
Optogenetics in Epilepsy [Электронный ресурс] / J. Nicole Bentley, M.D.; Cindy Chestek, Ph.D.; William C. Stacey, M.D., Ph.D.; Parag G. Patil, M.D., Ph.D — Электрон. журн. — Medscape, 2013. — Режим доступа к журн.: https://www.medscape.com/viewarticle/806659_1
