Helicobacter pylori и рак желудка

Ученые наконец-то нашли ответ на давно интересующий всех вопрос: как бактерия Helicobacter pylori вызывает рак желудка. Проводя эксперименты на мышах и линиях раковых клеток человека, они показали, что воспаление в результате бактериальной инфекции приводит к пролиферации эпителиальных клеток желудка, которые в конечном итоге образуют опухоли желудка. Блокируя белковый путь, ответственный за эту пролиферацию, исследователи предотвращали образование опухоли желудка.
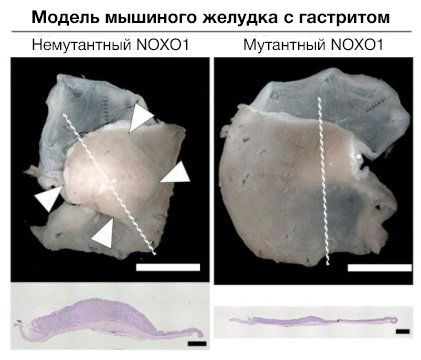
Рисунок 1 | Фотографии гиперплазии слизистой оболочки желудка, связанной с гастритом (стрелки, слева) в модели мышиного желудка. Гиперплазия была значительно снижена при мутации гена Noxo1 (справа). Гистологические срезы участков слизистой оболочки показаны внизу (окрашивание H & E), что указывает на полное подавление гиперплазии, связанной с гастритом, с помощью нарушения работы Noxo1.
В 1982 году ученые сообщили о связи между хроническим гастритом и бактерией желудка Helicobacter pylori, что вызвало волну исследований этого нового идентифицированного патогена. Эти исследования показали, что, помимо вовлечения в гастрит, H. pylori является важным фактором развития как пептической язвы, так и рака желудка. Но, хотя связь между бактерией и заболеванием была очевидной, то, как именно H. pylori вызывал опухоли желудка оставалось неясным. Теперь, почти четыре десятилетия спустя, исследователи из Университета Канадзава и Японского агентства медицинских исследований и разработок наконец-то показали, как воспаление, вызванное инфекцией H. pylori вызывает пролиферацию стволовых клеток эпителия желудка, что приводит к опухолям желудка.
В отчете, опубликованном недавно в журнале генетики рака «Oncogene», исследователи описывают, как они разгадал эту тайну. «Ранее мы показали, что фактор некроза опухоли альфа (TNF-α) — цитокин, вызывающий воспаление, способствует образованию опухоли желудка, активируя белок под названием NOXO1 (NADPH Oxidase Organizer 1)», — говорит ведущий автор исследования доктор Канаэ Эчизен. «Мы не знали, как именно NOXO1 вызывает образование опухоли в желудке».
NOXO1 является компонентом комплекса NOX1 (NADPH oxidase 1 — НАДФ оксидаза 1), который вырабатывает молекулы, повреждающие ткани, называемые активными формами кислорода (АФК). Окислительный стресс, вызванный этими молекулами, может привести к мутациям в ДНК клеток желудка, что приводит к образованию опухоли. Воспаление, вызванное инфекцией H. pylori, также способствует увеличению концентрации активных форм кислорода, усиливая окислительный стресс в желудке.
В недавно опубликованном исследовании группа ученых показала, что воспаление вызывает избыточную продукцию белков комплекса NOX1, в ответ на сигналы от NF-κB — регуляторного белка, который активирует гены для борьбы со стрессом или бактериальной инфекцией и который является основным игроком в воспалительном ответе. Однако, что наиболее важно, они обнаружили, что передача сигналов NOX1/АФК вызывала неконтролируемое размножение эпителиальных стволовых клеток желудка, что приводило к образованию опухоли.
Зная это, ученые применили препарат для подавления активности комплекса NOX1, который остановил рост раковых клеток желудка. Еще более увлекательно то, что разрушение NOXO1 на модели мышиного гастрита остановило пролиферацию эпителиальных стволовых клеток. «Мы наконец смогли показать, что воспаление усиливает экспрессию NOXO1, вызывает пролиферацию стволовых клеток эпителия желудка и приводит к опухолям желудка», — объясняет доктор Масанобу Осима, ведущий автор исследования. «Рак желудка занимает четвертое место по распространенности среди онкологических заболеваний в мире и второе место по уровню летальности. Если мы сможем нарушить путь передачи сигналов NOX1/АФК в естественных условиях, мы сможем предотвратить развитие этого агрессивного заболевания».
