11 клинических испытаний, которые повлияют на медицину в 2022 году

Несмотря на непрекращающиеся проблемы, связанные с COVID-19, в 2021 году были получены некоторые важные результаты клинических испытаний.
2022 год тоже обещает быть успешным, поэтому Nature Medicine спрашивает лидеров в своей области, какие, по их мнению, результаты клинических испытаний будут наиболее важными в наступающем году.
Терапия COVID-19
Эдвард Миллс: Испытание TOGETHER стало революционным, поскольку в 2021 году с помощью этой программы удалось оценить девять различных методов лечения, что впоследствии позволило отказаться от шести из них на ранних этапах из-за недостаточной эффективности, тем самым сэкономив время и деньги. Самое главное и наиболее меня волнующее — то, что это первое совместное испытание, которое демонстрирует, что флувоксамин, недорогое перепрофилированное лекарство, может предотвратить госпитализацию вследствие COVID-19. Сейчас мы переходим к комбинированным препаратам, и я думаю, что именно за этим будущее лечения COVID-19. В следующем году мы должны узнать об эффективности нескольких комбинаций, включая флувоксамин или флуоксетин плюс ингаляционный стероид, а также флувоксамин плюс противовирусный препарат прямого действия молнупиравир.
Эдвард Миллс — профессор медицинских наук в Университете Макмастера.
Универсальные противогриппозные вакцины
Нил П. Кинг: Как и существующие вакцины против сезонного гриппа, FluMos-v1 (таблица 1) предназначена для выработки антител к нескольким различным штаммам вируса. В отличие от существующих прививок от гриппа, в новой вакцине используется иммуноген из мозаичных наночастиц, который совместно отображает антигены нескольких вирусов гриппа на одной и той же поверхности наночастиц. В нашей доклинической работе мы обнаружили, что иммуноген из наночастиц вызывает большее разнообразие защитных антител, чем современные вакцины против гриппа. Нам особенно интересно узнать о том, как вакцина будет взаимодействовать с иммунными системами, которые ранее уже сталкивались с вирусами гриппа или вакцинами. Такой иммунный статус может повлиять на эффективность вакцины, и это то, о чем мы не смогли узнать на доклиническом уровне.
Нил П. Кинг — доцент Института дизайна белка Вашингтонского университета.
Таблица 1 | Клинические исследования в 2022 году
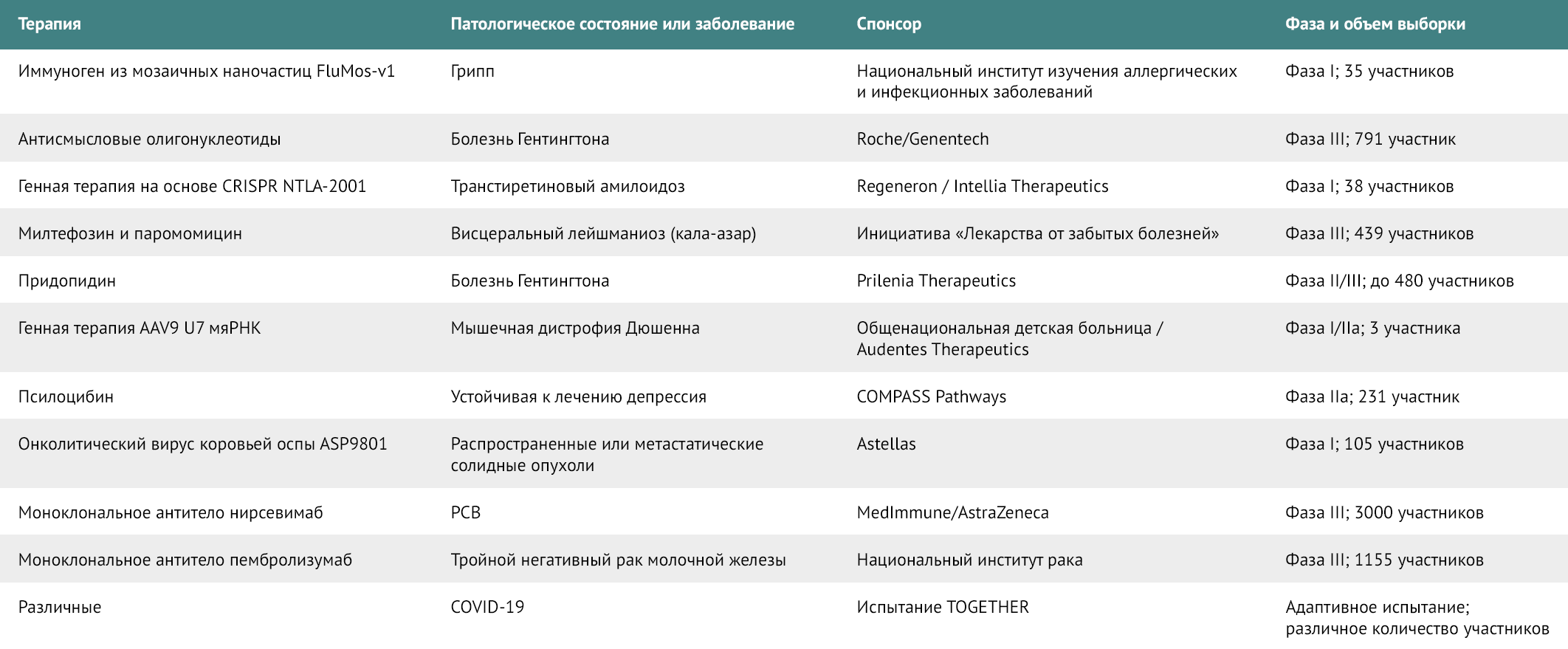
AAV9 — аденоассоциированный вирус 9; мяРНК — малая ядерная РНК
Моноклональные антитела длительного действия к РСВ
Рут А. Каррон: Респираторно-синцитиальный вирус (RSV) является основной причиной тяжелых респираторных инфекций у младенцев и детей, но в настоящее время вакцины против вируса нет. Нирсевимаб — это моноклональное антитело, которое нацелено на белок F на поверхности вируса. Он несет мутацию YTE, которая продлевает его период полураспада; это означает, что однократная доза антитела может защитить младенца в течение всего сезонного воздействия РСВ. Это значительное улучшение по сравнению с паливизумабом — существующим на настоящим момент моноклональным антителом к РСВ, действие которого длится около месяца, и поэтому применяющимся только для младенцев высокого риска. Окончательные результаты будут интересными, потому что они определят, готовы ли органы, определяющие политику относительно вакцин, одобрить моноклональное антитело в качестве профилактического продукта вместо вакцины.
Рут А. Каррон — профессор департамента международного здравоохранения Школы общественного здравоохранения Блумберга Джона Хопкинса, директор Центра исследований иммунизации и директор-основатель Инициативы Джона Хопкинса по вакцинации.
▶ Материалы по теме: статья РСВ инфекция: что важно знать врачу и подкаст Разбор #17 | РСВ инфекция и недоношенные дети
CRISPR для лечения амилоидоза
Джулиан Гиллмор: Я наблюдаю за пациентами с транстиретиновым амилоидозом в течение 25 лет, и еще пять лет назад я просто смотрел, как ухудшается их здоровье. Несколько лет назад стали доступны сайленсеры генов, которые улучшили исходы для пациентов, что было очень существенным достижением. Но пациенты, получающие терапию сайленсерами, нуждаются в повторном лечении на протяжении всей жизни, и хотя у большинства пациентов заболевание стабилизируется, у некоторых наблюдается прогрессия. Предварительные данные этого исследования впервые показали, что генную терапию на основе CRISPR можно проводить путем внутривенной инфузии для редактирования определенного гена в клетках печени. Более полные результаты ожидаются в следующем году. Эта новая терапия редактирования генов предлагает пациентам перспективу значительных клинических улучшений после однократного приема препарата.
Джулиан Гиллмор — специалист по медицине и почетный консультант-нефролог Королевской Лондонской больницы.
▶ Материалы по теме: Нобелевская премия по химии 2020 года || Технологии редактирования генов набирают обороты || CRISPR: от кишечной палочки до палочек и колбочек
Пероральная терапия кала-азара
Моник Васунна: Я рада видеть результаты третьей фазы нашего клинического исследования, в котором мы искали оптимальный режим лечения висцерального лейшманиоза, также известного как «кала-азар». В этом исследовании тестируются новые комбинированные схемы применения милтефозина и паромомицина в Эфиопии, Судане, Кении и Уганде в Восточной Африке. Цель состоит в том, чтобы заменить токсичный компонент стибоглюконат натрия при нынешнем инъекционном лечении кала-азара пероральным введением милтефозина. Это остро необходимое улучшение, которого ждали пациенты, и мы работаем над этим в течение многих лет, поскольку пероральное лечение можно проводить в местных медицинских центрах, ближе к пострадавшему населению. Пациенты с диагнозом кала-азар умрут, если их не лечить. Новая, менее токсичная и более легко вводимая схема также будет полезна для детей, которые сильно страдают от висцерального лейшманиоза. Дети в возрасте до 12 лет составляли 60 % пациентов, участвовавших в клинических исследованиях, и предварительные результаты показывают многообещающе высокую эффективность.
Моник Васунна является директором регионального отделения инициативы «Лекарства от забытых болезней» в Африке, Найроби.
Воздействие на рецептор сигма-1 при нейродегенеративных заболеваниях
Блэр Ливитт: В настоящее время проводится несколько исследований придопидина, направленного на замедление прогрессирования нейродегенеративных расстройств. Придопидин — это пероральный низкомолекулярный препарат, который избирательно воздействует на рецептор сигма-1 и имеет хорошо зарекомендовавшие себя показатели безопасности, полученные в ходе предыдущих клинических испытаний на людях. За последние несколько лет была установлена роль рецептора сигма-1 в процессе нейродегенерации и получено немало многообещающих доклинических данных, позволяющих предположить, что придопидин оказывает защитное действие при болезни Гентингтона и других нейродегенеративных расстройствах, таких как боковой амиотрофический склероз. В настоящее время также проводится фазы II/III исследования придопидина при боковом амиотрофическом склерозе, и сообщество с нетерпением ожидает результатов.
Блэр Ливитт — невролог-консультант и директор по исследованиям Центра болезни Гентингтона Университета Британской Колумбии.
Пропуск экзонов при мышечной дистрофии
Кевин М. Фланиган: У небольшого числа мальчиков с мышечной дистрофией Дюшенна заболевание обусловлено дупликацией экзона 2 в гене DMD (который кодирует дистрофин). Дупликация может быть удалена с помощью вектора на основе аденоассоциированного вируса 9, который несет копии некодирующей малой ядерной РНК U7 с последовательностью, направленной на донорные и акцепторные сайты сплайсинга в дублированном экзоне. Этот подход с пропуском экзонов впервые исследуется на людях и заключается в исключении копии экзона 2 DMD и экспрессии полноразмерного дистрофина дикого типа. В настоящее время тестируются еще четыре метода генной терапии мышечной дистрофии Дюшенна, но каждый из них требует доставки гена, кодирующего сконструированный микродистрофин, которого нет в природе и который, как ожидается, приведет к существенному функциональному улучшению.
Кевин М. Фланиган — практикующий невролог в Национальном детском учреждении, заведующий кафедрой нервно-мышечных исследований Фонда Роберта Ф. и Эдгара Т. Вулфа и профессор педиатрии и неврологии в Медицинском колледже Университета штата Огайо.
Психоделическая терапия
Дэвид Натт: Псилоцибин — психоделик, полученный из грибов, — демонстрирует большие перспективы в лечении психических расстройств. Я в восторге от этого испытания по трем основным причинам. Во-первых, он решает огромную проблему депрессии, которая устойчива к существующим методам лечения. Во-вторых, это многоцентровое и многонациональное испытание, которое позволит исследователям протестировать психоделическую терапию в различных группах людей. Наконец, в нем также будут даны некоторые данные о соотношении «доза — эффект», поскольку тестируются три сильно отличающиеся дозы псилоцибина: 1 мг, 10 мг и 25 мг.
Дэвид Натт — профессор нейропсихофармакологии Эдмонда Дж. Сафры и директор отделения нейропсихофармакологии в Отделе наук о мозге Имперского колледжа Лондона.
Онколитические вирусы
Йошиказу Йонемицу: Это фаза I открытого исследования препарата ASP9801, вводимого путем внутриопухолевой инъекции пациентам с распространенными или метастатическими солидными опухолями. ASP9801 представляет собой генетически модифицированный онколитический вирус коровьей оспы, экспрессирующий два цитокина — IL-7 и IL-12, которые помогают стимулировать противоопухолевые иммунные реакции. ASP9801 был эффективен на нескольких иммунокомпетентных мышиных моделях и показал многообещающие результаты при непосредственном лечении первичного очага опухоли и метастазов. Это исследование впервые позволит оценить безопасность, переносимость и противоопухолевую активность этого онколитического вируса у онкологических пациентов.
Йошиказу Йонемицу — профессор Высшей школы фармацевтических наук Университета Кюсю.
Антисмысловые нуклеотиды против болезни Гентингтона
Клаудия Теста: Это исследование по болезни Гентингтона закрылось досрочно в марте 2021 года из-за отсутствия результата. Несмотря эту неудачу, окончательные данные еще не получены, а они критически важны. Этот антисмысловой олигонуклеотид (ASO) нацелен как на мутантную, так и на нормальную мРНК гентингтина, которая полностью отличается от других ASO на рынке. Результаты испытаний дадут нам первый реальный взгляд на фундаментальные аспекты стратегий снижения уровня РНК, в том числе на то, как препарат влияет на различные биомаркеры у сотен участников. Результаты могут изменить направление клинических испытаний для других патологий, поддающихся лечению с помощью ASO. Это исследование прекрасно демонстрирует, что хорошо продуманные и грамотно проведенные испытания не проваливаются окончательно — усилия ученых будут иметь решающее значение для ускорения сроков безопасного и эффективного лечения болезни Гентингтона, даже если результаты не приведут к созданию препарата, одобренного FDA.
Клаудия Теста — начальник отдела точной медицины и нейрогенетики университета Калифорнии в Чапел-Хилле.
Адъювантная иммунотерапия рака молочной железы
Дженнифер Литтон: Люди с тройным негативным раком молочной железы имеют меньше вариантов лечения, чем другие пациенты с этим типом рака. Хотя пембролизумаб (продаваемый как Кейтруда) первоначально был разработан для терапии прогрессирующей меланомы, позднее он был одобрен для лечения и других онкологических заболеваний. Это исследование ответит на важные вопросы об использовании пембролизумаба в адъювантном режиме у пациентов с тройным негативным раком молочной железы высокого риска. Исследование Keynote 522 предоставило важную информацию о использовании пембролизумаба неоадъювантно у этих пациентов, но оно также оставило много вопросов о продолжительности лечения и роли этого препарата в послеоперационном периоде. Это исследование прольет свет на вышеперечисленные вопросы и станет важным руководством для продвижения вперед.
Дженнифер Литтон — вице-президент по клиническим исследованиям и профессор отделения медицинской онкологии молочной железы Онкологического центра доктора медицинских наук Андерсона.
