Доставка РНК с помощью человеческих вирусоподобных частиц
РНК-карго переносится в культивируемые клетки с помощью системы доставки, содержащей лишь человеческие компоненты.
РНК все чаще привлекает внимание исследователей как мощное терапевтическое средство в различных областях — от разработки вакцин до заместительной белковой терапии. Во многих других сферах, помимо создания вакцин, главным препятствием для клинической разработки служит нехватка эффективных методов доставки РНК к специфическим клеткам и тканям. В недавней статье в Science Сегел с соавт. [1] сообщили о новой стратегии доставки РНК, позаимствованной из генома человека. В подходе используется белок из человеческого ретровируса с редкой способностью упаковывать свою РНК и транспортировать ее за пределы клетки с помощью вирусоподобных частиц (VLP). Авторы показывают, что их подход, названный «селективное эндогенное капсидирование для клеточной доставки» (SEND) позволяет доставлять в клетки экзогенные мРНК-карго, такие как Cre и Cas9, in vitro без использования компонентов, взятых от других видов. Хотя такая стратегия доставки находится еще на ранней стадии разработки, будучи полностью человеческой системой, она может стать более безопасной альтернативой ныне существующим методам.
▶ Читайте также: Стартапы способствуют запуску новой волны мРНК-терапии
В настоящее время наиболее широко используемым методом доставки РНК являются липидные наночастицы, собранные из натуральных и синтетических ионизируемых аминолипидов. Липидные наночастицы стали подспорьем замечательного успеха мРНК-вакцин против SARS-CoV-2, но в прочих ситуациях они имеют ряд недостатков. Среди них — неуверенность относительно их безопасности и эффективности при неоднократном введении и при пересечении биологических барьеров для воздействия на специфические типы клеток. Вирусные последовательности, встроенные в разные области человеческого генома, создают заманчивую возможность использовать их естественные функции для доставки терапевтической РНК. Ретроэлементы в человеческом геноме составляют около 8 % [2]. Хотя большинство эндогенных ретровирусных генов утратили свои функции, некоторые продолжают участвовать в физиологии человека. Сообщалось, что ряд ретроэлементов сохраняют часть своей исходной функциональности, такой как связывание и перенос мРНК и формирование капсида внутри клетки [2].
Чтобы найти ретроэлементные гены-кандидаты для доставки ДНК, Сегел с соавт. [1] рассмотрели консервативные эндогенные ретроэлементы, сфокусировавшись на гомологах структурных ретровирусных белков Gag, содержащих коровый капсидный домен. Этот домен защищает геном как от ретротранспозонов, так и от вирусов, формируя VLP; это позволяет предположить, что содержащие его белки могут быть способны переносить другие РНК. Авторы сузили поле поиска до белков, которые консервативны у людей и мышей и имеют определяемые уровни РНК, поскольку такие белки более склонны сохранять функциональность в клетках млекопитающих. Они сделали скрининг наиболее подходящих белков в клетках бактерий и млекопитающих для определения того, секретируются ли они в виде внеклеточных везикул, таких как VLP. Фракция VLP оказалась наиболее обогащена мышиным (Mus musculus) PEG10, который также обнаруживается на ощутимом уровне в сыворотке мышей. Более того, VLP, сформированные белком PEG10, содержали полноразмерный мРНК-транскрипт Peg10.
Чтобы исследовать, могут ли такие мышиные PEG10 VLP включать в себя неродственные РНК, Сегел с соавт. [1] поместили по краям последовательности, кодирующей рекомбиназу Cre, 5′- и 3′-нетранслируемые участки (UTR) Peg10 и провели котрансфекцию этого конструкта совместно с PEG10 в клетки мышиной нейробластомы Neuro2a. Они также сконструировали VLP с добавлением белка оболочки вируса везикулярного стоматита (VSVg) для усиления доставки в клетки. Примечательно, что PEG10 VLP с VSVg секретировались во внеклеточных везикулах и переносили мРНК Cre mRNA в клетки loxP–GFP (рис. 1). Это наблюдение дает основание предположить, что добавление UTRs Peg10 к мРНК-карго позволяет PEG10 VLP переносить выбранную мРНК, и что для проникновения в клетку требуется вирусный фузогенный белок. Человеческий PEG10, подобно мышиному ортологу, может формировать VLP и переносить мРНК.
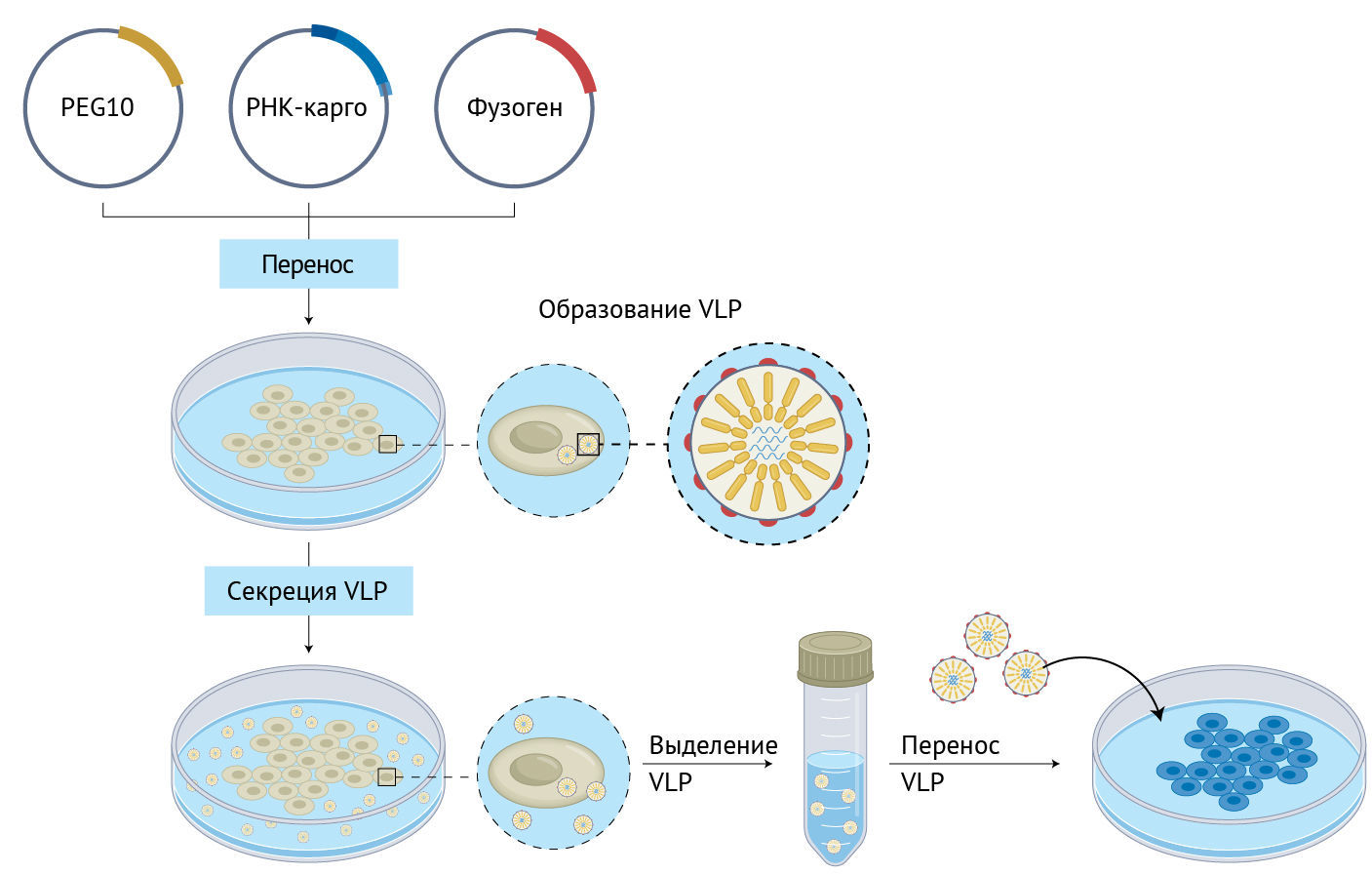
Такая комбинация PEG10, модифицированной мРНК и фузогена образует систему SEND. Чтобы сделать эту систему полностью эндогенной, Сегел с соавт. [1] оценили фузогены мыши и человека, которые могли бы заменить VSVg. Они сосредоточились на синцитине — эндогенном фузогенном трансмембранном белке, который возник в результате эволюции из ретровирусных элементов и применялся для псевдотипирования лентивирусов с целью доставки нуклеиновых кислот. Авторы обнаружили, что у мыши фузогенные синцитины — SYNA и SYNB — имели паттерн экспрессии, сходный с таковым для мышиного PEG10, и что мышиный SYNA может успешно заменить VSVg при переносе мРНК Cre в фибробласты кончика хвоста. Синцитины человека (ERVW-1 и ERVFRD-1) работают сходным образом, что делает SEND полностью человеческой системой для функционального переноса генов — по крайней мере, in vitro.
Для проверки универсальности SEND авторы также использовали ее для доставки крупной мРНК SpCas9 и протестировали ее функциональность, оценивая генное разобщение в клетках нейробластомы мыши Neuro2a, конститутивно экспрессирующих одиночную направляющую РНК (sgRNA) против Kras. Система SEND доставляла мРНК-карго Cas9 и вызывала значительное — 60 % — редактирование локуса Kras в клетках-реципиентах. Однако SEND оказалась неспособна доставить sgRNA-карго в клетки, экспрессирующие Cas9. Тогда авторы скомбинировали sgRNA и мРНК Cas9, чтобы получить вектор «все в одном». Этот вектор усилил редактирование гена Kras в клетках Neuro2a с помощью мышиной системы SEND на 30 % и редактирование гена VEGFA в клетках HEK293 с помощью человеческой SEND на 40 %.
Исследование Сегела с соавт. [1] примечательно в качестве первого примера эндогенной системы, способной осуществлять упаковку, секрецию и доставку специфических мРНК. Прежде чем рассматривать ее практическое применение, необходимо провести обширные дальнейшие исследования. Система SEND была изучена только in vitro; необходимо оценить ее работу in vivo. Как сообщалось ранее [3], мышиный PEG10 выполняет множество функций в плаценте и при развитии нервной ткани, и неизвестно, повлияет ли добавление белка PEG10 извне на его нативные функции. Дополнительные вопросы касаются возможных аутоиммунных реакций при экспрессии эндогенного белка в другом биологическом контексте, а также биораспределения, токсичности, эффективности и масштабируемости.
Работы будущего также должны провести сравнение системы SEND с существующими системами доставки мРНК, включая липидные наночастицы, применяемые для создания вакцин против SARS-CoV-2 [4, 5], а также многими другими подходами, проходящими сейчас клинические испытания [6]. Будет важно понять, обладает ли система внутренней специфичностью по отношению к клеткам и можно ли влиять на такую специфичность биоинженерными методами. Следующее поколение липидных наночастиц включает таргетные стратегии, которые недавно показали специфичность к типам клеток, мощную эффективность и безопасность на различных животных моделях воспаления, злокачественных опухолей и генетических заболеваний — с применением одной лишь мРНК или комбинации с sgRNA для нокаута онкогенов [7–10]. Тем не менее, система SEND могла бы стать более безопасной и даже более эффективной альтернативой. После дальнейшей разработки она может иметь преимущества в решении биологических вопросов, доставке вакцин и лечении болезней, что особенно важно в случае хронических заболеваний, требующих пожизненной терапии.
