Хроническая обструктивная болезнь легких (перевод статьи из Nature)
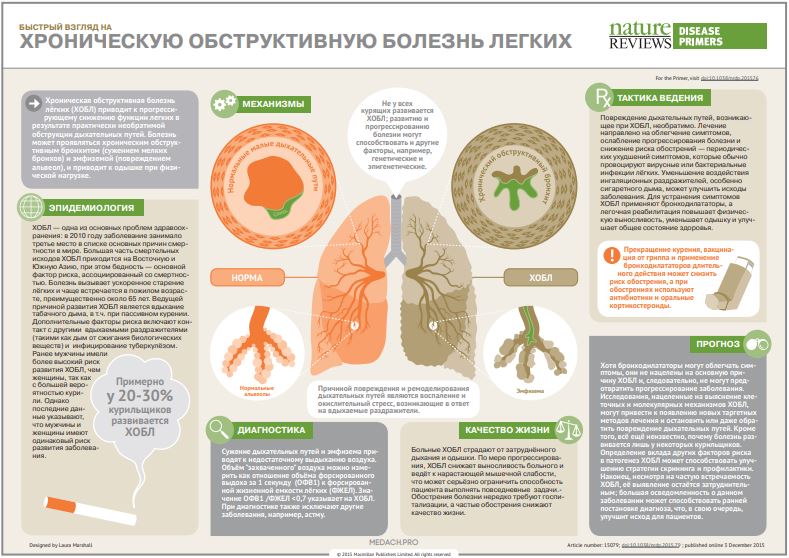
ХОБЛ (инфографика), открыть PDF
Хроническая обструктивная болезнь легких (ХОБЛ) является одной из самых актуальных проблем мирового здравоохранения, характеризующейся неуклонно растущими показателями заболеваемости и смертности. Вследствие этого, в целях поддержания здоровья населения, необходимо повышать уровень осведомлённости о заболевании, а также внедрять эффективную систему терапии ХОБЛ. Лечение стабильной ХОБЛ должно основываться на степени тяжести болезни, оцениваемой по степени ограничения воздушного потока, выраженности симптомов и наличия факторов риска обострения. Ведущее место в терапии ХОБЛ занимают бронходилатирующие препараты. Последние достижения в разработке М-холиноблокаторов и β2-адреномиметиков длительного действия позволяют не только улучшить функционирование дыхательной системы в целом и уменьшить выраженность симптомов, но и снизить как частоту обострений, так и темп прогрессирования бронхообструкции. С учетом частой этиологической связи ХОБЛ с воспалительными изменениями дыхательных путей, пациентам, подверженным частым обострениям, а так же при сочетании ХОБЛ с бронхиальной астмой, рекомендовано применение ингаляционных глюкокортикостероидов наряду с индивидуально подобранным режимом терапии ингаляционными бронходилататорами длительного действия. В настоящее время ведется поиск новых терапевтических мишеней в патофизиологическом каскаде развития ХОБЛ в целях формирования новых подходов к лечению, которые бы позволили уменьшить скорость прогрессирования заболевания, развитие сопутствующих заболеваний и снизить величину показателя смертности.
Введение
Хроническая обструктивная болезнь легких (ХОБЛ) является одной из самых актуальных проблем мирового здравоохранения, характеризующейся неуклонно растущими показателями заболеваемости и смертности. Согласно статистике, ХОБЛ подвержено около 7% всего населения в мире. Среди лиц старше 65 лет частота встречаемости повышается до 10%. В действительности большое число случаев ХОБЛ остаются недиагностированными, в связи с чем реальные цифры, вероятно, значительно превышают официальные данные. По прогнозам, к 2020 году ХОБЛ станет третьей по счёту причиной всех летальных исходов в мире. ХОБЛ характеризуется хроническими воспалительными изменениями в легочной ткани и периферических дыхательных путях в ответ на длительное воздействие вредных частиц или газов. В большинстве случаев причиной развития ХОБЛ являются вредные частицы, содержащиеся в сигаретном дыме. При ХОБЛ развивается прогрессирующая и необратимая бронхообструкция, сопровождающаяся увеличением резистентности стенок мелких бронхов и увеличением эластичности легочной ткани в результате эмфизематозного поражения. Основные симптомы ХОБЛ - одышка и повышенная продукция мокроты. Одышка при физической нагрузке может быть ранним признаком ХОБЛ. Причинами одышки являются сужение просвета дыхательных путей вследствие развития фиброза и утолщения их стенок, а так же спадение стенок бронхиол в процессе выдоха из-за снижения радиального натяжения, вызванного разрушением альвеолярной ткани. Усиление продукции мокроты, в свою очередь, связано с увеличением количества бокаловидных клеток и гиперплазией слизистых желез. Поскольку ХОБЛ приводит к необратимой прогрессирующей бронхообструкции, вся терапия (как медикаментозная, так и немедикаментозная) должна быть направлена на контроль симптоматики, улучшение качества жизни и переносимости физической нагрузки, профилактику обострений, сопутствующих заболеваний, а также на снижение темпов прогрессирования и улучшение прогноза. В частности, последние исследования сообщают о том, что именно одышка является наиболее серьезным фактором, оказывающим негативное влияние на качество жизни пациентов, следовательно, именно с ней нужно бороться в первую очередь. Для достижения перечисленных целей, помимо индивидуально подобранного медикаментозного лечения, рекомендуется снизить воздействие факторов риска (в особенности курения), а так же проводить оксигенотерапию, своевременную вакцинацию против дыхательных инфекций в соответствии с состоянием пациента и выраженностью заболевания на ранних этапах лечения с последующей оценкой эффективности предпринимаемых терапевтических мер. Последние клинические наблюдения подтвердили гипотезу о том, что чрезмерный выброс медиаторов воспаления из легочной ткани в кровоток при ХОБЛ может приводить к возникновению системной воспалительной реакции, в свою очередь способствующей возникновению или прогрессированию ИБС, сердечной недостаточности, анемии, сахарного диабета, депрессии, остеопороза, рака лёгкого. Таким образом, у пациентов с ХОБЛ важно контролировать течение и сопутствующих заболеваний. В данной статье представлен обзор нынешних подходов к лечению ХОБЛ, а также рассмотрены последние достижения в области разработки и применения бронходилататоров длительного действия. Помимо этого обсуждаются новые терапевтические мишени для фармакотерапии ХОБЛ.
Текущие рекомендованные подходы к терапии ХОБЛ
Бронходилататоры
Бронходилататоры - основная группа препаратов, рекомендованная к применению у пациентов с ХОБЛ. Назначение их должно проводиться с учетом выраженности клинических симптомов, факторов риска обострения и степени бронхообструкции. Бронходилататоры способствуют развитию долговременнного улучшения симптоматики и переносимости физической нагрузки даже при минимальных положительных изменениях по данным спирографии, так как ингаляционные препараты этой группы уменьшают перерастяжение легочной ткани, возникающее в процессе активности. По последним данным, эффект бронходилататоров должен быть оценен по степени снижения сопротивления дыхательных путей и по изменению величины дыхательного объема в покое, нежели чем по величине ОФВ1, особенно в случае оценки выраженности одышки. Кроме того, следует учитывать положительные изменения в степени переносимости физической нагрузки и качестве жизни пациента.
Возможно применение бронходилататоров в ингаляционной или таблетированной формах, перкутанно, а также введение их растворов подкожно или внутривенно. Чаще всего на практике используются ингаляционные препараты, так как местное введение обеспечивает развитие максимального эффекта при минимальных системных побочных реакциях. Ингаляции могут осуществляться при помощи простого дозированного аэрозольного ингалятора (ДАИ), мелкодисперсного аэрозольного ингалятора (МАИ), дозированного порошкового ингалятора (ДПИ) или небулайзера. ДАИ, МАИ и ДПИ позволяют облегчить процесс выполнения терапевтических назначений, что, во-первых, имеет большое значение во взаимодействии пациента с лечащим врачом (повышение комплаенса), а во-вторых, снижает потребность в назначении добавочных препаратов. Выбор способа введения лекарственного средства должен основываться как на состоянии пациента (степени бронхообструкции и выраженности сопутствующих заболеваний), так и на его способности следовать технике проведения ингаляций в целях создания условий для адекватного поступления лекарственного вещества .
Класс препаратов - бронходилататоров включает такие группы ЛС как β2- адреномиметики, антихолинергические препараты и метилксантин, который в последнее время назначается редко. В случае неэффективности монотерапии, возможно сочетание разных лекарственных средств описываемого класса, так как механизмы действия каждой группы препаратов различны.
β2- адреномиметики активируют β 2-адренорецепторы в составе гладкой мускулатуры стенок дыхательных путей. Эти рецепторы сопряжены с активирующим аденилатциклазу G-белком, поэтому связь агонистов с ними приводит к повышению внутриклеточного уровня цАМФ и активации протеинкиназы A. Подобные клеточные изменения способствуют инактивации киназы легких цепей миозина и усилению работы соответствующей фосфатазы. Более того, β2- адреномиметики способствуют открытию кальций-зависимых калиевых каналов, последующему развитию гиперполяризации в гладкомышечных клетках (ГМК), а следовательно, мышечному расслаблению и бронходилатации.
Антихолинергические средства (М-холиноблокаторы) инактивируют M3 мускариновые холинорецепторы, находящиеся в составе ГМК и подслизистых желез. Результатом действия М-холиноблокаторов, таким образом, становится расслабление мышечных волокон, снижение секреции слизи и расширение просвета бронхов .
Метилксантин является конкурентным неселективным ингибитором фосфодиэстеразы, действие которого проявляется в повышении концентрации внутриклеточного цАМФ с последующей миорелаксацией и бронходилатацией.
Бронходилататоры короткого действия
Антихолинергические препараты и β2- адреномиметики короткого действия рекомендуются к использованию у пациентов с умеренной непостоянной клинической симптоматикой. Действие β 2- адреномиметиков развивается быстрее, нежели м-холиноблокаторов, в то время как максимальная эффективность в отношении бронходилатации у последних выше. Возможно использование монотерапевтического подхода, однако более предпочтительно сочетанное применение двух групп препаратов короткого действия, так как суммарное их действие, направленное на расширение бронхов, в комбинации проявляется сильнее.
Бронходилататоры длительного действия
Антихолинергические препараты длительного действия
Примерами препаратов данной группы являются тиотропий, гликопирроний, аклидиний и умеклидиний. Эти вещества имеют больший аффинитет в отношении рецепторов М3, нежели М2 и диссоциируют из связи с рецептором типа М3 медленне, что способствует длительному расширению просвета бронхов.
Тиотропий – наиболее изученное к настоящему времени антихолинергическое средство длительного действия для ежедневного применения, избирательно связывающееся с М1 и М3-типами рецепторов. В литературе имеются данные о том, что при систематическом применении тиотропия отмечается достоверное улучшение легочной функции (увеличение ОФВ1 и ФЖЕЛ) и качества жизни, а так же повышение переносимости физической нагрузки, уменьшение выраженности одышки и снижение частоты обострений ХОБЛ. Кроме того, многими авторами предполагается, что прием тиотропия способствует замедлению темпа снижения ОФВ1 у пациентов с ХОБЛ умеренно тяжелого течения –. Существуют противоречивые данные о неблагоприятном влиянии тиотропия на сердечно-сосудистую систему. В одном из последних проведенных мета-анализов показано, что применение мелкодисперсного аэрозольного ингалятора, содержащего тиотропий, — «Респимат» (Respimat®)- ассоциировано со значительным повышением риска летального исхода. Особенно часто описанная зависимость отмечается у пациентов с ХОБЛ тяжелого течения, вынуждающего использовать высокие суточные дозы препарата в процессе терапии. В то же время, данные продолжительного рандомизированного исследования показали, что препараты тиотропия снижают риск смерти от любых причин на 11 % по сравнению с плацебо. Сходные результаты были получены в ходе одного из последних рандомизированных двойных слепых исследований, которое подтвердило безопасность применения мелкодисперсного аэрозольного ингалятора с тиотропием.
Гликопирроний – антихолинергическое средство для ежедневного приема, так же селективно взаимодействующее с M1 и M3 типами холинорецепторов. Гликопирроний эффективно улучшает показатели функции легких (в частности, ОФВ1) и снижает выраженность одышки и частоту обострений.
Аклидиний селективно блокирует рецепторы M3 типа и рекомендован к ежедневному приему. Длительность действия аклидиния короче, чем у тиотропия, поэтому для достижения эффекта от применения данного препарата рекомендуется его двукратный прием в течение суток . Некоторые исследования показали развитие значительных улучшений параметров (спады и пики) ОФВ1. Кроме того, как и другие препараты группы, аклидиний положительно влияет на снижение выраженности одышки и частоты обострений, что было продемонстрировано в ряде плацебо-контролируемых исследований. Умеклидиний связывается с M3 рецепторами и принимается 1 раз в сутки. Препарат способствует улучшению параметров ОФВ1 (спады) и позволяет снизить необходимость частого приема β 2- адреномиметиков короткого действия. Умеклидиний используется в сочетании с адреномиметиком длительного действия вилантеролом в составе ингалятора.
β2- адреномиметики длительного действия
К β 2- адреномиметикам длительного действия относятся такие препараты, как сальметерол, формотерол, индакатерол, олодатерол и вилантерол. До настоящего времени антихолинергические средства длительного действия имели преимущества в назначении перед β2- адреномиметиками длительного действия, в связи с эффективностью первых на протяжении 24 часов, а так же удобством приема (1 раз в сутки) и дозирования. β2- адреномиметики, в свою очередь, для достижения адекватного эффекта требуют двухкратного приема в течение суток. В настоящее время, с появлением адреномиметиков, которые можно применять раз в сутки, назначение того или иного средства определяется характером сопутствующей патологии у пациента и развитием побочных эффектов.
Сальметерол и формотерол используются для поддержания стабильности течения ХОБЛ. Особенностью формотерола по сравнению с сальметеролом является более быстрое развитие и большая сила действия. Оба препарата значительно улучшают легочную функцию, уменьшают тяжесть одышки, улучшают прогноз и качество жизни пациента, что было продемонстрировано в плацебо-контролируемых исследованиях.
Для индакатерола характерно быстроразвивающееся и длительное (до 24 часов) действие, что, вероятно, связано с его высоким аффинитетом к липидным рафтам в составе плазматической мембраны клето . Рандомизированные контролируемые исследования показали снижение выраженности одышки и частоты развития обострения, а так же улучшение функции легких (ОФВ1) при приеме данного препарата. Кроме того, отмечена большая эффективность индакатерола, принимаемого однократно, по сравнению с препаратами, требующими приема дважды в сутки.
Олодатерол - β2- адреномиметик длительного действия с рекомендованным однократным режимом ежедневного применения используется для терапии ХОБЛ в Европе и США. Выпускается в составе мелкодисперсного аэрозольного ингалятора. Клинические исследования выявили улучшение параметров ОФВ1( как пиков, так и спадов), а так же качества жизни. Побочные эффекты в группе принимавшей олодатерол не отличались от таковых, наблюдаемых в группе, плучавшей плацебо. Вилантерол так же, как и олодатерол, характеризуется длительным действием и быстрым развитием эффекта. Тем не менее, данный препарат не рекомендуется для монотерапии и применяется в сочетании с умеклидинием или флутиказона фуроатом.
Сравнение β 2- адреномиметиков и антихолинергических препаратов длительного действия
Как м-холиноблокаторы, так и β2-адреномиметики длительного действия могут применяться раз в день, поэтому с клинической точки зрения важен вопрос: какая группа препаратов предпочтительна в терапии ХОБЛ? В одном из рандомизированных контролируемых исследований было проведено сравнение препаратов длительного действия с однократным режимом приема: индакатерола (группа β 2- адреномиметиков) и тиотропия (группа антихолинергических средств). По результатам проводимых в течение 26 недель наблюдений за пациентами с ХОБЛ умеренно тяжелого и тяжелого течения, к 12 неделе преимущество индакатерола в улучшении легочной функции и ОФВ1 в сравнении с тиотропием не оставляло сомнений, однако к 26 неделе оба препарата сравнялись по эффективности, которая была значительно выше плацебо. Данное исследование показало более значительно снижение выраженности одышки (транзиторный индекс одышки) и улучшение показателей качества жизни, определяемого состоянием здоровья (опросник St. George) на фоне приема индакатерола, чем при приеме тиотропия. По степени снижения частоты осложнений и по переносимости терапии оба препарата показали примерно одинаковые результаты. Другое недавно проведенное рандомизированное контролируемое исследование, в котором в течение 12 недель принимали участие пациенты с умеренно тяжелым и тяжелым течением ХОБЛ, выявило большую эффективность индакатерола по сравнению с тиотропием в уменьшении выраженности одышки, улучшении показателей качества жизни и снижении потребности в приеме препаратов короткого действия. В то же время влияние на величину ОФВ1 у обоих ЛС было примерно одинаковым.
Еще в одном рандомизированном контролируемом исследовании, проведенном с участием пациентов с ХОБЛ тяжелого течения и как минимум одним умеренным или тяжелым обострением в течение года, была показана равная эффективность как тиотропия, так и индакатерола в улучшении параметров ОФВ1, снижении частоты обострений и прогноза жизни и здоровья .
Комбинированная терапия
В случае, если с помощью монотерапии бронходилататором длительного действия не удается достичь должного контроля симптоматики, пациенту назначается еще один бронходилататор из другой группы. Мета-анализ пяти проведенных исследований, в которых использовалось сочетанное применение антихолинергического препарата длительного действия тиотропия и β2- адреномиметика короткого действия- сальметерола (или индакатерола, формотерола) показало лишь небольшое усиление эффективности во влиянии на увеличение пикового значения ОФВ1 и на улучшение прогноза и качества жизни по сравнению с монотерапией тиотропием . В степени влияния на частоту осложнений и переносимости терапии особенных преимуществ у комбинированной терапии не выявлено. Недавно для применения был одобрен дозированный порошковый ингалятор, содержащий комбинацию умеклидиния и вилантерола. Клинические исследования показали значительное улучшение показателя ОФВ1 по сравнению с монотерапией этими препаратами, а так же в сравнении с тиотропием. Комбинированное лечение с использованием ингалятора, в отличие от монотерапии и плацебо, так же выявило значительно улучшение качества жизни, связанного с состоянием здоровья и выраженности одышки, оцененной по индексу. Эффективность сочетания умеклидиния и вилантерола в снижении частоты обострений ХОБЛ оказалась сравнимой с таковой у умеклидиния при его изолированном применении. Другой недавно одобренный к применению у пациентов с ХОБЛ дозированный порошковый ингалятор, содержащий индакатерол и гликопирроний, тоже показал преимущества в эффективности (в частности по показателю ОФВ1) по сравнению с аналогичными препаратами, использованными в качестве монотерапии, а так же по сравнению с тиотропием. Комбинация индакатерола и гликопиррония выявила значительное положительное влияние на частоту обострений и качество жизни пациентов в сравнении с монотерапией индакатеролом или тиотропием .
Метилксантин
Метилксантин является препаратом, дополняющим основную терапию бронходилататорами и ингаляционными глюкокортикостероидами. У пациентов с ХОБЛ чаще используется пролонгированная таблетированная форма теофиллина. Для него характерен более умеренный бронходилатирующий эффект по сравнению с ингаляционными бронходилататорами. Для достижения эффективного расширения просвета бронхов рекомендовано поддержание плазменного уровня теофиллина в диапазоне от 10 до 20 мг/мл. Вследствие доказанной токсичности метилксантиновых препаратов необходимо проведение строго мониторинга их концентрации в крови. В последние годы появились сообщения о противовоспалительном эффекте низких доз теофиллина (приблизительно, 5 мг/мл), который, вероятно, реализуется за счет усиления экспрессии НDAC2 b и активации альвеолярных макрофагов.
Ингаляционные кортикостероиды
ХОБЛ – это воспалительное заболевание, при котором наблюдается как воспаление дыхательных путей, так и системное воспаление. Поскольку терапия ингаляционными кортикостероидами (ИКС) способствует уменьшению воспаления, полагают, что терапия ИКС может улучшать клинические исходы при ХОБЛ. В нескольких клинических испытаниях, в том числе в крупнейшем рандомизированном контролируемом испытании, было установлено, что монотерапия ИКС снижает число обострений и умеренно замедляет прогрессирование одышки, но при этом минимально влияет или не оказывает влияния на функцию легких и выживаемость пациентов с ХОБЛ . Таким образом, терапию ИКС следует добавлять к базисной терапии, включающей бронхолитики, при соответствующих клинических фенотипах ХОБЛ; ИКС не рекомендуются в качестве монотерапии для пациентов со стабильной ХОБЛ. К клиническим фенотипам, для которых требуется дополнительное лечение ИКС, относятся пациенты с частыми обострениями, а также пациенты с перекрестным фенотипом «ХОБЛ-бронхиальная астма», поскольку у пациентов с данными фенотипами выражено легочное воспаление . В прошлых испытаниях было высказано мнение о том, что ИКС могут применяться в качестве комбинированной терапии совместно с бронхолитиками для уменьшения частоты обострений ХОБЛ у тяжелых/очень тяжелых пациентов. В одном испытании комбинация сальметерола и флутиказона достоверно улучшала легочную функцию и КЖ, связанное со здоровьем, а также снижала частоту обострений в сравнении с плацебо, монотерапией сальметеролом и монотерапией флутиказоном . В другое клиническое испытание были включены 1323 пациента со стабильной, преимущественно тяжелой ХОБЛ, которые были рандомизированы для приема комбинации сальметерол/флутиказон или монотерапии тиотропием на протяжении двух лет. Не было отмечено различий в частоте обострений, хотя комбинация сальметерола и флутиказона снижала смертность и улучшала КЖ, связанное со здоровьем . С другой стороны, при последующем анализе данного испытания было установлено, что пневмония достоверно чаще наблюдалась в группе, использовавшей сальметерол/флутиказон, несмотря на меньшую смертность . Также было показано, что другой комбинированный ингаляционный препарат, применяющийся дважды в день (будесонид/формотерол) увеличивает минимальный ОФВ1, при этом наблюдалось достоверно большее улучшение в сравнении с монотерапией формотеролом. В группе будесонид/формотерол отмечено достоверно большее время до первого обострения в сравнении с группой формотерола, а также достоверно большее улучшение вторичных исходов, в том числе КЖ, связанного с симптомами и здоровьем . Помимо комбинированных ингаляционных препаратов, применяемых дважды в день, для лечение ХОБЛ в США одобрен применяемый раз в сутки порошковый ингалятор, содержащий флутиказона фуроат и вилантерол. Многоцентровое 24-недельное испытание, в которое были включены стабильные пациенты с умеренной и тяжелой ХОБЛ и рандомизированы для приема комбинации флутиказон/вилантерол, флутиказона, вилантерола или плацебо, показало, что комбинация флутиказон/вилантерол умеренно снижала частоту умеренных и тяжелых обострений в сравнении с монотерапией вилантеролом . Частота пневмоний была более высокой в группе комбинации флутиказон/вилантерол . Поскольку доказано, что ДДМХБ также предотвращают обострения , а два типа длительно действующих бронхолитиков (ДДБА и ДДМХБ, включая комбинированные препараты) сегодня назначаются пациентам с тяжелой ХОБЛ, оставалось неясным, дают ли ингаляционные кортикостероиды достоверные дополнительные преимущества пациентам с тяжелой ХОБЛ, получаюшим оба типа длительно действующих бронхолитиков. Для получения ответа на этот вопрос было проведено недавнее 12-месячное рандомизированное контролируемое испытание, в которое были включены 2485 пациентов с тяжелой ХОБЛ и наличием обострений ХОБЛ в анамнезе . Пациенты получали тройную терапию, включавшую тиотропий, сальметерол и флутиказона пропионат, в течение 6-недельного вводного периода. Пациентов затем рандомизировали для приема тройной терапии или терапии с отменой флутиказона в три этапа в течение 12 недель; пациенты наблюдались до недели 52. Результаты показали, что в группе с отменой кортикостероидов не было отмечено худших результатов в отношении предотвращения обострений и улучшения одышки в сравнении с группой продолжающих кортикостероиды, хотя на неделе 52 были отмечены небольшие изменения ОФВ1 и состояния здоровья в группе отмены кортикостероидов. Данный отчет позволяет предположить, что дополнительные ИКС могут не понадобиться для снижения риска обострения ХОБЛ у тяжелых пациентов с ХОБЛ, пролеченных ДДБА и ДДМХБ, хотя также вероятно, что потребность в дополнительных ИКС может зависеть от фенотипа ХОБЛ (воспалительный или невоспалительный).
Ингибиторы ФДЭ-4
Фосфодиэстераза-4 (ФДЭ-4) относится к семейству фосфодиэстераз циклических нуклеотидов (ФДЭ) и включает 4 семейства генов (A–D) . Как и другие ФДЭ, ФДЭ-4 гидролизует циклический аденозинмонофосфат (цАМФ). Ингибиторы ФДЭ-4 блокируют гидролиз цАМФ, что ведет к повышению внутриклеточного уровня цАМФ. Установлено, что ингибирование ФДЭ-4 уменьшает воспаление и может способствовать расслаблению гладкой мускулатуры дыхательных путей. Рофлумиласт – пероральный ингибитор ФДЭ-4, одобренный для применения у пациентов с ХОБЛ в США. Для анализа эффектов ингибиторов ФДЭ-4 были проведены рандомизированные контролируемые испытания, а также мета-анализ. Рандомизированное контролируемое испытание, в которое был включен 3091 пациент с ХОБЛ, показало, что рофлумиласт достоверно улучшает минимальный ОФВ1 и уменьшает частоту умеренных и сильных обострений в ходе 52-недельного испытания . В другое испытание были включены 933 пациента с умеренной и тяжелой ХОБЛ, которые были рандомизированы для приема комбинации рофлумиласт/сальметерол и монотерапии сальметеролом, а 743 пациента были рандомизированы для приема комбинации рофлумиласт/тиотропий и монотерапии тиотропием . Рофлумиласт достоверно улучшал минимальный ОФВ1, хотя в группах рофлумиласта чаще наблюдались такие побочные эффекты, как тошнота, диарея и потеря веса. В ходе мета-анализа 23 рандомизированных испытаний рофлумиласта и циломиласта (еще одного ингибитора ФДЭ-4) в сравнении с плацебо было установлено, что лечение ингибитором ФДЭ-4 умеренно улучшает ОФВ1 и снижает риск обострений, но при этом слабо влияет на КЖ, связанное со здоровьем . Эти исследования говорят о том, что пероральные ингибиторы ФДЭ-4 могут использоваться в качестве дополнительной поддерживающей терапии у пациентов с тяжелой ХОБЛ для предотвращения обострений. На данный момент не установлено, дают ли эти препараты дополнительные преимущества в рамках комбинированной терапии с применением прочих лекарственных средств (ДДБА и ДДМХБ, или ДДБА и ингаляционные кортикостероиды)
Новые терапевтические мишени будущей фармакотерапии ХОБЛ
Важными целями лечения ХОБЛ являются замедление прогрессирования заболевания, профилактика обострений, а также снижение смертности. Хотя последние достижения в области разработок бронхолитиков позволили достигнуть значимых бронхолитических эффектов, улучшения симптоматики и качества жизни, сегодняшние препараты, в том числе длительно действующие бронхолитики, существенно не замедляют прогрессирование заболевания, не уменьшают смертность и риск обострений, поскольку бронхолитики не обладают значимыми противовоспалительными эффектами. Показано, что ХОБЛ ассоциируется с хроническим воспалением периферических дыхательных путей и легочной паренхимы, а также с системным воспалением, обусловливающим сопутствующую патологию, в том числе сердечно-сосудистые заболевания. Таким образом, естественно предположить, что эффективная противовоспалительная терапия необходима для замедления прогрессирования заболевания и уменьшения смертности среди пациентов с ХОБЛ. Однако, ни одна из ныне используемых групп препаратов, включая ингаляционные кортикостероиды и ингибиторы ФДЭ-4, не может эффективно контролировать воспаление, лежащее в основе ХОБЛ, у пациентов с данной патологией. Последние достижения в рамках исследований фонового воспаления предполагают новые терапевтические мишени для противовоспалительных методик лечения у пациентов с ХОБЛ (Рис. 1) . Среди возможных терапевтических подходов можно назвать новые антиоксиданты, ингибиторы инфламмасом, антагонисты цитокинов и хемокинов, ингибиторы провоспалительных киназ, антипротеазы, устранение стероидорезистентности и эпигенетическую модуляцию; некоторые из них уже проходят клинические испытания.
Терапевтические мишени будущей фармакотерапии ХОБЛ. Последние достижения в рамках исследований хронического воспаления, лежащего в основе заболевания, позволили определить новые терапевтические мишени у пациентов с ХОБЛ. Среди возможных терапевтических подходов можно назвать новые антиоксиданты, ингибиторы инфламмасом, антагонисты цитокинов и хемокинов, ингибиторы провоспалительных киназ, антипротеазы, эпигенетическая модуляция. IKK: ингибитор NF κB-киназы (киназы ядерного фактора «Каппа-Би»); ИЛ: интерлейкин; JAK: янус-киназа; MAPK: митоген-активируемая киназа; NRF-2: NF-E2-ассоциированный фактор (фактор, ассоциированный с ядерным фактором NF-E2); NLRP3: Семейство NOD (нуклеотидсвязывающий олигомерный домен)-подобных рецепторов, содержащих пириновый домен-3; PI3K: фосфоинозитид-3-киназа
Заключение
Последние достижения в области разработок длительно действующих бронхолитиков обеспечили значимое улучшение симптоматики и легочной функции у пациентов с ХОБД. Эти препараты также в некоторой степени снижают риск обострений и скорость прогрессирования ограничения воздушного потока. Для создания новейших стратегий терапии ХОБЛ, которые смогут значительно замедлить прогрессирование заболевания, уменьшить смертность и частоту сопутствующей патологии, требуются новые терапевтические подходы для воздействия на лежащее в основе ХОБЛ хроническое воспаление и патофизиологические изменения в легких; в настоящий момент такие подходы проходят клинические испытания.
Список сокращений
цАМФ: циклический аденозинмонофосфат ХОБЛ: Хроническая обструктивная болезнь легких ОФВ1: Форсированный объем выдоха за 1 секунду ФЖЕЛ: Форсированная жизненная емкость легких ДПИ: дозированный порошковый ингалятор ДАИ: дозированный аэрозольный ингалятор ЛС: лекарственное средство ГМК: гладкомышечные клетки ПИ: порошковый ингалятор; ОФВ1: Объем форсированного выдоха за первую секунду; ФЖЕЛ: Форсированная жизненная емкость легких; ИКС: Ингаляционный кортикостероид; ДДБА: длительно действующий β2-агонист; ДДМХБ: длительно действующие м-холиноблокаторы; ДИ: дозирующий ингалятор; КЖ: качество жизни; КДБА: короткодействующий β2-агонист; SGRQ: Анкета госпиталя Святого Георгия для оценки дыхательной функции (St. George's respiratory questionnaire); ИМА: Ингалятор с «мягким» аэрозолем (Soft mist inhaler); ДИО: динамический индекс одышки.
Источники
-
Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM: Global burden of COPD: systematic review and meta-analysis.Eur Respir J 2006, 28:523-532.
-
Ford ES, Croft JB, Mannino DM, Wheaton AG, Zhang X, Giles WH: COPD surveillance--United States, 1999–2011.Chest 2013, 144:284-305.
-
Menezes AM, Perez-Padilla R, Jardim JR, Muino A, Lopez MV, Valdivia G, et al. Chronic obstructive pulmonary disease in five Latin American cities (the PLATINO study): a prevalence study. Lancet. 2005;366:1875–81.
-
Buist AS, McBurnie MA, Vollmer WM, Gillespie S, Burney P, Mannino DM, et al. International variation in the prevalence of COPD (the BOLD Study): a population-based prevalence study. Lancet. 2007;370:741–50.
-
Fukuchi Y, Nishimura M, Ichinose M, Adachi M, Nagai A, Kuriyama T, et al. COPD in Japan: the Nippon COPD Epidemiology study. Respirology. 2004;9:458–65.
-
Lopez AD, Shibuya K, Rao C, Mathers CD, Hansell AL, Held LS, et al. Chronic obstructive pulmonary disease: current burden and future projections. Eur Respir J. 2006;27:397–412.
-
Hogg JC: Pathophysiology of airflow limitation in chronic obstructive pulmonary disease.Lancet 2004, 364:709-721.
-
Hogg JC, Chu F, Utokaparch S, Woods R, Elliott WM, Buzatu L, et al. The nature of small-airway obstruction in chronic obstructive pulmonary disease. N Engl J Med. 2004;350:2645–53.
-
O'Donnell DE, Webb KA: Exertional breathlessness in patients with chronic airflow limitation. The role of lung hyperinflation.Am Rev Respir Dis 1993, 148:1351-1357.
-
O'Donnell DE, Revill SM, Webb KA: Dynamic hyperinflation and exercise intolerance in chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2001, 164:770-777.
-
Hogg JC, Macklem PT, Thurlbeck WM: Site and nature of airway obstruction in chronic obstructive lung disease.N Engl J Med 1968, 278:1355-1360.
-
McDonough JE, Yuan R, Suzuki M, Seyednejad N, Elliott WM, Sanchez PG, et al. Small-airway obstruction and emphysema in chronic obstructive pulmonary disease. New Engl J Med. 2011;365:1567–75.
-
Lai H, Rogers DF: New pharmacotherapy for airway mucus hypersecretion in asthma and COPD: targeting intracellular signaling pathways.J Aerosol Med Pulm Drug Deliv 2010, 23:219-231.
-
Braido F, Baiardini I, Scichilone N, Sorino C, Di Marco F, Corsico A, et al. Disability in moderate chronic obstructive pulmonary disease: prevalence, burden and assessment - results from a real-life study. Respiration. 2015;89:100–6.
-
Barnes PJ, Celli BR: Systemic manifestations and comorbidities of COPD.Eur Respir J 2009, 33:1165-1185.
-
Agusti AG, Noguera A, Sauleda J, Sala E, Pons J, Busquets X: Systemic effects of chronic obstructive pulmonary disease.Eur Respir J 2003, 21:347-360.
-
Soriano JB, Visick GT, Muellerova H, Payvandi N, Hansell AL: Patterns of comorbidities in newly diagnosed COPD and asthma in primary care.Chest 2005, 128:2099-2107.
-
Belman MJ, Botnick WC, Shin JW: Inhaled bronchodilators reduce dynamic hyperinflation during exercise in patients with chronic obstructive pulmonary disease.Am J Respir Crit Care Med 1996, 153:967-975.
-
Santus P, Radovanovic D, Henchi S, Di Marco F, Centanni S, D'Angelo E, et al. Assessment of acute bronchodilator effects from specific airway resistance changes in stable COPD patients. Respir Physiol Neurobiol. 2014;197:36–45.
-
Scichilone N, Benfante A, Bocchino M, Braido F, Paggiaro P, Papi A, et al. Which factors affect the choice of the inhaler in chronic obstructive respiratory diseases? Pulm Pharmacol Ther. 2015;31:63–7.
-
Johnson M: The beta-adrenoceptor.Am J Respir Crit Care Med 1998, 158:S146-153.
-
Roux E, Molimard M, Savineau JP, Marthan R: Muscarinic stimulation of airway smooth muscle cells.Gen Pharmacol 1998, 31:349-356.
-
Essayan DM: Cyclic nucleotide phosphodiesterases.The Journal of allergy and clinical immunology 2001, 108:671-680.
-
Ofir D, Laveneziana P, Webb KA, Lam YM, O'Donnell DE: Mechanisms of dyspnea during cycle exercise in symptomatic patients with GOLD stage I chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2008, 177:622-629.
-
O'Donnell DE, Laveneziana P, Ora J, Webb KA, Lam YM, Ofir D: Evaluation of acute bronchodilator reversibility in patients with symptoms of GOLD stage I COPD.Thorax 2009, 64:216-223.
-
Bone R, Boyars M, Braun SR, Buist S, Campbell S, Chick T, et al. In chronic obstructive pulmonary disease, a combination of ipratropium and albuterol is more effective than either agent alone. An 85-day multicenter trial. COMBIVENT Inhalation Aerosol Study Group. Chest 1994, 105:1411–1419.
-
Vogelmeier C, Banerji D: NVA237, a long-acting muscarinic antagonist, as an emerging therapy for chronic obstructive pulmonary disease.Ther adv Respir Dis 2011, 5:163-173.
-
Gavalda A, Miralpeix M, Ramos I, Otal R, Carreno C, Vinals M, et al. Characterization of aclidinium bromide, a novel inhaled muscarinic antagonist, with long duration of action and a favorable pharmacological profile. J Pharmacol Exp Ther. 2009;331:740–51.
-
Gross NJ: Tiotropium bromide.Chest 2004, 126:1946-1953.
-
Casaburi R, Mahler DA, Jones PW, Wanner A, San PG, ZuWallack RL, et al. A long-term evaluation of once-daily inhaled tiotropium in chronic obstructive pulmonary disease. Eur Respir J. 2002;19:217–24.
-
Donohue JF, van Noord JA, Bateman ED, Langley SJ, Lee A, Witek Jr TJ, et al. A 6-month, placebo-controlled study comparing lung function and health status changes in COPD patients treated with tiotropium or salmeterol. Chest. 2002;122:47–55.
-
Dusser D, Bravo ML, Iacono P: The effect of tiotropium on exacerbations and airflow in patients with COPD.Eur Respir J 2006, 27:547-555.
-
Niewoehner DE, Rice K, Cote C, Paulson D, Cooper Jr JA, Korducki L, et al. Prevention of exacerbations of chronic obstructive pulmonary disease with tiotropium, a once-daily inhaled anticholinergic bronchodilator: a randomized trial. Ann Intern Med. 2005;143:317–26.
-
van Noord JA, Bantje TA, Eland ME, Korducki L, Cornelissen PJ: A randomised controlled comparison of tiotropium nd ipratropium in the treatment of chronic obstructive pulmonary disease.The Dutch Tiotropium Study Group. Thorax 2000, 55:289-294
-
Vincken W, van Noord JA, Greefhorst AP, Bantje TA, Kesten S, Korducki L, et al. Improved health outcomes in patients with COPD during 1 yr's treatment with tiotropium. Eur Respir J. 2002;19:209–16.
-
Vogelmeier C, Hederer B, Glaab T, Schmidt H, Rutten-van Molken MP, Beeh KM, et al. Tiotropium versus salmeterol for the prevention of exacerbations of COPD. N Engl J Med. 2011;364:1093–103.
-
Decramer M, Celli B, Kesten S, Lystig T, Mehra S, Tashkin DP: Effect of tiotropium on outcomes in patients with moderate chronic obstructive pulmonary disease (UPLIFT): a prespecified subgroup analysis of a randomised controlled trial.Lancet 2009, 374:1171-1178.
-
Troosters T, Celli B, Lystig T, Kesten S, Mehra S, Tashkin DP, et al. Tiotropium as a first maintenance drug in COPD: secondary analysis of the UPLIFT trial. Eur Respir J. 2010;36:65–73.
-
Tashkin DP, Celli BR, Decramer M, Lystig T, Liu D, Kesten S: Efficacy of tiotropium in COPD patients with FEV1 >/= 60 % participating in the UPLIFT(R) trial.COPD 2012, 9:289-296.
-
Singh S, Loke YK, Enright PL, Furberg CD: Mortality associated with tiotropium mist inhaler in patients with chronic obstructive pulmonary disease: systematic review and meta-analysis of randomised controlled trials.BMJ 2011, 342:d3215.
-
Dong YH, Lin HH, Shau WY, Wu YC, Chang CH, Lai MS: Comparative safety of inhaled medications in patients with chronic obstructive pulmonary disease: systematic review and mixed treatment comparison meta-analysis of randomised controlled trials.Thorax 2013, 68:48-56.
-
Tashkin DP, Celli B, Senn S, Burkhart D, Kesten S, Menjoge S, et al. A 4-year trial of tiotropium in chronic obstructive pulmonary disease. N Engl J Med. 2008;359:1543–54.
-
Wise RA, Anzueto A, Cotton D, Dahl R, Devins T, Disse B, et al. Tiotropium Respimat inhaler and the risk of death in COPD. N Engl J Med. 2013;369:1491–501.
-
D'Urzo A, Ferguson GT, van Noord JA, Hirata K, Martin C, Horton R, et al. Efficacy and safety of once-daily NVA237 in patients with moderate-to-severe COPD: the GLOW1 trial. Respir Res. 2011;12:156.
-
Kerwin E, Hebert J, Gallagher N, Martin C, Overend T, Alagappan VK, et al. Efficacy and safety of NVA237 versus placebo and tiotropium in patients with COPD: the GLOW2 study. Eur Respir J. 2012;40:1106–14.
-
Jones PW, Singh D, Bateman ED, Agusti A, Lamarca R, de Miquel G, et al. Efficacy and safety of twice-daily aclidinium bromide in COPD patients: the ATTAIN study. Eur Respir J. 2012;40:830–6.
-
Kerwin EM, D'Urzo AD, Gelb AF, Lakkis H, Garcia Gil E, Caracta CF: Efficacy and safety of a 12-week treatment with twice-daily aclidinium bromide in COPD patients (ACCORD COPD I).COPD 2012, 9:90-101.
-
Decramer M, Maltais F, Feldman G, Brooks J, Harris S, Mehta R, et al. Bronchodilation of umeclidinium, a new long-acting muscarinic antagonist, in COPD patients. Respir Physiol Neurobiol. 2013;185:393–9.
-
Mahler DA, Donohue JF, Barbee RA, Goldman MD, Gross NJ, Wisniewski ME, et al. Efficacy of salmeterol xinafoate in the treatment of COPD. Chest. 1999;115:957–65.
-
Rennard SI, Anderson W, ZuWallack R, Broughton J, Bailey W, Friedman M, et al. Use of a long-acting inhaled beta2-adrenergic agonist, salmeterol xinafoate, in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2001;163:1087–92.
-
Calverley PM, Anderson JA, Celli B, Ferguson GT, Jenkins C, Jones PW, et al. Salmeterol and fluticasone propionate and survival in chronic obstructive pulmonary disease. N Engl J Med. 2007;356:775–89.
-
Dahl R, Greefhorst LA, Nowak D, Nonikov V, Byrne AM, Thomson MH, et al. Inhaled formoterol dry powder versus ipratropium bromide in chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2001;164:778–84.
-
Lombardi D, Cuenoud B, Kramer SD: Lipid membrane interactions of indacaterol and salmeterol: do they influence their pharmacological properties?Eur J Pharm Sci 2009, 38:533-547.
-
Dahl R, Chung KF, Buhl R, Magnussen H, Nonikov V, Jack D, et al. Efficacy of a new once-daily long-acting inhaled beta2-agonist indacaterol versus twice-daily formoterol in COPD. Thorax. 2010;65:473–9.
-
Donohue JF, Fogarty C, Lotvall J, Mahler DA, Worth H, Yorgancioglu A, et al. Once-daily bronchodilators for chronic obstructive pulmonary disease: indacaterol versus tiotropium. Am J Respir Crit Care Med. 2010;182:155–62.
-
Kornmann O, Dahl R, Centanni S, Dogra A, Owen R, Lassen C, et al. Once-daily indacaterol versus twice-daily salmeterol for COPD: a placebo-controlled comparison. Eur Respir J. 2011;37:273–9.
-
Koch A, Pizzichini E, Hamilton A, Hart L, Korducki L, De Salvo MC, et al. Lung function efficacy and symptomatic benefit of olodaterol once daily delivered via Respimat(R) versus placebo and formoterol twice daily in patients with GOLD 2–4 COPD: results from two replicate 48-week studies. Int J Chron Obstruct Pulmon Dis. 2014;9:697–714.
-
ZuWallack R, Allen L, Hernandez G, Ting N, Abrahams R: Efficacy and safety of combining olodaterol Respimat((R)) and tiotropium HandiHaler((R)) in patients with COPD: results of two randomized, double-blind, active-controlled studies.Int J Chron Obstruct Pulmon Dis 2014, 9:1133-1144.
-
Ferguson GT, Feldman GJ, Hofbauer P, Hamilton A, Allen L, Korducki L, et al. Efficacy and safety of olodaterol once daily delivered via Respimat(R) in patients with GOLD 2–4 COPD: results from two replicate 48-week studies. Int J Chron Obstruct Pulmon Dis. 2014;9:629–45.
-
Buhl R, Dunn LJ, Disdier C, Lassen C, Amos C, Henley M, et al. Blinded 12-week comparison of once-daily indacaterol and tiotropium in COPD. Eur Respir J. 2011;38:797–803.
-
Decramer ML, Chapman KR, Dahl R, Frith P, Devouassoux G, Fritscher C, et al. Once-daily indacaterol versus tiotropium for patients with severe chronic obstructive pulmonary disease (INVIGORATE): a randomised, blinded, parallel-group study. The Lancet Respiratory medicine. 2013;1:524–33.
-
Karner C, Cates CJ: Long-acting beta(2)-agonist in addition to tiotropium versus either tiotropium or long-acting beta(2)-agonist alone for chronic obstructive pulmonary disease.Cochrane Database Syst Rev 2012., 4Article ID CD008989
-
Celli B, Crater G, Kilbride S, Mehta R, Tabberer M, Kalberg CJ, et al. Once-daily umeclidinium/vilanterol 125/25 mcg in COPD: a randomized, controlled study. Chest. 2014.
-
Donohue JF, Maleki-Yazdi MR, Kilbride S, Mehta R, Kalberg C, Church A: Efficacy and safety of once-daily umeclidinium/vilanterol 62.5/25 mcg in COPD.Respir Med 2013, 107:1538-1546.
-
Donohue JF, Niewoehner D, Brooks J, O'Dell D, Church A. Safety and tolerability of once-daily umeclidinium/vilanterol 125/25 mcg and umeclidinium 125 mcg in patients with chronic obstructive pulmonary disease: results from a 52-week, randomized, double-blind, placebo-controlled study. Respir Res. 2014;15:78.
-
Maleki-Yazdi MR, Kaelin T, Richard N, Zvarich M, Church A: Efficacy and safety of umeclidinium/vilanterol 62.5/25 mcg and tiotropium 18 mcg in chronic obstructive pulmonary disease: results of a 24-week, randomized, controlled trial.Respir Med 2014, 108:1752-1760.
-
Rodrigo GJ, Plaza V: Efficacy and safety of indacaterol and Glycopyrronium in COPD: an update.Chest 2014., 146Article ID e75
-
Rodrigo GJ, Plaza V: Efficacy and safety of a fixed-dose combination of indacaterol and Glycopyrronium for the treatment of COPD: a systematic review.Chest 2014, 146:309-317.
-
Vincken W, Aumann J, Chen H, Henley M, McBryan D, Goyal P: Efficacy and safety of coadministration of once-daily indacaterol and glycopyrronium versus indacaterol alone in COPD patients: the GLOW6 study.Int J Chron Obstruct Pulmon Dis 2014, 9:215-228.
-
Barnes PJ: Theophylline for COPD.Thorax 2006, 61:742-744.
-
Culpitt SV, de Matos C, Russell RE, Donnelly LE, Rogers DF, Barnes PJ: Effect of theophylline on induced sputum inflammatory indices and neutrophil chemotaxis in chronic obstructive pulmonary disease.Am J Respir Crit Care Med 2002, 165:1371-1376.
-
Hirano T, Yamagata T, Gohda M, Yamagata Y, Ichikawa T, Yanagisawa S, et al. Inhibition of reactive nitrogen species production in COPD airways: comparison of inhaled corticosteroid and oral theophylline. Thorax. 2006;61:761–6.
-
Kobayashi M, Nasuhara Y, Betsuyaku T, Shibuya E, Tanino Y, Tanino M, et al. Effect of low-dose theophylline on airway inflammation in COPD. Respirology. 2004;9:249–54.
-
Ito K, Lim S, Caramori G, Cosio B, Chung KF, Adcock IM, et al. A molecular mechanism of action of theophylline: Induction of histone deacetylase activity to decrease inflammatory gene expression. Proc Nat Acad Sci U S A. 2002;99:8921–6.
-
Ito K, Ito M, Elliott WM, Cosio B, Caramori G, Kon OM, et al. Decreased histone deacetylase activity in chronic obstructive pulmonary disease. N Engl J Med. 2005;352:1967–76.
-
Cosio BG, Tsaprouni L, Ito K, Jazrawi E, Adcock IM, Barnes PJ: Theophylline restores histone deacetylase activity and steroid responses in COPD macrophages.J Exp Med 2004, 200:689-695.
-
Ito K, Yamamura S, Essilfie-Quaye S, Cosio B, Ito M, Barnes PJ, et al. Histone deacetylase 2-mediated deacetylation of the glucocorticoid receptor enables NF-kappaB suppression. J Exp Med. 2006;203:7–13.
-
Celli BR, Thomas NE, Anderson JA, Ferguson GT, Jenkins CR, Jones PW, et al. Effect of pharmacotherapy on rate of decline of lung function in chronic obstructive pulmonary disease: results from the TORCH study. Am J Respir Crit Care Med. 2008;178:332–8.
-
Miravitlles M, Soler-Cataluna JJ, Calle M, Soriano JB: Treatment of COPD by clinical phenotypes: putting old evidence into clinical practice.Eur Respir J 2013, 41:1252-1256.
-
Bettoncelli G, Blasi F, Brusasco V, Centanni S, Corrado A, De Benedetto F, De Michele F, Di Maria GU, Donner CF, Falcone F, et al.: The clinical and integrated management of COPD. An official document of AIMAR (Interdisciplinary Association for Research in Lung Disease), AIPO (Italian Association of Hospital Pulmonologists), SIMER (Italian Society of Respiratory Medicine), SIMG (Italian Society of General Medicine). Multidisciplinary respiratory medicine 2014, 9:25.
-
Wedzicha JA, Calverley PM, Seemungal TA, Hagan G, Ansari Z, Stockley RA: The prevention of chronic obstructive pulmonary disease exacerbations by salmeterol/fluticasone propionate or tiotropium bromide.Am J Respir Crit Care Med. 2008, 177:19-26.
-
Calverley PM, Stockley RA, Seemungal TA, Hagan G, Willits LR, Riley JH, et al. Reported pneumonia in patients with COPD: findings from the INSPIRE study. Chest. 2011;139:505–12.
-
Fukuchi Y, Samoro R, Fassakhov R, Taniguchi H, Ekelund J, Carlsson LG, et al. Budesonide/formoterol via Turbuhaler(R) versus formoterol via Turbuhaler(R) in patients with moderate to severe chronic obstructive pulmonary disease: phase III multinational study results. Respirology. 2013;18:866–73.
-
Larsson K, Janson C, Lisspers K, Jorgensen L, Stratelis G, Telg G, et al. Combination of budesonide/formoterol more effective than fluticasone/salmeterol in preventing exacerbations in chronic obstructive pulmonary disease: the PATHOS study. J Intern Med. 2013;273:584–94.
-
Martinez FJ, Boscia J, Feldman G, Scott-Wilson C, Kilbride S, Fabbri L, et al. Fluticasone furoate/vilanterol (100/25; 200/25 mug) improves lung function in COPD: a randomised trial. Respir Med. 2013;107:550–9.
-
Magnussen H, Disse B, Rodriguez-Roisin R, Kirsten A, Watz H, Tetzlaff K, et al. Withdrawal of inhaled glucocorticoids and exacerbations of COPD. N Engl J Med. 2014;371:1285–94.
-
Spina D: PDE4 inhibitors: current status.Br J Pharmacol 2008, 155:308-315.
-
Calverley PM, Rabe KF, Goehring UM, Kristiansen S, Fabbri LM, Martinez FJ: Roflumilast in symptomatic chronic obstructive pulmonary disease: two randomised clinical trials.Lancet 2009, 374:685-694.
-
Fabbri LM, Calverley PM, Izquierdo-Alonso JL, Bundschuh DS, Brose M, Martinez FJ, et al. Roflumilast in moderate-to-severe chronic obstructive pulmonary disease treated with longacting bronchodilators: two randomised clinical trials. Lancet. 2009;374:695–703.
-
Chong J, Poole P, Leung B, Black PN: Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease. Cochrane Database Syst Rev. 2011. doi:10.1002/14651858.CD002309.pub3.
-
Barnes PJ: New anti-inflammatory targets for chronic obstructive pulmonary disease.Nature reviews Drug discovery 2013, 12:543-559.
-
Martinez FJ, Donohue JF, Rennard SI: The future of chronic obstructive pulmonary disease treatment--difficulties of and barriers to drug development.Lancet 2011, 378:1027-1037.

