Никотин

Колумб не только Америку открыл
Никотин — одно из веществ, обладающих биологической активностью, содержащихся в растениях, в основном в табаке и в меньших концентрациях в некоторых других растениях. Первые упоминания о свойствах табака относятся ко временам открытия Америки, ещё Христофор Колумб отметил, что индейцы курят свернутые высушенные листья некого растения, к которому относятся особенно, используя его для шаманских обрядов и некоторых других важных мероприятий. Во время второй поездки в Новый Свет (1493) Колумба сопровождал испанский миссионер Фрэй Романо Пане и, познакомившись с табаком, немедленно отослал его Карлу V, после чего тот приказал выращивать его на Кубе. В Европе табачные семена впервые появились в 1520 году, после чего его стали выращивать также в Португалии. Примерно в 1560 году послом из Франции в Португалию был Жан Нико, он послал листочки табака Екатерине Медичи, королеве Франции. Табак был описан королеве как «растение, которое способно облегчить ужасные мигрени». Табак стал называться «травой королевы» и интенсивно употреблялся при королевском дворце, после чего распространился на всю Европу. Сам никотин в неочищенном виде был описан Жаком Гоори как «масло табака», использовавшееся для лечения кожных заболеваний (1579); детально описал метод получения никотина путём перегонки Николя Лефевр (1660). Полученный им продукт использовали для лечения астмы, эпилепсии, воспаления селезенки. В 1809 году французский химик-аналитик Луи Николя Воклен опубликовал работу, в ходе которой он смог выделить довольно чистую фракцию никотина, связанного с яблочной кислотой, а также смог их разделить, однако многие оспаривают его роль первооткрывателя в связи с тем, что он не определил никотин как алкалоид. В 1828 году немецкие химики Кристиан Вильгельм Посселт и Карл Людвиг Райманн открыли активное начало табака и установили, что он является алкалоидом, правда, долго велись споры о достоверности этого открытия, так как многие другие исследователи не верили, что алкалоид может быть жидкостью, но Кристиан и Карл с помощью созыва независимой комиссии доказали свою точку зрения, и именно они считаются в народе первооткрывателями никотина как такового. В 1843 году Луи Мельсеном была эмпирически выведена формула никотина. 1893 году собственно структура была установлена немецким химиком Адольфом Пиннером, но и тут не обошлось без разногласий: для подтверждения структуры требовался синтез данного вещества, чего Адольфу не довелось реализовать. Тем не менее, синтез был реализован Аме Пикте в 1904 году. В своих статьях он упомянул не только никотин, но и продукты его окисления: никотирин и дигидроникотирин. Правда, часть реакций проходила в жестких условиях, что снова породило много сомнений, но последующий (1928) синтез, проведённый в мягких условиях, подтвердил правильность установленной формулы.
#ЛошадьЖиви
Таким образом, не без труда было установлено, что никотин, алкалоид растительного происхождения, как и все алкалоиды — высокоактивное вещество и, как любой из них в высокой концентрации, способен вызвать много нежелательных последствий. В низких же концентрациях многие алкалоиды эффективно используются в медицинских целях. Чтобы понять, как «капля никотина убивает лошадь»[1] (или все-таки нет?), стоит разобраться в механизме его взаимодействия с организмом.
Кто есть кто
Основной нейромедиатор, являющийся посредником передачи нервных импульсов, например, в парасимпатической нервной системе и нервно-мышечных синапсах — ацетилхолин. Накапливаясь в цитоплазме аксонов в виде везикул, он, высвобождаясь при стимуляции преганглионарного нейрона, изливается в синаптическую щель, где взаимодействует с рецептором на мембране постганглионарного нейрона, вызывая биологический ответ, который может выражаться в замедлении сердечных сокращений, расширении периферических кровеносных сосудов и понижении артериального давления, усилении перистальтики желудка и кишечника, сокращении мускулатуры бронхов, матки, желчного и мочевого пузыря, усилении секреции пищеварительных, бронхиальных, потовых и слёзных желез, сужении зрачков. Но это не все! Ацетилхолин является медиатором и в симпатической нервной системе, в ней он является медиатором в преганглионарных нейронах (в то время как постганглионарным является норадреналин), а значит, он вызывает и все ответы, характерные для действия симпатики: учащение сердцебиения, повышение давления, увеличение уровня глюкозы в крови и интенсивности липолиза (распада жиров), плюс, угнетение центров голода (этим обосновывается мнение о том, что от курения худеют). Все это вызывается в первую очередь действием симпатической нервной системы на надпочечники, что вызывает выброс адреналина, который и повинен во всех «бодрящих» эффектах.Рецепторы же к нему делят на 2 больших класса: Мускариновые (М-холинорецепторы, mAChR) и Никотиновые (N-холинорецепторы, nAChR). Названы они в честь своих агонистов (веществ, способных взаимодействовать с рецептором, вызывая биологический ответ): мускарина, выделенного из мухоморов, и никотина, соответственно. В данном случае нас интересует второй рецептор.Никотин имеет схожую с ацетилхолином структуру и действует на рецепторы последнего:
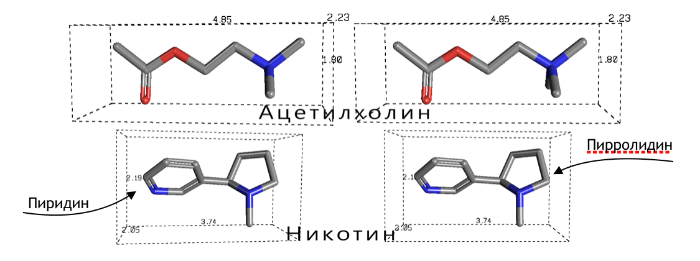
Атом азота пирролидинового (5-членного гетероцикла) кольца в никотине (выделен синим) имитирует четвертичный атом азота в ацетилхолине (выделен красным), а атом азота пиридина (6-членного гетероцикла) является донором электронных пар, как и кислород кетогруппы ацетилхолина (выделены красным). Внешне они, может быть, и не очень похожи, но тут важнее функционал: пространственное распределение электронной плотности обеспечивает практически одинаковый характер связи с рецептором и вызывает аналогичный биологический ответ. Теперь, выяснив, какие эффекты влечёт за собой связывание ацетилхолина (и его функционального «двойника») с рецептором, перейдём к более подробному рассмотрению механизма этих хитрых взаимодействий.
А ларчик просто открывался
В активном центре рецептора к ацетилхолину никотинового типа содержится несколько петель, главная из которых — С-петля, содержащая триптофан. Триптофан, в свою очередь, является ароматической аминокислотой. Он обладает большим отрицательным зарядом, благодаря, во-первых, избытку электронной плотности (половина связей — двойные), во-вторых, циклической структуре. Дело в том, что в этой циклической структуре двойные связи являются «делокализованными», то есть некорректно говорить, что они находятся у 1, 3, 5 атомов углерода или у 2, 4, 6 — они как бы «размазаны» по шестичленному кольцу, к тому же, эти двойные (π) связи имеют электронную плотность в виде объёмной восьмерки, поставленной перпендикулярно плоскости кольца, так что избыточная электронная плотность висит даже не одним колесом, а двумя — над и под плоскостью кольца!
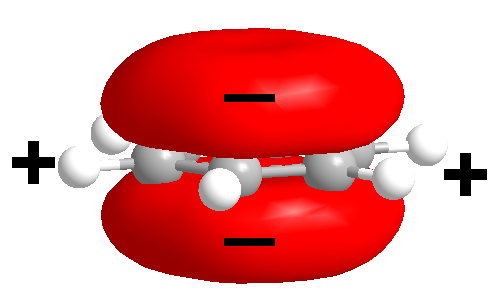
Ароматическое кольцо
Само понятие «избыток электронной плотности» означает, что в этом участке пространства скапливается избыточный отрицательный заряд, попросту — минус. Выше было упомянуто, что атом азота в никотине имеет недостаток электронной плотности, то бишь, плюс. А дальше действуют базовые законы физики: подчиняясь закону Кулона, плюс тянется к минусу и входит в кольцо, как ключ в замок, причём двойной, застревая между отрицательно заряженными «прокладками»! А после этого он оттуда не хочет выходить, следуя принципу минимума энергии, а минимум как раз достигается внутри «минусового кольца».
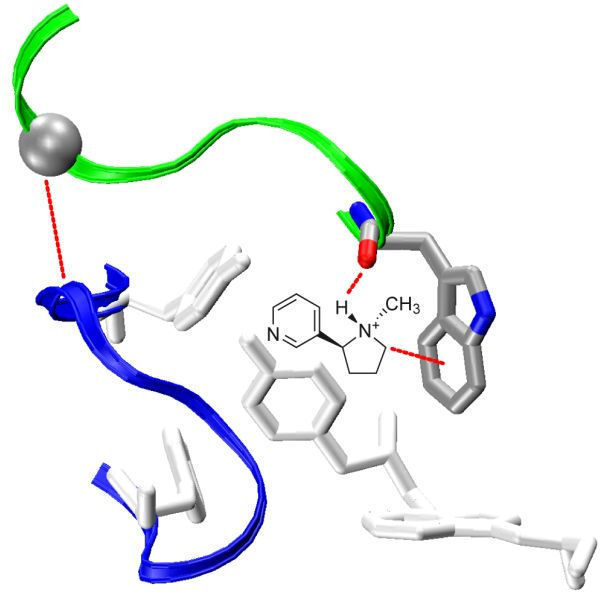
C-петля и никотин
Это взаимодействие является необычайно сильным, связь крайне прочной, настолько, что превосходит ковалентные взаимодействия и имеет собственное название: катион-π связь[2]. К тому же, между углеродным скелетом триптофана пресловутой С-петли и азотом ароматического кольца никотина образуется водородная связь. Да, она не очень прочная, но, в дополнение к крепкой π-связи, она дополнительно стабилизирует её пространственно, и именно таким образом эта связь оказывается «железной».
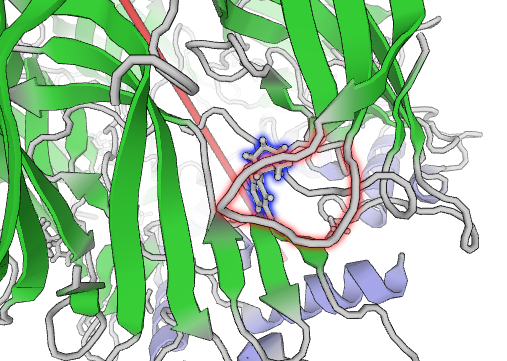
Рецептор с никотином
От слов к делу
Теперь о том, к чему вообще были рассмотрены все эти супрамолекулярные механизмы: от связывания к биологическому ответу.
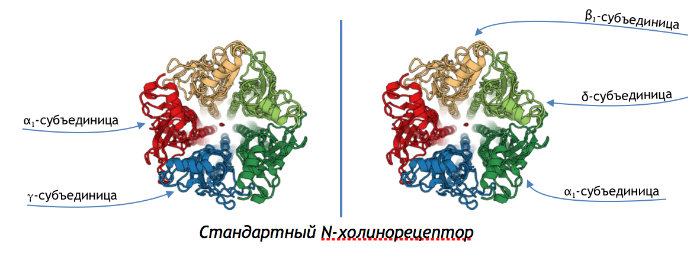
Ацетилхолиновый рецептор по сути своей является трансмембранной белковой порой, состоящей из 5 доменов, причём 2 самых распространённых типа: α3β2 и α2β3 (α и β — названия разных доменов). И есть исследование, показывающее, что α2β3 более чувствителен к никотину[2], и при постоянном поступлении никотина экспрессия этого рецептора возрастает, но зато со временем чувствительность снижается. Так вот, при связывании того или иного агониста конформация белка меняется, пора открывается, и натрий, сосредоточенный в основном во внеклеточном пространстве, бросается в открывшуюся пору, меняя заряд клетки (катионы натрия создавали положительный заряд вне клетки, на её поверхности, относительно отрицательного внутри неё). Этот процесс называется деполяризацией. Собственно, это и есть нервный импульс со всеми вытекающими событиями: либо деполяризуется следующий нейрон, либо вызывается сокращение мышцы, деятельность железы, в ЦНС — когнитивные процессы и великое множество иных процессов, которые запускаются действием ацетилхолина, либо какого-то агониста. Следует упомянуть о том, что на скелетные мышцы никотин не оказывает сколь-либо заметного действия — пара аминокислот в белке рецептора там заменена другой, не образуется стабилизирующая водородная связь (несмотря на то, что катион-π связь так же образуется, но она слабее, чем в нейрональных рецепторах, так как не стабилизирована водородной). Центральное действие (то есть на головной мозг) никотина обосновано активацией им α4β2 рецепторов мозга. Этот рецептор имеет настолько высокое сродство к никотину, что даже ацетилхолин в высокой дозе не способен стать последнему конкурентом в данном случае. Таких рецепторов в мозге на долю всех Н-холинорецепторов приходится более 80 %. А, значит, центральное действие никотина самое заметное. И это настолько же положительная, насколько и отрицательная новость для медицины. А дело вот в чем. Никотиновые рецепторы данного типа, имеющие преимущественно пресинаптическую локализацию, участвуют в выбросе большого спектра медиаторов: например, глутамата, дофамина и ГАМК (γ-аминомасляной кислоты). А, значит, никотин, эффективно активируя эти рецепторы, стимулирует другие типы взаимодействий, что во многих случаях положительно влияет на те или иные мозговые процессы (например, запоминание). В добавок к этому существуют механизмы активации экспрессии (синтеза) никотиновых ацетилхолиновых рецепторов, связанных с взаимодействием никотина с рецептором. Чем больше никотина — тем больше экспрессия. И здесь становится абсолютно неважно, имеют ли эти рецепторы достаточную чувствительность, потому что сам высокий уровень экспрессии приводит к активному метаболизму клеток, что отсрочивает их апоптоз. И эта мысль натолкнула исследователей на идею профилактики болезни Альцгеймера и других дегенеративных заболеваний мозга с помощью никотина [9]. И исследования таки продемонстрировали очень интересную статистику. Среди пациентов с болезнью Альцгеймера не более 26 % курящих, из которых более половины начали курить позже 30 лет[10].
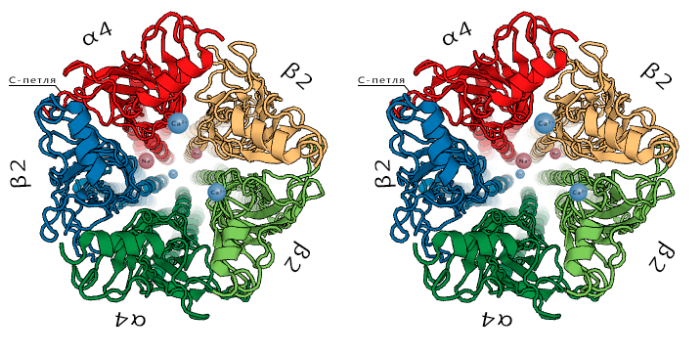
Что происходит с лигандом дальше? Он не остаётся там надолго в макроскопическом понимании времени; то, что эта связь крепкая и долгая, значит, что она долгая по сравнению со средним временем жизни молекулы. После того, как молекула никотина сделала своё дело, она «вымывается» из рецептора, затем с током крови переносится в печень, где метаболизируется посредством цитохрома р450 (гидроксилированием) до своего «наследника» — котинина[3]
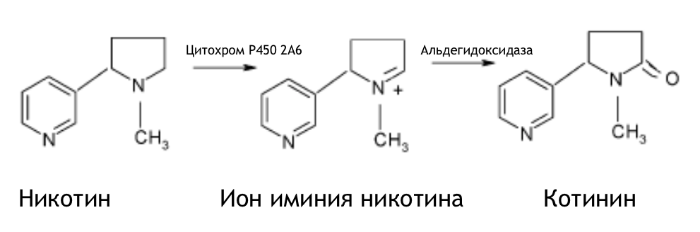
Схема метаболизма никотина
(анаграмма от слова «никотин»). В виде котинина выводится 70-80% никотина, 3-5% в виде гидроксиникотина, некоторое количество метаболизируется путём глюкуронирования и никотина, и котинина. Интересно, что котинин вызывает схожие с действием никотина эффекты, хотя и с меньшей интенсивностью: связывается с рецептором, активирует его, оказывая ноотропное, антидепрессантное и психостимулирующее действие. Ещё одна ощутимая разница между никотином и котинином в периодах полувыведения: половина никотина выводится из организма через 2 часа, а вот котинина — 20 часов, вследствие чего котинин является ценным маркёром активного потребления никотина.
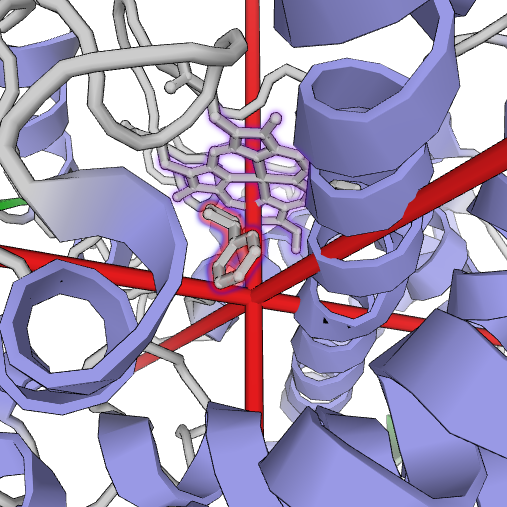
Цитохром P450 (лиловый — порфирин гема) и никотин (красно-фиолетовый)
Растениям тоже нужен никотин
Зачем же никотин вообще образуется в растениях? Дело в том, что на синтез такого сложного алкалоида, как никотин, тратится около 10% всей энергии, запасенной в результате фотосинтеза[8]. Такая трата вполне оправдана, так как транспортируясь в листья, алкалоид делает их несъедобными для колорадского жука. У ближайшего «родственника» табака, картофеля, тоже вырабатывается никотин, но его оказывается так мало, что эффективность практически нулевая, и в данном случае траты напрасны. Синтезируется никотин в растениях в пути от орнитина или пролина и никотиновой кислоты. Все эти соединения встречаются в единой системе реакций.
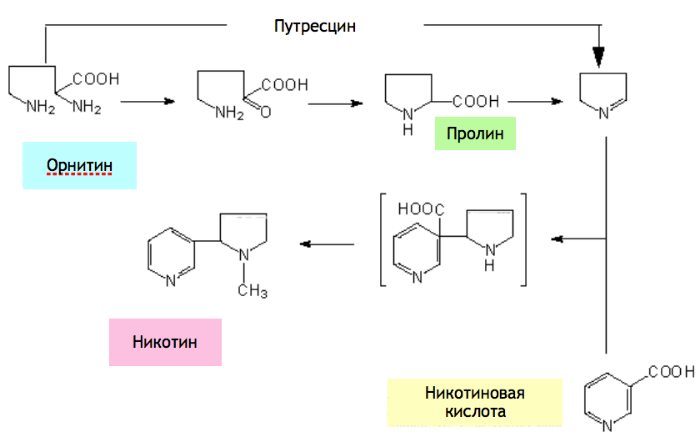
Схема синтеза никотина
О других тараканах
Никотин проявляет противовоспалительные свойства, действуя в качестве холинергического агониста[5], активируя α7 никотиновый ацетилхолиновый рецептор (α7nAChR) на иммунных клетках, в частности, дендритных клетках и макрофагах. Очевидно, что активация никотинового рецептора при помощи либо самого никотина, либо нейромедиатора ацетилхолина может подавлять воспалительные реакции на иммунных клетках и снижать секрецию провоспалительных цитокинов.Никотин и его метаболит котинин отрицательно воздействуют на структуру семенников и циркулирующие уровни тестостерона[6].Было показано, что никотин способен активировать mTOR при инкубировании его в культуру скелетных мышц, из-за чего снижается чувствительность к инсулину[7].
Заключение
Можно было бы еще долго и много говорить о свойствах никотина, как положительных, так и отрицательных. Есть несколько трудов о иммунных влияниях никотина, о влияниях на личность, на сознание и даже на плод. Но все эти темы плохо изучены и не вписываются в данный обзор. Есть данные о том, что никотин и котинин ингибируют ароматазу[4], что, по сути, является очень интересным свойством, которое может найти свое применение в дальнейших исследованиях, но это свойство не является классическим и исключительным, поэтому также не включено в обзор.
Источники:
- Kellogg J.H. «Tobaccoism» Am J Public Health. 2002 June; 92(6): 932–934.
- Zhong, W; Gallivan, JP; Zhang, Y; Li, L; Lester, HA; Dougherty, DA (1998). «From ab initio quantum mechanics to molecular neurobiology: A cation–π binding site in the nicotinic receptor». Proc. Natl. Acad. Sci. USA 95 (21): 12088–12093.
- Benowitz NL, Jacob P 3rd. «Metabolism of nicotine to cotinine studied by a dual stable isotope method. Clin Pharmacol Ther.» (1994)
- Doering IL, Richter E. «Inhibition of human aromatase by myosmine.» Drug Metab Lett. (2009)
- Lakhan SE, Kirchgessner A. «Anti-inflammatory effects of nicotine in obesity and ulcerative colitis.» J Transl Med. (2011)
- Aydos K, et al. «Nicotine toxicity to the ultrastructure of the testis in rats.» BJU Int. (2001)
- Tzatsos A. «Raptor binds the SAIN (Shc and IRS-1 NPXY binding) domain of insulin receptor substrate-1 (IRS-1) and regulates the phosphorylation of IRS-1 at Ser-636/639 by mTOR.» J Biol Chem. (2009)
- Семенов А.А. «Очерк химии природных соединений», Сибирская издательская фирма РАН (2000)
- Lombardo S., Maskos U. «Role of the nicotinic acetylcholine receptor in Alzheimer’s disease pathology and treatment.» J. Neuropharmocology. (2014)
- James Le Furo «Relationship between cigarette smoking and Alzheimer’s disease in a population‐based case‐control study.» The Times of London. (1993)
