BDNF: волшебный эликсир мозга
В 50-х годах прошлого столетия Рита Леви-Монтальчини и Виктор Хамбургер, проводя исследования, заметили, что нервные волокна цыплят растут быстрее, если рядом присутствуют опухолевые клетки мышей. На основании этого Леви-Монтальчини предположила, что в раковых клетках существует вещество, стимулирующее рост нервной ткани. Спустя некоторое время вместе со Стэнли Коэном, американским биохимиком, они выделили белок, которые назвали фактором роста нервов, или NGF (nerve growth factor). За это в 1986 году они оба были удостоены Нобелевской премии в области физиологии и медицины.
Исследования Риты Леви-Монтальчини способствовали открытию целого ряда подобных факторов роста нервов, одним из которых являлся нейротрофический фактор мозга, или BDNF (brain-derived neurotrophic factor). BDNF является нейротрофином, веществом, которое стимулирует и поддерживает жизнеспособность и развитие нейронов. «Волшебный эликсир мозга», так его называет Норман Дойдж в своей книге «Пластичность мозга».
Итак, давайте разберемся, что же это такое — нейротрофический фактор мозга.
Данный фактор кодируется геном BDNF. У человека он картирован на хромосоме 11p. Ген BDNF имеет четыре 5′ экзонов (экзоны I–IV) — участков ДНК, копии которых составляют зрелую РНК, которые связаны с различными промоутерами, — и один 3' экзон (экзон V), который кодирует зрелый белок BDNF.
Уже было описано множество факторов, которые изменяют экспрессию гена BDNF как при физиологическом, так и при патологическом состояниях. Например, световая стимуляция увеличивает мРНК BDNF в зрительной коре, осмотическая стимуляция увеличивает мРНК BDNF в гипоталамусе. Электрические стимулы, которые вызывают долгосрочное потенцирование в гиппокампе, клеточной модели обучения и памяти, увеличивают экспрессию BDNF и NGF. Было показано, что даже физические упражнения увеличивают экспрессию NGF и BDNF в гиппокампе. Интересно, что уровень BDNF варьирует в зависимости от эстрального цикла, который коррелирует с его воздействием на нервную возбудимость.
Сам нейротрофический фактор мозга является димером, состоящим из двух идентичных пептидных цепей, которые взаимодействуют друг с другом через нековалентные связи (рис. 1).

Рисунок 1 | Модель BDNF
Стабильный мономер BDNF до сих не был обнаружен ни внутри-, ни внеклеточно. Как всякий секретируемый белок, BDNF в виде предшественника белка (pre-pro-BDNF) выделяется в эндоплазматической сети. Этот предшественник ответственен за связывание мРНК BDNF с рибосомой эндоплазматической сети и транспорт белка-BDNF в эндоплазматическую сеть, и после поступления белка будет сразу же от него отщеплен. Т. е. таким образом pre-pro- BDNF переходит в pro-BDNF. Созданный pro-BDNF выходит из эндоплазматической сети через аппарат Гольджи к транссети-Гольджи, где далее преобразуется. Далее из транссети-Гольджи pro-BDNF транспортируется в секреторные гранулы, где он расщепляется прогормоном конвертаза 1 (PC1). В секреторных гранулах нейротрофический фактор мозга содержится уже либо в виде отдельных фрагментов BDNF, либо в виде зрелого mBDNF (рис. 2).
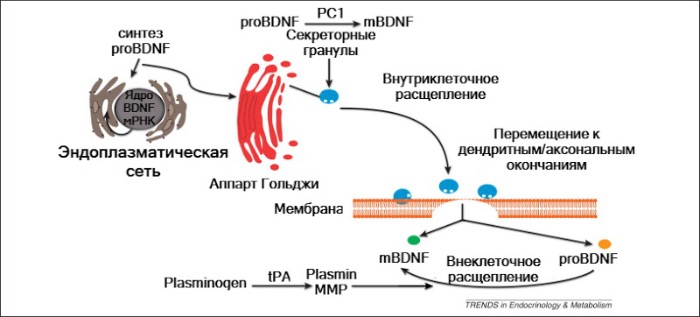
Рисунок 2 | Синтез BDNF
В нормальных физиологических условиях in vivo BDNF присутствует во многих частях головного мозга, но выражен достаточно слабо. В срезах головного мозга белок обнаруживается только с помощью вторичных антител, у которых ферментативно усиливают сигнал. С использованием этой методики эндогенный BDNF может быть обнаружен в теле, аксоне и дендритах глутаматергических нейронов. У взрослых крыс и мышей данный фактор находят в CA3 области гиппокампа, зрительной и соматосенсорной коре, или также в миндалине.
Иммуноцитохимические исследования флуоресцентными меченными вторичными антителами (без усиления сигнала) подтверждают особенно заметную аксональную локализацию эндогенного BDNF CA3 области гиппокампа.
При таких же экспериментальных условиях доказательство наличия эндогенного нейротрофического фактора в дендритах гиппокампа in vivo возможно только в отдельных случаях. Можно предположить, что уровень BDNF в этих структурах ниже предела обнаружения флуоресцентными антителами. Однако дендритная локализация мРНК данного фактора является явным признаком дендритного синтеза и дендритной локализации в пирамидных клетках гиппокампа и коры.
На поверхности клеток BDNF связывается по меньшей мере с двумя видами рецепторов: TrkB ( производное «Track B») and the LNGFR ( low-affinity nerve growth factor receptor, рецептор фактора роста нервов с низким сродством, также известный как p75). Он также может модулировать активность различных рецепторов нейротрансмиттеров, включая A7-никотиновых рецепторов.
Уже первые исследования BDNF показали, что он влияет на синаптическую передачу, увеличивая частоту маленьких возбуждающих постсинаптических токов. С тех пор изучению этого факта были посвящены многие исследования. В целом, BDNF усиливает действие возбуждающих глутаматергических синапсов и ослабляет ингибирующие ГАМК-ергические синапсы. Но до сих пор интенсивно обсуждается, чем вызвано это синаптическое потенцирование, вызванное BDNF: пресинаптическим действием (например, за счет высвобождения глутамата) или постсинаптическим (путем фосфорилирования рецепторов нейротрансмиттеров). Ряд исследований предоставил доказательства пресинаптического локуса, но также были получены доказательства и постсинаптических действий.
Почему же нейротрофический фактор мозга так важен для человека?
Уже во время нейрогенеза BDNF играет важную роль. Он способствует защите проводящих путей, повышая выживаемость клеток.
Но на этом его функция не заканчивается. BDNF играет одну из главных ролей, укрепляя изменения, происходящие с головным мозгом в критические периоды онтогенеза, т.е. те периоды, когда развивающийся организм наиболее чувствителен к воздействию внешних и внутренних факторов. По утверждению Michael M. Merzenich, профессора неврологии Калифорнийского университета в Сан-Франциско, это происходит четырьмя различными способами.
Выполнение какого-либо действия, которое требует одновременной активации определенных нейронов, приводит к выделению BDNF. С его помощью происходит укрепление связи между данными нейронами, что помогает их соединить вместе и обеспечивает их совместную активацию и в будущем. Также BDNF способствует образованию тонкой жировой оболочки вокруг каждого нейрона,что ускоряет передачу электрических сигналов.
Во время сенситивного периода данный фактор активирует базальное ядро, что позволяет нам фокусировать внимание и поддерживает его в активном состоянии в течение всего критического периода.
Последняя функция BDNF: он заканчивает укрепление ключевых связый и отключает базальное ядро.
Различные исследования показывают связь между BDNF и различными состояниями, такими как депрессия, шизофрения, обсессивно-компульсивное расстройство, болезнь Альцгеймера, болезнь Гентингтона, синдром Ретта, деменция, нервная анорексия и нервная булимия.
Было отмечено избирательное уменьшение мРНК BDNF в гиппокампе при болезни Альцгеймера. При болезни Паркинсона также обнаружили снижение уровня BDNF в черной субстанции.
Недавнее исследование показало роль BDNF и при болезни Гентингтона. Гентингтин, белок, мутирующий при данном заболевании, способствует транскрипции BDNF, и потеря гентингтин-индуцированной транскрипции BDNF приводит к потери трофической поддержки полосатых нейронов, что впоследствии перерастает в патологические признаки данного заболевания. Одно из последних исследований продемонстрировало, что гентингтин в норме ингибирует нейронный ограничивающий глушитель (the neuron restrictive silencer element), вовлеченный в тоническую репрессию транскрипции BDNF. То есть при нарушении функционирования гентингтина начинает действовать нейронный ограничивающий глушитель, и происходит репрессия транскрипции.
Если изменение уровня BDNF приводит к возникновению данных заболеваний, то в будущем будет возможно использование данного фактора мозга для их лечения. Нейротрофический фактор может также участвовать в формировании аффективного поведения. Окружающий человека стресс,такой как например низкая подвижность, индуцирует депрессию, а также снижает уровень мРНК BDNF. И наоборот, было замечено, что физические упражнения связаны с уменьшением депрессии и увеличением мРНК BDNF. Считается, что существующие методы лечения депрессии действуют главным образом за счет усиления эндогенной моноаминергической (то есть серотонинергической и норадренергической) синаптической передачи, а недавние исследования показали, что эффективные антидепрессанты увеличивают также мРНК и белок BDNF. Экзогенное поступление BDNF способствует прорастанию и функционированию серотонинергических нейронов у взрослых крыс, а у мышей с дефицитом-BDNF также снижена и серотонинергическая иннервация. Таким образом, новые фармакологические стратегии сосредоточены на потенциальной роли BDNF как антидепрессанта.
Также было выдвинуто предположение, что BDNF может участвовать в биполярном расстройстве. Интересен тот факт, что литий, основной препарат для лечения биполярного расстройства, увеличивает активацию BDNF и TrkB в церебральных кортикальных нейронах. Сейчас BDNF является хорошим кандидатом-геном для объяснения механизма предрасположенности к биполярному расстройству. Однако то, как изменение в активности BDNF может соотноситься с чередованием приступов мании и депрессии при биполярном расстройстве, все еще является предметом обсуждений.
В последние годы также активно исследуют возможную связь между BDNF и аутизмом.
Источники
- Binder D. K., Scharfman H. E. Mini review //Growth factors. – 2004. – Т. 22. – №. 3. – С. 123-131.
- Brigadski T., Lessmann V. BDNF: Ein Regulator von Lern-und Gedächtnisprozessen mit klinischem Potenzial //e-Neuroforum. – 2014. – Т. 20. – №. 1. – С. 166-177.
- Дойдж Н. Пластичность мозга. Потрясающие факты о том, как мысли способны менять структуру и функции нашего мозга. – Litres, 2018.
