Роль HSP-70 в снижении цитотоксичности бета-амилоида при болезни Альцгеймера
Болезнь Альцгеймера (БА) - заболевание, относящееся к дегенеративным болезням центральной нервной системы (МКБ-10) и связанное с изменением пространственной структуры белков. Белки с поврежденной структурой накапливаются в коре головного мозга, слипаются, образуя крупные белковые агрегаты, и приводят к нарушению работы нейронов и синапсов. При развитии болезни Альцгеймера наблюдаются конформационные изменения двух белков: тау-белка, или microtubule-associated protein tau (MAPT), и предшественника бета-амилоида, или amyloid precursor protein (APP). Причиной, по которой тау-белок, в норме стабилизирующий микротрубочки, начинает вести себя аномально, является его гиперфосфорилирование, в механизме которого главную роль играет GSK3. Гиперфосфорилированный тау-белок способен влиять на неизмененный тау-белок, вызывая тем самым его слипание в агрегаты. Такие соединения уже не способны к стабилизации микротрубочек, которые ответственны за передачу сигналов вдоль аксонов. Бета-амилоидные бляшки образуются из APP под действием протеолитических ферментов, преимущественно β- и γ-секретазы; они вредны для кальциевого обмена, поскольку такое нарушение приводит к апоптозу.
При исследовании мозга человека, страдавшего от БА было обнаружено повышение уровня содержания молекулярных шаперонов (по-другому их называют белками теплового шока и используют сокращение HSP) и ко-шаперонов: HSP-27, HSP-70, HSP-60, HSP-90 и STl1, α-Б-кристалина. HSP27 и α-Б-кристалин поддерживают β-амилоид в токсичной нефибриллярной форме. В то же время имеются данные, что низкомолекулярные sHSP препятствуют распространению токсичности β-амилоида. HSP-70 и HSP-90 способствуют правильному скручиванию тау-белка в функциональные микротрубочки, уменьшая его гиперфосфорилирование и предотвращая тем самым образование белковых агрегатов. Также HSP70 и HSP90 повышают деградацию неправильного свернутого тау-белка.
Неправильно свернутые белки называются misfolded proteins. Каков же общий механизм действия шаперонов? После обнаружения подобного нарушения структуры шаперон возвращает белок в исходную ненативную конформацию. В такой конформации белок представляет цепочку аминокислотных остатков. Шапероны связываются с белковыми цепями и тем самым не дают им слипнуться между собой и образовать агрегаты, а затем сворачивают их заново в нативную, правильную конформацию.
Подробнее рассмотрим роль HSP-70.
В ходе исследований, проведенных I. Rivera и ее коллегами, было замечено, что HSP-70 повлиял на процесс сборки in vitro Aβ олигомера. Более того, присутствие HSP-70 уменьшило Aβ токсичность культивируемых нейронов (клетки N2A). Как это выяснили? Aβ-пептиды в мономерной форме инкубировали при температуре 37 градусов по Цельсию, постепенно увеличивая концентрацию HSP-70. Добавление HSP-70 к Aβ-мономерам привело к уменьшению процесса олигомеризации (рисунок 1), даже когда молекулярное соотношение между HSP-70 и пептидами бета-амилоида составляло 1:150. Хотя добавление HSP-70 к Aβ приводило к ингибированию комплексов с большой молекулярной массой, он, по-видимому, не влиял на наличие димерных, тримерных и тетрамерных комплексов. Затем клетки N2A инкубировали с HSP-70 (0,2 мкМ), пептидными мономерами Aβ (10 мкМ) или сочетанием пептидных мономеров Aβ и HSP-70 (соотношение 1:50) при 37 ° C в течение 48 часов. Снижение клеточной смерти на 50 % наблюдалась в клетках, инкубированных совместно с Aβ пептидом и HSP-70, по сравнению с клетками, инкубированными только с пептидом Aβ (рисунок 2).
Второе добавление HSP-70 (0,32 мкг, 0,4 мкМ конечный) спустя 24 ч в инкубированные пептиды Aβ и HSP-70 приводило к дальнейшему снижению количества погибших клеток (70 %), в отличие от клеток, которые инкубировали только с пептидами Aβ. При инкубации клеток только с HSP-70 токсического эффекта не наблюдалось.
В конце инкубации (48 ч) клеток, подвергнутых воздействию пептидов Aβ и HSP-70, во внеклеточной среде было обнаружено присутствие форм Aβ. Наблюдалась олигомеризация Aβ в образцах, собранных из клеток, которые были первоначально инкубированы с мономерным Aβ, что указывает на то, что мономеры образуют олигомеры во время инкубации при 37 ° C. Напротив, присутствие олигомеров Aβ1-42 было значительно снижено в среде клеток, инкубированных с пептидами Aβ и HSP-70. Это наблюдение подтверждает, что HSP-70 препятствует олигомеризации пептида Aβ, следовательно, в результате снижается его токсичность.
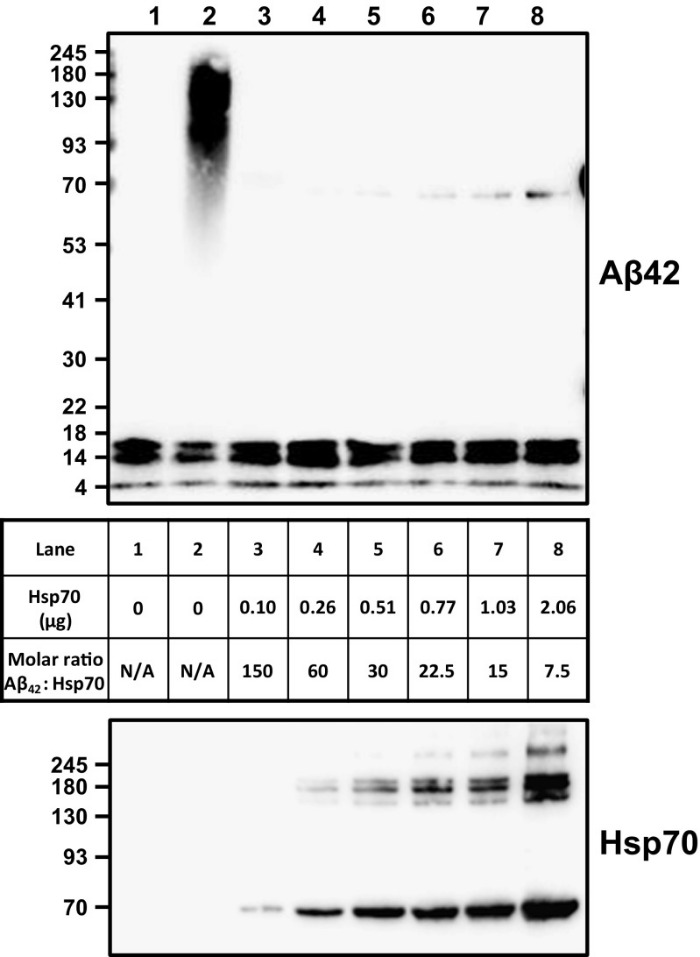
Рисунок 1 | Уменьшение процессов олигомеризации на фоне добавления HSP-70 к Aβ-мономерам
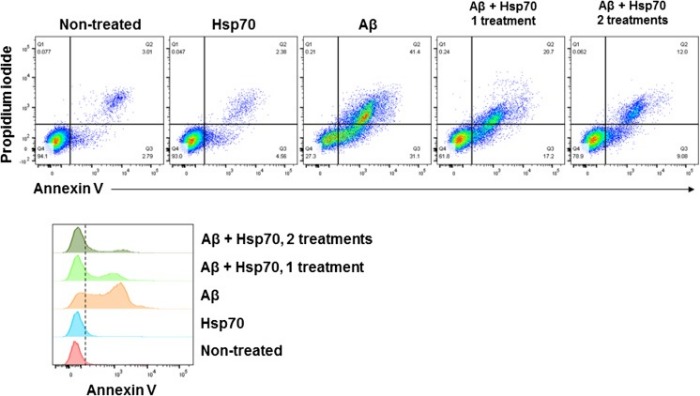
Рисунок 2 | Сравнении жизнеспособности клеток инкубированных совместно с Aβ пептидом и HSP-70 с клетками, инкубированными только с пептидом Aβ
На рисунке 3 представлена модель олигомеризации Aβ-пептида и роль в этом процессе HSP70. Aβ-пептиды и HSP70s высвобождаются из нейронов, глиальных клеток и астроцитов во внеклеточную среду. Мономеры Aβ получены ферментативным расщеплением мембранного APP. После высвобождения Aβ инициирует очень быстрый процесс олигомеризации с образованием димеров, тримеров и тетрамеров с последующей медленной сборкой олигомеров с большой молекулярной массой, которые представляют собой цитотоксические комплексы и волокна. HSP70s являются препятствием для сборки этих олигомеров с большими молекулярными массами - цитотоксичность снижается.
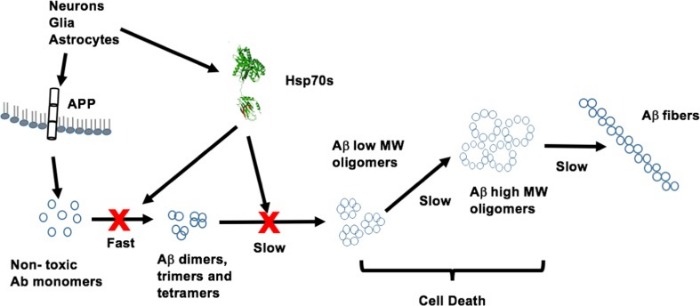
Рисунок 3 | Модель олигомеризации Aβ-пептида и роль HSP70 в этом процессе
Таким образом, проведенный эксперимент доказал, что HSP-70 снижает степень токсичности бета-амилоидных бляшек, препятствуя их образованию.
Источники
1. Rivera I., Capone1 R., David M. Cauvi1, Nelson Arispe 3, De Maio A. (2018). Modulation of Alzheimer's amyloid β peptide oligomerization and toxicity by extracellular HSP70. Cell Stress and Chaperones 23:269–279.
2. Sun Y1, Zhang JR1, Chen S1. (2017). Suppression of Alzheimer's disease-related phenotypes by the heat shock protein 70 inducer, geranylgeranylacetone, in APP/PS1 transgenic mice via the ERK/p38 MAPK signaling pathway. Experimental and therapeutic medicine 14: 5267-5274.
