Центральная серозная хориоретинопатия
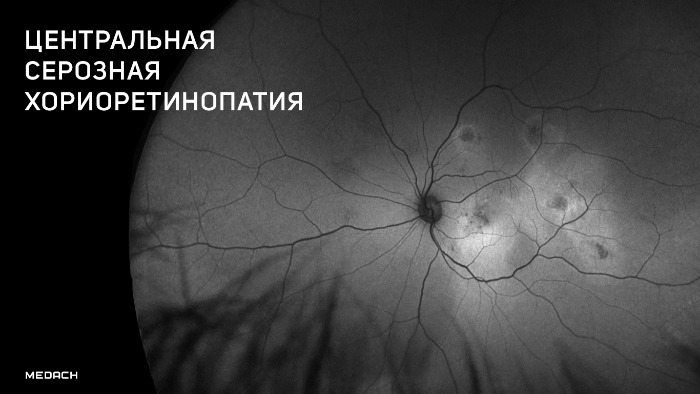
ЦСХ (CSC) представляет собой серозную отслойку нейроэпителия сетчатки с отслойкой пигментного эпителия (RPE, ПЭС) или без нее в результате повышенной проницаемости мембраны Бруха и просачивания жидкости из хориокапилляров через пигментный эпителий сетчатки.
Ранее считалось, что в первую очередь ЦСХ затрагивает мужчин (в 6–10 раз чаще по сравнению с женщинами) в возрасте 30–40 лет. Spaide и его коллеги при наблюдении за 130 пациентами сообщили, что средний возраст таких больных составил 51 год, но они отметили, что у пожилых пациентов с большей вероятностью встречаются диффузные изменения ПЭС и вторичная хориоидальная неоваскуляризация (CNV), предполагая, что развитие заболевания произошло за несколько лет до его манифестации. Для постановки диагноза ЦСХ необходимо в первую очередь исключить возрастную макулярную дегенерацию (AMD) с хориоидальной неоваскуляризацией (CNV), которые по своим клиническим проявлениям могут напоминать ЦСХ.
CSC чаще встречается у представителей европеоидной расы, латиноамериканцев и азиатов, нежели чем у афро-американцев, однако это предположение остается спорным по сей день. Этиология данного заболевания не выяснена до сих пор, несмотря на достижения в методах визуализации и многочисленных проведенных исследованиях.
Современное понимание патогенеза CSC подчеркивает особую роль сосудистой оболочки. Использование индоцианин-зеленой ангиографии (ИЦЗА) показало важность состояния хориоидальной циркуляции в патогенезе ЦСХ (наличие многофокусной повышенной хориоидальной проницаемости и гиперфлюоресценцию). Это наводит на мысль о том, что дисфункция сосудистой оболочки впоследствии приводит к вторичной дисфункции прилежащего ПЭС.
Считается, что сверхпроницаемость сосудистой оболочки приводит к увеличению гидростатического давления тканей, что способствует отслойке пигментного эпителия (PED), подавляя его барьерную функцию, и приводит к накоплению жидкости между сетчаткой и ПЭС, а также отложению фибрина и иногда липофусцина.
Была обнаружена взаимосвязь между развитием ЦСХ и использованием ГКС. Глюкокортикоиды могут потенциально влиять на течение болезни, воздействуя на собственно сосудистую оболочку, мембрану Бруха или ПЭС. Предлагаемые механизмы в хориоидее включают влияние на ауторегуляцию хориоидальной гемодинамики посредством повышенной транскрипции адренергических рецепторов или потенцирования сосудистой реактивности, различные эффекты от вызванной стероидами системной гипертензии или протромботического эффекта. Carvalho-Recchia и соавторы показали, что у 52 % пациентов с ЦСХ в анамнезе выявлялось использование стероидов за 1 месяц до проявлений заболевания по сравнению с 18 % контрольной группы. Кортикостероиды могут влиять на мембрану Бруха посредством их известного ингибирования синтеза коллагена.
Кроме того, Tewari и его коллеги установили, что пациенты с ЦСХ имеют снижение парасимпатической активности и значительное увеличение симпатической активности вегетативной нервной системы.
L. Cotticelli и коллеги показали интересную взаимосвязь между Helicobacter pylori и ЦСХ. Так в одном из исследований было показано, что среди пациентов с ЦСХ частота инфицирования НР составляет около 40 % в сравнение с 25 % частотой инфицирования среди населения в целом. Одним из предполагаемых механизмов иммуно-опосредованного повреждения хориоидальных эндотелиальных клеток считается молекулярная мимикрия НР. В дальнейших исследованиях была попытка установить взаимосвязь между частотой снижения возникновения ЦСХ и эрадикационной терапией НР. Однако полученные результаты не смогли подтвердить ни вышеописанную взаимосвязь, ни прямую взаимосвязь между НР и ЦСХ.
ЦСХ по типу течения разделяют на острую и хроническую. Для острой ЦСХ (чаще развивается у молодых пациентов) характерна спонтанная резорбция субретинальной жидкости в течение 1–6 месяцев с восстановлением нормальной или близкой к норме остроты зрения. При этом во время проведения ФАГ будут определяться единичные или точки «просачивания» флуоресцирующего агента через ПЭС. Если заболевание развивается у лиц старше 45 лет, характеризуется двусторонним поражением и течением более 12 месяцев, а также при проведении ФАГ выявляется наличие множественных точек просачивания флуоресцирующего агента, то можно предполагать наличие хронической формы ЦСХ.
При опросе пациентов с ЦСХ основной их жалобой, из-за которой они вынуждены обратиться к специалисту, будет нерезкое снижение остроты зрения, чаще в утренние часы. Здесь стоить уточнить момент, что острота зрения может быть улучшена при гиперметропической коррекции (т. н. диоптрийный синдром). Помимо этого, при более подробном сборе анамнеза такие больные будут предъявлять также жалобы на наличие темного пятна перед глазом (центральная скотома), уменьшение или увеличение размеров рассматриваемых предметов (микро- и макрофотопсии), а также искажение формы рассматриваемых предметов (метаморфопсии).
При проведении визометрии будет выявляться снижение остроты зрения в среднем на 0,2–0,3, которое, как было описано выше, может быть легко скорректировано до исходного показателя при гиперметропической коррекции. При проведении прямой офтальмоскопии необходимо помнить о том, что отслойка является весьма невысокой и ограниченной, что сложно обнаружить при рутинном осмотре; в таком случае необходимо использование высокодиоптрийной линзы или трехзеркальной линзы Гольдмана. В обзорном окошке — дисковидная серозная отслойка в макулярной области, ограниченная дуговым рефлексом, макулярный рефлекс размыт, часто отсутствует, в пределах серозной отслойки — сероватые или желтоватые точки — преципитаты на задней поверхности сетчатой оболочки (преципитаты Бэра).
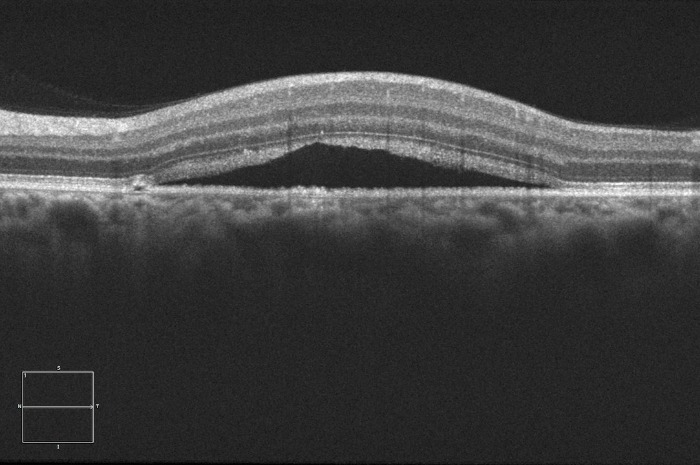
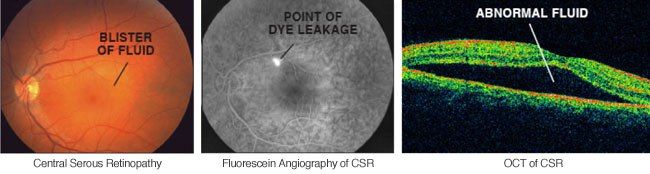
Наиболее объективным является исследование сетчатки с помощью оптической когерентной томографии (ОКТ). Так, на томограммах будет хорошо визуализироваться жидкость, располагающаяся между нейроэпителием и комплексом ПЭС + хориоидея. Также будут отчетливо видны дефекты ПЭС, через которые жидкость просачивается в субретинальное пространство. Наличие контраста между серозной жидкостью с низкой степенью светового отражения по сравнению с тканью сетчатки позволяет выявить участки отслоения или расслоения сетчатки.
При проведении ФАГ, как упоминалось выше, отмечается выявление участков гиперфлуоресценции (зоны серозной отслойки сетчатки в ранних фазах), которые будут соответствовать участкам просачивания флюоресцеина через ПЭС с формированием типичного симптома, описываемого в разных источниках как симптом «дымовой трубы» или «фары в тумане». Точка просачивания может быть представлена пятнышком при поступлении флюоресцеина в количестве, недостаточном для прокрашивания большой площади отслойки, либо полоской в противоположном случае.
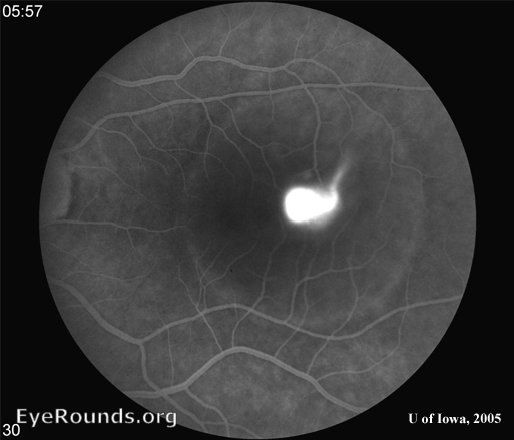
Рисунок 2 | Отслойка нейроэпителия и просачивание красителя при ФАГ
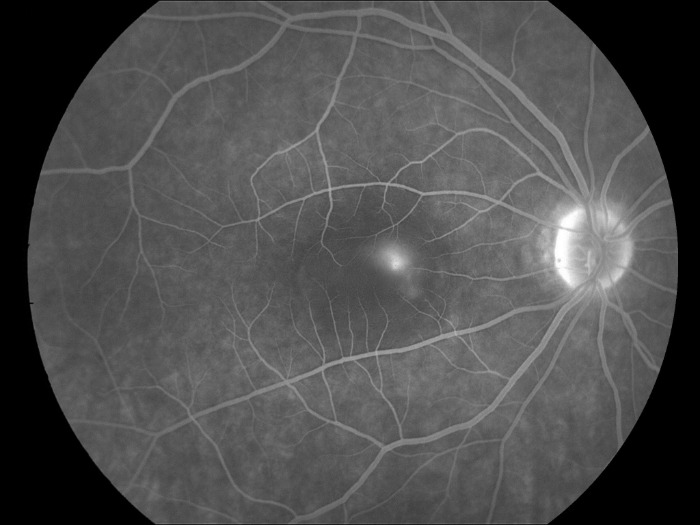
Рисунок 3 | Точка фильтрации видна на ФАГ
Переходя к лечению ЦСХ, первым и главным пунктом является наблюдение. Это связано с тем, что острая ЦСХ в 90 % случаев спонтанно разрешается (стоит помнить, что частота рецидивов достигает 30–50 %), поэтому динамическое наблюдение в течение минимум 3-х месяцев является первоочередным при обращении таких пациентов. Этот срок может быть уменьшен, если нарушения зрения сильно влияют на повседневную жизнь таких больных. Существует мнение, что применение ацетазоламида в терапевтических дозах с перерывами в течение 6 недель уменьшало время исчезновения субъективных и объективных признаков ЦСХ, однако лечение не влияло на финальную остроту зрения и частоту возникновения рецидивов.
Эффективных медикаментозных средств для лечения ЦСХ в настоящее время нет. В первую очередь в начале лечения стоит уточнить у больных момент, касающийся предшествующего появлению симптомов приему ГКС. По возможности стоит отменить их прием, так как это может привести к увеличению уже имеющихся серозных отслоек нейроэпителия.
Перспективным методом борьбы с ЦСХ считалось проведение терапии, направленной на снижение уровня эндогенного кортизола, который, как и экзогенные ГКС, влияет на формирование и дальнейшее прогрессирование ЦСХ. С этой целью использовался кетоконазол, противогрибковый препарат, который частично ингибировал превращение 11-дезоксикортизола в кортизол. С этой целью использовали различные дозировки (от 200 до 600 мг). Эффект был достигнут при использовании 600 мг кетоконазола в сутки в течение 8 недель. Также в качестве «ингибиторов эндогенного кортизола» использовали мифепристон, финастерид, рифампицин. Однако крупных исследований на данный момент проведено не было.
Использование ингибиторов VEGF не относится к терапии первой линии ввиду отсутствия крупных исследований. В исследовании Lim J.W. и Shin M.C. исследовали сосудистый эндотелиальный фактор роста (VEGF) и интерлейкин-8 (IL-8) в водянистой влаге и плазме пациентов с ЦСХ перед интравитреальной инъекцией авастина (в дозе 2,5 мг). Все пациенты с CSC показали существенное повышение центрального зрения с прилеганием отслойки нейросенсорного эпителия после интравитреальной инъекцией авастина. Но было установлено, что уровни водянистой влаги VEGF и IL-8 не были значительно увеличены у пациентов с CSC по сравнению со здоровой группой контроля (18,2 +/– 24,8 против 35,3 +/– 28,5 pg/mL, P > 0,05; 2,3 +/– 0,4 против 2,8 +/– 0,3 pg/mL, Pб> 0,05 соответственно). В плазме уровни VEGF и IL-8 у пациентов с ЦСХ не отличались от группы контроля. В связи с этим эффект введения авастина остается невыясненным.
Еще одно исследование показало, что у больных с ЦСХ отмечается повышенный уровень ингибитора активатора плазминогена по сравнению с контрольной. Этот вывод привел к гипотезе о том, что гиперкоагуляция играет роль в патогенезе ЦСХ. По итогам исследования, проведенного Caccavale и его коллегами с применением аспирина (100 мг в день в течение 1 месяца, затем 100 мг через день в течение 5 месяцев) у 109 пациентов, аспирин ускорял восстановление остроты зрения, уменьшал частоту возникновения рецидивов, а также приводил к лучшему визуальному результату (logMAR +0,07 +/– 0,13 или Snellen 20/23 против +0,17 +/– 0,13 или 20/30, P < 0,0001) в сравнении с контрольной группой.
Эффективным методом лечения ЦСХ остается традиционная или микроимпульсная лазеркоагуляция сетчатки, в зависимости от локализации точек фильтрации. Также перспективным методом коррекции хронической ЦСХ считается фотодинамическая терапия с визудином, а также транспупиллярная методика ФДТ.
Источники:
- Nicholson B. et al. Central serous chorioretinopathy: update on pathophysiology and treatment //Survey of ophthalmology. – 2013. – Т. 58. – №. 2. – С. 103-126.
- Daruich A. et al. Central serous chorioretinopathy: recent findings and new physiopathology hypothesis //Progress in retinal and eye research. – 2015. – Т. 48. – С. 82-118.
