Пересмотр эффекта Варбурга: некоторые опухоли замедляют тканевое дыхание

Опухолевые клетки обычно потребляют нормальное или повышенное количество кислорода в дополнение к гликолизу. Courtney et al. (2018) сообщают об уменьшении митохондриальной функции у пациентов с раком почки и, таким образом, классическом «эффекте Варбурга», что еще раз иллюстрирует гетерогенность метаболизма рака человека.
Почти сто лет назад Отто Варбург и его коллеги отметили, что опухоли потребляют значительное количество глюкозы даже в присутствии кислорода. Это наблюдение было основополагающим для понимания опухолевого метаболизма и послужило основой для своевременного обнаружения и мониторинга злокачественных новообразований с помощью 18-фтор-2-дезоксиглюкозной томографии (FDG-PET) (Liberti and Locasale, 2016). На протяжении многих лет гипотеза Варбурга, теперь называемая эффектом Варбурга или аэробным гликолизом, определялась как переход от окислительного метаболизма глюкозы с участием дыхания в митохондриях к ферментации в ходе гликолиза, которая генерирует лактат в качестве первичного источника энергии.
Однако даже в рамках первоначальной работы Варбурга было обнаружено, что многие виды злокачественных новообразований завершают цикл тканевого дыхания. Действительно, в последние годы с появлением методов анализа ракового метаболизма in vivo было показано, что немелкоклеточный рак легких (НМРЛ) (Hensley et al., 2016), опухолевые заболевания печени (Yuneva et al., 2012), а также первичные и метастатические опухоли головного мозга (Maher et al., 2012) демонстрируют нормальное или даже повышенное полное окисление глюкозы, о чем свидетельствуют изотопные исследования опухолей в мышиных моделях или у пациентов с инфузией 13C-глюкозы. Некоторые виды рака остаются зависимыми от функции митохондрий in vivo (Liu et al., 2016; Weinberg and Chandel, 2015), в то время как другие избирательно требуют аэробного гликолиза (Liberti et al., 2017). Примечательно, что эти явления могут быть связаны как с онкогенным метаболическим перепрограммированием, которое сильно зависит от типа опухолевых клеток, так и от окружения опухоли (Davidson et al., 2016; Yuneva et al., 2012). Эти наблюдения привели к развитию понимания эффекта Варбурга: опухоли приобретают способность использовать повышенный аэробный гликолиз, одновременно сохраняя, если не повышая митохондриальный метаболизм.
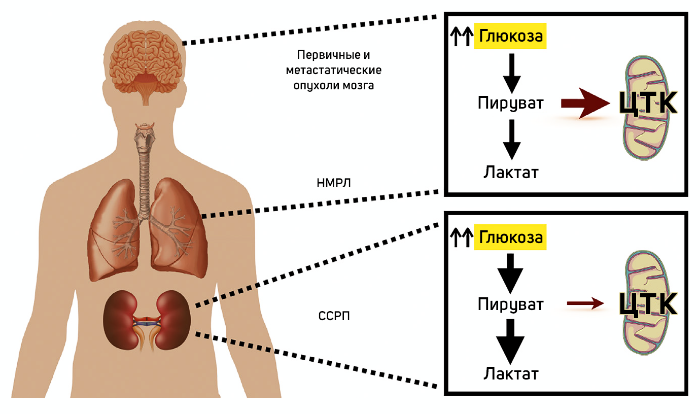
В выпуске Cell Metabolism (Courtney et al., 2018) авторы описывают полученные на пациентах экспериментальные данные, демонстрирующие работу «метаболического переключателя Варбурга» в различных условиях. Пяти пациентам с спорадическим светлоклеточным раком почки (ССРП) перед операцией была введена 13C-глюкоза. Неожиданно было обнаружено, что ССРП имеет удивительно отличающийся метаболический профиль относительно других типов опухолей. Усиленная маркировка метаболитов гликолиза при ССРП (в соответствии с предыдущими наблюдениями в других опухолях), сопровождалась снижением меток метаболитов цикла трикарбоновых кислот (ЦТК) по сравнению с нормальной почкой. Кроме того, опухоли ССРП демонстрировали уменьшенную долю меченых ацетил-КоА и почти не обнаруживаемый меченый глютамин, что указывает на значительное снижение активности ферментов пируватдегидрогеназы (ПДГ) и глютаминсинтетазы. Данные [1,2-13C]-ацетатной маркировки, собранные у одного пациента с ССРП, также указывали на низкий оборот ЦТК, не зависящий от активности ПДГ. Эти данные определяют метаболический фенотип, характеризующийся уменьшенным использованием окисления глюкозы в пользу аэробного гликолиза в соответствии с классическим видом эффекта Варбурга (Рис. 1).
Эти наблюдения особенно интересны при рассмотрении генетических особенностей этого подтипа рака, так как большинство случаев ССРП обусловлено потерей гена VHL — супрессора опухоли. Этот ген кодирует E3-убиквитин-лигазный компонент, который способствует деградации индуцируемых гипоксией факторов HIF-1a и HIF-2a, в результате чего ССРП имеет псевдогипоксическое состояние, характеризующееся повышенным накоплением HIF и активностью вследствие потери VHL. Учитывая хорошо известную роль HIF-1a в регулировании эффекта Варбурга, было высказано предположение, что метаболическая дисфункция может быть наиболее характерной для этих опухолей. Таким образом, индукция псевдогипоксического состояния клетки может быть одним из механизмов, включающих классический эффект Варбурга.
Двигаясь вперед, будет интересно узнать, является ли это уменьшение окисления глюкозы свойственным опухолям, не имеющим ген VHL, при ССРП, или последствием метаболической адаптации к специфической тканевой среде почек. Представляется вероятным, что этот метаболический фенотип будет наблюдаться при других типах рака, учитывая повсеместное присутствие генов, понижающих регуляцию тканевого дыхания в опухолях (Reznik et al., 2017).
Будет интересно понять, как это снижение дыхания может влиять на микроокружение опухоли и взаимодействие хозяин-опухоль по сравнению с опухолями, которые сохраняют относительно нормальные скорости клеточного дыхания. Например, популяции иммунных клеток и их эффекторные функции имеют разные требования к метаболизму митохондрий; если снижение дыхания является физиологически обоснованным, это также повлияет на инфильтраты иммунных клеток и их соответствующие эффекторные функции. Поскольку методология отслеживания изотопов in vivo, помимо подходов к метаболической визуализации, продолжает совершенствоваться и широко применяться, основные механизмы, которые определяют гетерогенность метаболизма раковых клеток у людей, несомненно, будут лучше поняты. Наконец, несколько текущих исследований у людей нацелены на митохондриальный метаболизм в опухолях.
