Методы инсулинотерапии: постоянная подкожная инфузия инсулина
Сейчас каждый врач в своей практике сталкивается с таким заболеванием, как сахарный диабет 1 типа (СД1). За последние несколько лет общие тенденции подхода к лечению сильно изменились: еще лет десять назад все с ужасом вспоминали эпоху кипячения шприцов, пользуясь многоразовыми и/или одноразовыми шприц-ручками с одноразовыми иглами, а сейчас все чаще можно услышать про помповую инсулинотерапию, или постоянную подкожную инфузию инсулина, провести мониторинг глюкозы, а то и узнать информацию о так называемых close-loop системах. При этом вы наверняка слышали хотя бы одно из этих понятий, однако далеко не каждый в момент необходимости сможет разобраться даже в общих принципах таких методов — о них мы сейчас и поговорим.
Первая искусственная поджелудочная железа появилась в 1963 году: это был огромный агрегат под названием Biostater (рис. 1), который не мог рассматриваться в качестве прибора для проведения постоянной терапии. В сегодняшнем понимании это даже не совсем инсулиновая помпа — прибор измерял уровень глюкозы в венозной крови каждые 5 минут и самостоятельно подавал инсулин внутривенно. Сама концепция подобной терапии далее усовершенствовалась и получила большое количество самых разных реализаций.
Кстати, сама идея использования насоса для введения инсулина была позаимствована из технологий, применявшихся при химиотерапии.
Рисунок 1 | Biostater
Также к 1963 году относят изобретение A. Kadish, который представил первую инсулиновую помпу, можно сказать, портативного вида (рис. 2), во всяком случае, ее можно было носить с собой. Это устройство использовало для инфузии инсулин и глюкагон.

Рисунок 2 | Arnold Kadish
Модель инсулиновой помпы AutoSyringe, получившей широкое практическое применение, принадлежала рукам Dean Kamen (кроме этого, он же в свое время изобрел Segway Human Transporter).
Рисунок 3 | Модель AutoSyringe
Безусловно, современные помпы сильно отличаются от перечисленных выше в первую очередь соотношением внешнего размера и функционала. Также необходимо отметить, что для любого подобного устройства выдвигается ряд требований по безопасности, необходимых для его выхода на рынок и возможности использования у различных пациентов (дети, беременные и т. д.).
Для понимания того, что же делает инсулиновая помпа, давайте сначала разберем, как в самых общих чертах будет компенсироваться СД1 при использовании инсулиновых шприц-ручек («на ручках», режим множественных инъекций инсулина).
При этом методе используется два вида инсулина: длительного действия и короткого. Инсулин длительного действия работает от 12 часов (инъекция 2 раза в сутки) до 48 часов (одна инъекция за двое суток) в зависимости от конкретного вида. Его задача — удерживать уровень глюкозы в крови на примерно одинаковом уровне, имитируя базальную секрецию поджелудочной железы (расход инсулина на процессы жизнеобеспечения), поэтому его также иногда называют базальным.
Инсулин короткого действия действует от 3 до 6 часов, как правило, с выраженным пиком действия; он используется для компенсации съеденной еды, и, соответственно, частота инъекций более индивидуальна, но в среднем составляет от 3 до 5 раз в сутки (классически — перед приемом пищи). Наиболее используемые сейчас шаги дозировки инсулина составляют 0,5 и 1 Ед.
Таким образом, самую общую схему инсулинотерапии при использовании множественных инъекций инсулина можно представить следующим образом (рис. 4).
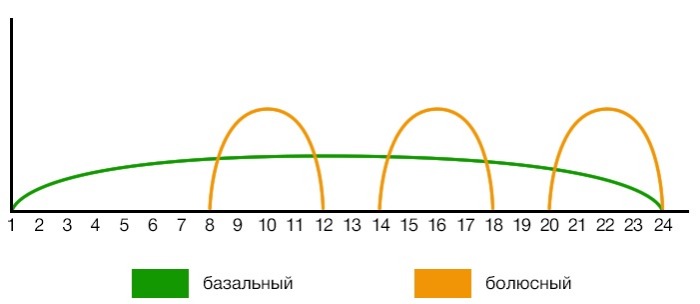
Рисунок 4 | Общая схема инсулинотерапии при использовании шприц-ручек
Инсулиновая помпа — высокоточный прибор, основной задачей которого является постоянное введение заданных пользователем дозировок инсулина. В зависимости от модели минимальный шаг составляет от 0,0025 Ед до 0,05 Ед, что как минимум в 10 раз меньше, нежели при использовании шприц-ручек. Подаваемый инсулин поступает в подкожно-жировую клетчатку постепенно, что создает более благоприятные условия для его реабсорбции и усвоения — при постоянной подкожной инфузии усваивается до 97 % поступающего инсулина против 70 % при использовании шприц-ручек. В связи с этим, а также более тонкой настройкой подачи инсулина, суммарная суточная дозировка инсулина при использовании помпы меньше (до 20–30 %).
В инсулиновых помпах используется один инсулин короткого действия (если точнее, из группы ультракоротких инсулинов), длительность действия которых составляет 3–4 часа. Этот инсулин выполняет роль и базального, и болюсного.
База формируется за счет равномерно распределенных во времени микроподколок: например, если пациенту необходимо подавать по 0,6 Ед/час, то каждые 5 минут будет вводиться по 0,05 Ед (рис. 5).
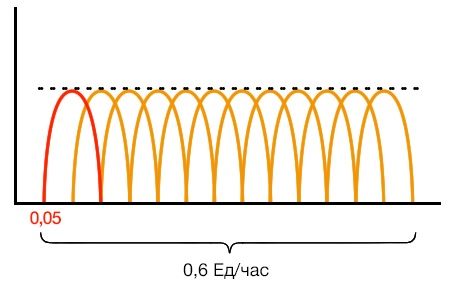
Рисунок 5 | Принцип формирования базы при использовании постоянной подкожной инфузии инсулина
Одним из преимуществ подобного подхода служит возможность изменять уровень базального инсулина в течение дня, не дожидаясь определенного времени инъекции инсулина длительного действия — то есть присутствует возможность увеличить уровень подачи базального инсулина (например, при болезни), уменьшить или вовсе отключить его подачу (при физической нагрузке), что снижает вероятность появления гипогликемического состояния. При этом скорость развития эффекта после изменения скорости подачи инсулина будет составлять от 20 мин до 2 часов (скорость усвоения инсулина и время наступления пика его действия).
Болюсное введение инсулина в помпах реализуется несколькими путями. Самый простой аналогичен таковому при использовании шприц-ручек: вся доза инсулина вводится сразу. Также существует растянутый (квадратный болюс) и болюс двойной волны (болюс нескольких волн). Первый будет работать по принципу, описанному выше для базального инсулина (введение указанной дозировки инсулина в течение указанного уровня), а болюс двойной волны является комбинацией простого и растянутого болюса, и именно он наиболее физиологичен. Это связано с тем, что не вся еда, которую съедает человек, усваивается одновременно.
«Быстрые» углеводы поступают в кровь быстрее, «сложные» влияют на изменение уровня глюкозы в крови более отсроченно, в то время как белки, для усвоения которых также необходим инсулин, оказывают свое воздействие еще позже. Поэтому целесообразно вводить инсулин постепенно: часть болюса, предназначенная для компенсации простых углеводов — сразу, а для белковой еды использовать растянутый болюс. Многими исследованиями показано, что подобный способ введения инсулина способствует уменьшению постпрандиальных уровней глюкозы, а также позволяет избегать постпрандиальных гипогликемий.
Инсулиновая помпа как таковая представляет собой небольшой прибор, внешне похожий на пейджер. Большинство из них — «проводные»: помпа прикреплена к телу человека посредством инфузионной системы — тонкой трубочки, заканчивающейся катетером, по которой инсулин поступает в подкожно-жировую клетчатку (рис. 6). «Беспроводной», вариант помпы представляет собой так называемую пластырную помпу: она состоит из пода, который заполняется инсулином и крепится на тело, а регуляция подачи инсулина осуществляется через пульт дистанционного управления (рис. 7). В этом случае получается, что основная часть помпы прикреплена непосредственно к телу человека.
Рисунок 6 | Вид инсулиновой помпы, подающей инсулин через инфузионную систему
Рисунок 7 | Общий вид «беспроводной» инсулиновой помпы
Современные инсулиновые помпы оснащены дополнительными функциями, такими как калькулятор болюса (расчет необходимого инсулина, исходя из количества углеводов и текущего уровня глюкозы), расчет активного инсулина, различного рода напоминания и будильники, блокировки (защита от случайного введения инсулина) и т. д. Ряд инсулиновых помп интегрируется с глюкометрами, а также — последние модели — с системами непрерывного мониторирования глюкозы.
Недостатки использования помп заключаются в субъективном дискомфорте от постоянного ношения дополнительного прибора на себе и необходимости как регулярной замены инфузионных систем (раз в 2–5 дней в зависимости от их типа), так и внеурочной (например, в связи с окклюзией катетера). Одним из требований к пользователям является регулярное (не менее 4 раз в день) мониторирование уровня глюкозы крови.
И врачам, и пациентам следует помнить, что использование инсулиновой помпы — это всего лишь один из инструментов для компенсации диабета, и ее наличие никак не освобождает больного от необходимости выполнять все остальные предписанные действия (подсчет углеводов, контроль гликемии и т. д.).
Данная статья носит ознакомительный характер: как и у каждого устройства и вида терапии, для описанного метода присутствуют свои показания и противопоказания.
Источники:
- Инсулиновая помпа (помощь врачу и пациенту для эффективного управления диабетом) / И. И. Дедов, В. А. Петеркова, Т. Л. Кураева, Д. Н. Лаптев., - М.: 2014. - 126 с.
- F. M. Alsaleh, F. J. Smith, S. Keady, K. M. G. Taylor Insulin pumps: from inception to the present and toward the future // Journal of Clinical Pharmacy and Therapeutics. - 2010. - №35. - С. 127-138.
