Уязвимость раковых клеток к высоким дозам витамина С Часть 3
Заключительная часть пересказа эссе Брайана Нго о возможной роли витамина C в борьбе со злокачественными опухолями. Сам Брайан подчеркивает, что это высокие дозы витамина С не следует рассматривать как универсальный метод лечения рака, но тем не менее это явление может быть интересно для дальнейшего изучения. Оригинальная статья была опубликована в журнале Nature Reviews Cancer как идея о перспективных направлениях.

Таргетинг эпигенетических регуляторов
Эпигенетическое репрограммирование при раке включает гиперметилирование ДНК, которое часто происходит в промоторных областях островков CpG и, как известно, подавляет супрессоры опухолей.
В большинстве случаев гиперметилирование ДНК при раке можно объяснить повышенной активностью ДНК-метилтрансфераз и потерей активности транслокационных белков (TET, ten-eleven translocation proteins). Транслокационные белки (TET1, TET2 и TET3) деметилируют ДНК и принадлежат к семейству ферментов αКГ-зависимых диоксигеназ.
Используя кислород и αКГ, они катализируют реакции окисления, сначала превращая 5-метилцитозин в 5-гидроксиметилцитозин (Часть 2, рисунок 2). TET2 часто мутирует или соматически утрачивается при миелоидных и лимфоидных злокачественных новообразованиях.
Интересно, что мутации TET2 взаимоисключают мутации, усиливающие активность изоцитратдегидрогеназы 1 (ИЦДГ1) и ИЦДГ2 при миелолейкозе. ИЦДГ1 и ИЦДГ2 превращают изоцитрат в αКГ в цитозоле и митохондриях соответственно.
Но мутация в ИЦДГ1 и/или ИЦДГ2 вызывает изменение ферментативной активности и накопление 2-гидроксиглутарата, который ингибирует функцию αКГ-зависимых ферментов, таких как TET2, что приводит к потере 5-гидроксиметилцитозина, метилированию ДНК и изменению экспрессии генов, которые способствуют развитию рака.
Витамин С как кофактор может активировать транслокационные белки TET. Молекула аскорбиновой кислоты может отдать электрон Fe3+ для синтеза Fe2+, который в свою очередь необходим для активности ТЕТ (Часть 2, рисунок 2). Большая часть мутаций TET2 при остром миелолейкозе — это гетерозиготные мутации, и каждая изоформа TET функционально избыточна. Применение аскорбата может усиливать активность остаточных белков ТЕТ и таким образом предотвращать метилирование ДНК.
Например, ежедневная внутрибрюшинная инъекция высоких доз аскорбиновой кислоты (4г/кг-1) в индуцированной делецией TET2 модели лейкемии на мышах способствовала восстановлению TET2 путем деметилирования ДНК и экспрессии генов, необходимых для дифференцировки миелоидных клеток.
Кроме того, аскорбат in vitro способствовал деметилированию ДНК в генах-усилителях и промоторах генов, связанных с миелоидной дифференцировкой, а также экспрессии нескольких ключевых гемопоэтических генов в клетках мышиного костного мозга, экспрессирующих мутантный ИЦДГ1. При определенных типах лимфом, где TET часто мутируют, лечение аскорбатом in vitro повышает активность TET, приводя к деметилированию ДНК, повышенной экспрессии генов-супрессоров опухоли и повышенной чувствительности к химиотерапевтическим препаратам.
Следует отметить, что во всех исследованиях было исключено влияние окислительного стресса в ответ на высокие дозы аскорбата путем добавления каталазы (которая превращает H2O2 в воду) в культуральную среду, мониторинга изменений клеточных уровней АФК и/или использования 2-фосфат l-аскорбиновой кислоты — стабильного производного витамина С, которое не окисляется в условиях эксперимента.
Также лечение мышей аскорбатом способствовало повышению уровня 5-гидроксиметилцитозина в клетках меланомы и рака мочевого пузыря. Предполагается, что лечение аскорбатом также может быть эффективным при солидном раке с низким уровнем 5-гидроксиметилцитозина.
Еще одно исследование также предполагает, что пероральный прием аскорбата может играть профилактическую роль в развитии лейкоза. Используя несколько различных генно-инженерных моделей мышей, включая мышей Gulo -/-, в организме которых не синтезируется витамин C, и TET2 -/-, было показано, что дефицит аскорбата нарушает регуляцию функции ГСК (гемопоэтические стволовые клетки), что ведет к возникновению лейкоза.
Таргетинг HIF1 сигналинга
Опухоли могут сдавливать окружающие кровеносные сосуды. Чтобы приспособиться к гипоксии, опухолевые клетки активируют фактор транскрипции HIF1 (hypoxia-inducible factor 1 — индуцируемый гипоксией фактор 1), что приводит к активации широкого спектра генов. HIF1, важная мишень в терапии рака, представляет собой гетеродимерный транскрипционный фактор, состоящий из двух субъединиц: O2-регулируемого HIF1α и конститутивно экспрессированного HIF1β.
Ключевой механизм, посредством которого O2 регулирует активность HIF1α, заключается в использовании белков пролин-гидроксилазного домена (PHD1, PHD2 и PHD3) и аспарагин-гидроксилазы (фактор, ингибирующий HIF (FIH)), известных под общим названием HIF-гидроксилазы. В нормоксических условиях PHDs гидроксилируют пролиновые остатки на HIF1α. Пролилгидроксилированный HIF1α затем связывается с белком-супрессором опухолей VHL (von Hippel-Lindau gene — ген болезни Гиппеля-Линдау), который рекрутирует лигазу E3-убиквитин, нацеленную на HIF1α для протеасомной деградации (рисунок 3). С другой стороны, FIHs гидроксилируют остаток аспарагина на HIF1α, который блокирует ассоциацию HIF1α с коактиватором белка p300, что приводит к ингибированию транскрипционной активности HIF1 (рисунок 3). Подобно TET, обе HIF-гидроксилазы принадлежат к Fe2+-содержащим αKГ-зависимым диоксигеназам, которые используют O2 и αKГ в качестве субстратов. Из-за их относительно более низкой аффинности к O2 (константа Михаэлиса (Km) = 230–250 мкМ) по сравнению с другими, αKГ-зависимые диоксигеназы s76 в гипоксических условиях PHD и FIH неактивны, что приводит к стабилизации и активации HIF1.
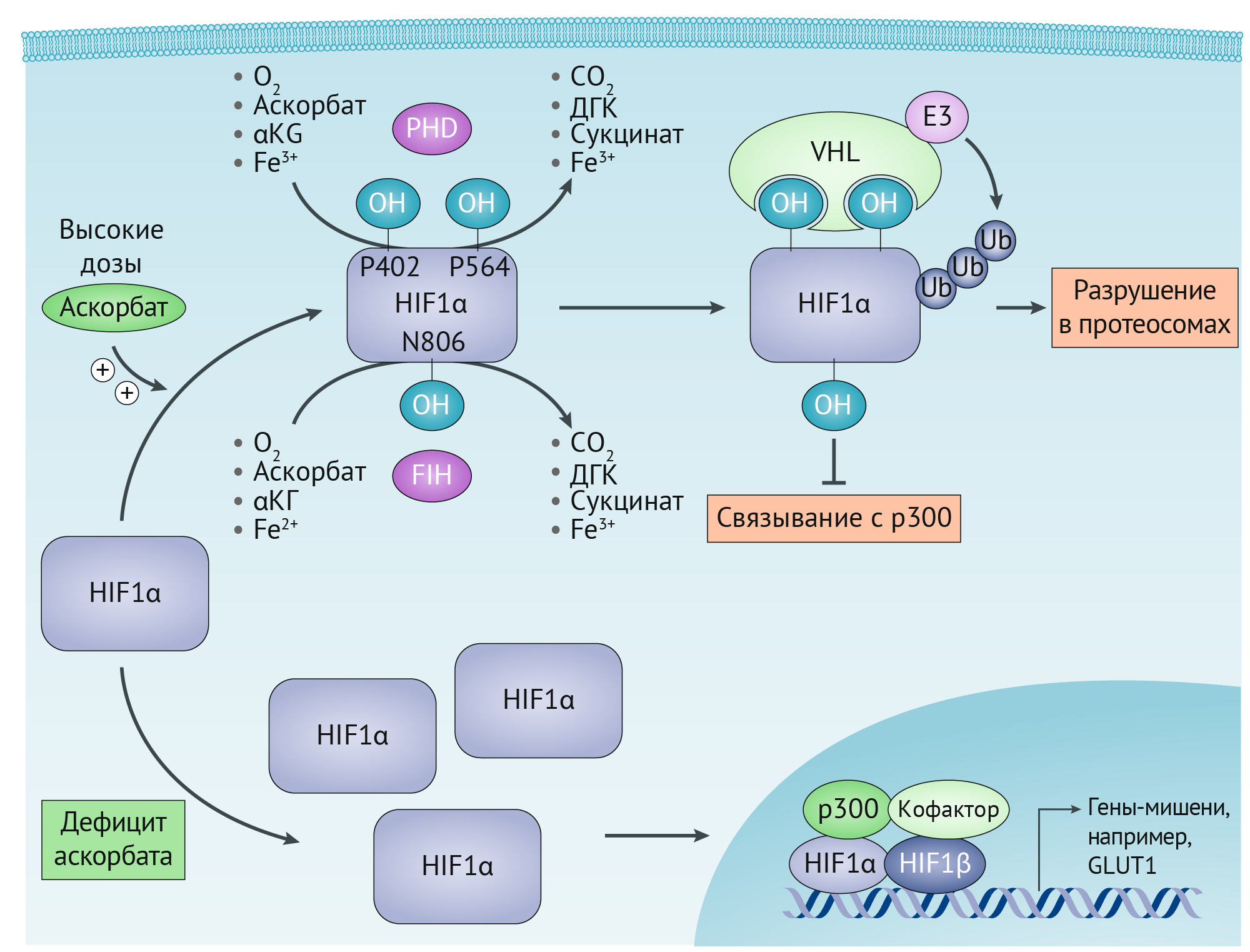
Рис 3 | Аскорбат и регуляция HIF1α
Подобно ТEТ, HIF гидроксилазы нуждаются в аскорбате в качестве кофактора для рециркуляции Fe2+. Следовательно, клетки с дефицитом аскорбата могут иметь повышенную функцию HIF1α, что потенциально способствует прогрессированию опухоли. Это подразумевает, что применение аскорбата может повышать активность HIF-гидроксилазы, таким образом ингибируя активность HIF1α и подавляя рост опухоли.
Уровень аскорбата обратно пропорционален уровню экспрессии HIF1α при поражениях щитовидной железы, и исследование in vitro показало, что лечение аскорбатом индуцировало дозозависимое снижение экспрессии HIF1α и ГЛЮТ1 в раковых клетках щитовидной железы.
В исследованиях на мышах Gulo -/- карцинома легкого, имплантированная мышам Gulo -/-, росла медленно, когда мышей лечили высокими дозами аскорбата в питьевой воде (3,3 г на литр) или ежедневными внутрибрюшинными инъекциями (1 г/кг—1), по сравнению с мышами Gulo -/-, получавшими низкую дозу аскорбата в питьевой воде (0,33 г на литр). Опухоли, подвергшиеся воздействию высоких доз аскорбата, также имели пониженные уровни экспрессии HIF1α, VEGF (vascular endothelial growth factor — фактор роста эндотелия сосудов, ФРЭС) и пониженную плотность микрососудов.
Кроме того, ретроспективные исследования на людях также подтверждают связь между витамином С, активностью HIF1 и онкогенезом. С использованием образцов опухолей пациентов и контрольных образцов рака эндометрия, почечно-клеточного и колоректального рака (КРР) было продемонстрировано, что опухоли с дефицитом аскорбата обладали наибольшей активностью HIF1.
Также было показано, что пациенты с КРР с высоким уровнем аскорбата в клетках опухоли демонстрировали лучшую выживаемость и более благоприятный исход заболевания.
Пока все исследования свидетельствуют о корреляции, но не о причинно-следственной связи. Стабилизация HIF1α даже в нормоксических условиях может происходить, например, при почечно-клеточном раке, где делеция опухолевого супрессора VHL предотвращает деградацию HIF1α при нормоксии. Клетки почечно-клеточного рака с дефицитом VHL погибают при воздействии витамина С в условиях нормоксии.
Более высокие уровни ГЛЮТ1 в нормоксических VHL-дефицитных клетках, чем в клетках с нормальным уровнем VHL, способствовали увеличению поглощения ДГК (дегидроаскорбиновая кислота), полученного из аскорбата, что приводило к увеличению количества АФК и гибели клеток.
В дополнение к мутациям VHL стабильность и активность HIF1α также могут быть повышены путем мутаций двух ферментов-супрессоров опухолей в цикле трикарбоновых кислот: сукцинатдегидрогеназы (СДГ) и фумаратдегидрогеназы (фумарат ДГ). Мутации, приводящие к потере функции СДГ и фумарат ДГ, способствуют накоплению сукцината и фумарата соответственно. Повышенные уровни сукцината и фумарата могут ингибировать активность HIF-гидроксилазы, и таким образом индуцировать нормоксическую активность HIF1α in vitro.
Витамин С как средство против рака
Высокие дозы витамина С не следует рассматривать как универсальный метод лечения рака.
Способ введения витамина С может влиять на его максимальную концентрацию в плазме у пациентов. В настоящее время считается, что миллимолярная концентрация аскорбата, необходимая для индукции цитотоксичности в раковых клетках, может быть достигнута только при внутривенном введении. Например, клиническое исследование I фазы показало, что концентрации аскорбата могут достигать 25–30 мМ при внутривенной инфузии 100 г витамина С. В этом исследовании концентрации в плазме около 10 мМ поддерживались в течение 4 часов, что, на основании доклинических исследований, достаточно для замедления роста раковых клеток. Исследования показали, что внутривенное введение высоких доз аскорбата хорошо переносится пациентами, улучшает качество их жизни и демонстрирует синергетический терапевтический эффект с лучевой и стандартной химиотерапией, а также снижает побочные эффекты последних.
Но многие из этих исследований не были предназначены для крупномасштабных РКИ — эффективность терапии высокими дозами аскорбата еще предстоит определить. Определено три различных механизма, с помощью которых высокие дозы аскорбата могут ингибировать рост опухолей, возможно, эти механизмы могут не работать изолированно друг от друга. Например, субпопуляции мутантных клеток колоректального рака KRAS или BRAF, которые не были полностью уничтожены с помощью прооксидантного механизма in vivo (возможно, из-за их удаленности от кровеносных сосудов, плохой перфузии или устойчивости к АФК) все еще могут подвергаться воздействию аскорбатной терапии посредством ингибирования передачи сигналов HIF1 и/или активации ферментов TET.
На основании текущих доклинических исследований аскорбат может быть более эффективным у онкологических пациентов с мутациями в KRAS, BRAF, TET2, ИЦДГ1 и/или ИЦДГ2, VHL, SH или FDH.
Комбинированная терапия
Клинический потенциал аскорбата в качестве противоопухолевой терапии может заключаться в использовании совместно с другими видами лечения рака.
Например, недавнее исследование показало, что витамин С усиливает действие ингибитора ДНК-метилтрансферазы 5-аза-CdR (децитабина), способствуя деметилированию эндогенных ретровирусов человека и усиливая экспрессию интерферон-стимулируемых генов, приводящих к гибели раковых клеток.
Выдвигаются предложения использовать высокие дозы витамина С, который, как известно, улучшает функцию иммунных клеток (отвечающих как за врожденный, так и за приобретенный иммунитет). Опухоли существуют в сложной иммунной среде, которая включает нейтрофилы, макрофаги и лимфоциты. Хотя мало что известно о том, как аскорбат используется различными клетками, составляющими микроокружение опухоли, исследования показали, что фагоциты и лимфоциты имеют концентрации аскорбата в 10–100 раз выше, чем в плазме. Более того, появляются новые сведения о влиянии аскорбата на воспалительный ответ и функцию иммунных клеток. Возможно, аскорбат даст синергетический эффект в сочетании с современной иммунотерапией.
Заключение
Недавние открытия разнообразных биологических функций аскорбата и их значение в терапии рака породили интересные и многообещающие гипотезы относительно использования аскорбата в лечении рака. Чтобы полностью выяснить биологические функции аскорбата и его отношение к развитию опухолей, исследователи должны будут использовать модели in vivo. Значительное количество исследований на людях последовательно показывает, что лечение аскорбатом улучшает качество жизни пациентов с раком, а в комбинированной терапии аскорбат защищает здоровые ткани от токсических эффектов, вызванных химиотерапией.
Текущие результаты доклинических и ранних клинических испытаний I/II фазы позволяют предположить, что утверждения Линуса Полинга относительно терапевтического потенциала витамина С при раке могут быть не такими уж возмутительными
Источник: Targeting cancer vulnerabilities with high-dose vitamin C
