Новая парадигма стволовых клеток
Классические представления о гемопоэтических стволовых клетках (ГСК) основываются на том, что поддержание количества клеток крови осуществляется уникальной клеточной популяцией со строго определенным набором характеристик: малочисленность популяции, экспрессия специфических маркеров, состояние «покоя», самообновление за счет асимметричного деления (одна из дочерних клеток полностью идентична материнской, вторая — вступает на путь дифференцировки до зрелой клетки и утрачивает стволовые свойства), однонаправленная дифференциация (невозможность вернуться в мультипотентное состояние и неизбежная гибель) [1, 2]. Эта иерархическая модель послужила стереотипным шаблоном в биологии стволовых клеток и долгое время считалась эталонной. Однако поиски популяции «профессиональных» стволовых клеток в большинстве других тканей не увенчались успехом. В связи с этим возник новый, более широкий подход к пониманию «стволовости» клетки: основополагающим моментом становится способность заменять погибшие клетки. Природа такой клетки может быть различной в условиях устойчивого состояния и в период регенерации тканей [3].
Регенеративный потенциал имеют весьма обильно представленные в конкретной ткани клоны клеток. Например, базальные клетки эпидермиса способны продуцировать клоны, которые со временем меняют форму и размеры, а также способны сохраняться в течение очень длительных периодов [4]. Обнаружение этого факта стало одним из первых поводов усомниться в том, что редкость (малочисленность), асимметричное деление или состояние покоя являются универсальными характеристиками стволовых клеток ткани взрослого организма.
Впоследствии в тканях других активно обновляющихся органов, структура которых включает большие популяции активно пролиферирующих клеток, также были обнаружены регенеративные способности. К таким органам относятся пищевод, кишечные крипты, железы слизистой оболочки желудка и яичко [5]. Как и в эпидермисе, пролиферативные клетки в каждом из этих компартментов имеют потенциал к генерации долгоживущей клеточной линии. Эти постоянно пролиферирующие клетки вынуждены конкурировать за ограниченное пространство стволовой ниши. Активное деление одной клетки может привести к вытеснению соседа, причем этот процесс носит стохастический (случайный) характер. Такая конкуренция в итоге формирует ткань, которая постоянно теряет клоны стволовых клеток, в то время как оставшиеся в нише клоны-«победители» становятся все многочисленнее [6].
Активно делящиеся потенциальные стволовые клетки в этих тканях не соответствуют классическим характеристикам ГСК. Они представлены в органе в изобилии и постоянно делятся по принципу симметричной модели (обе дочерние клетки идентичны материнской). Становится ли каждая из этих двух дочерних клеток фактически стволовой зависит от их местонахождения относительно нишевого пространства. Их продолжительность жизни не предопределена и может быть крайне вариабельна [7].
Поддержание относительного постоянства данной популяции стволовых клеток обеспечивается микроокружением, главным образом, размерами стволовой ниши.
Необратимость процесса клеточной дифференцировки также не абсолютна. Существует пул так называемых резервных стволовых клеток. Он формируется из частично или даже полностью дифференцированных клеток при повреждении тканей (рис. 1) [5, 8, 9]. Такая экстренная мобилизация клеток характерна для печени. Помимо гепатоцит-индуцированной регенерации, потенциально стволовой клеткой является и холангиоцит. Когда различные токсины, вирусы или наследственные дефекты метаболизма приводят к повреждению практически всех гепатоцитов, в ткани печени возле желчных протоков обнаруживаются клетки, экспрессирующие маркеры дедифференцировки (эпителиальную молекулу клеточной адгезии EpCAM или транскрипционный фактор Sox9). Эти овальные клетки (или атипичные протоковые клетки) обеспечивали регенерацию обоих типов клеток (как холангиоцитов, так и гепатоцитов) in vivo на мышиных моделях, у которых пролиферация гепатоцитов генетически заблокирована. «Профессиональных» стволовых клеток в печени не обнаружено, и ее уникальная способность к регенерации обеспечивается за счет пластичности двух эпителиальных клеточных линий — гепатоцитов и холангиоцитов [8, 9].
.
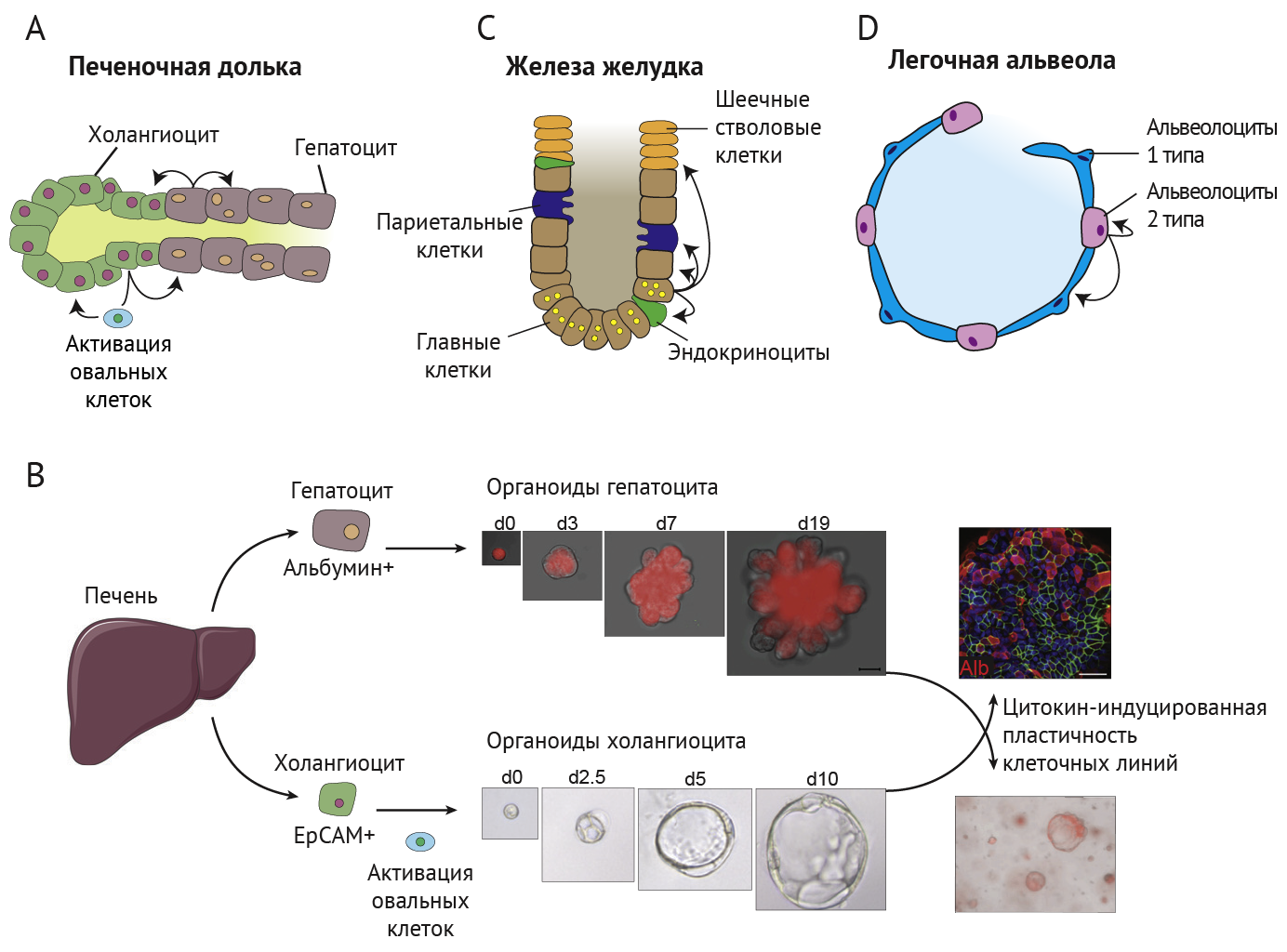
EpCAM+ — молекула клеточной адгезии эпителия
Альбумин+ — экспрессия специфичного для гепатоцитов белка
(B) Клональные органоиды, полученные из гепатоцитов [7] или холангиоцитов [8], могут длительно пролиферировать (на рисунке d – срок культивирования в днях) и трансдифференцироваться между собой.
(C) Дифференцированные главные клетки могут вносить вклад в обновление всех других типов клеток в железах желудка.
(D) В альвеолах альвеолоциты типа 2 (большие или гранулярные) могут действовать как резервные стволовые клетки и генерировать как тип 2, так и тип 1 (плоские или респираторные) [5].
Плюрипотентные стволовые клетки (эмбриональные стволовые клетки, а также
индуцированные плюрипотентные стволовые клетки) могут быть культивированы в течение длительных периодов времени, находясь в состоянии постоянной пролиферации. Отсутствие у данного типа клеток состояния покоя не исключает их способности служить источником всех типов тканей здоровой мыши при инъекции в бластоцисту [5].
Из приведенных примеров становится ясно, что клеточные парадигмы одной системы организма не должны быть экстраполированы на другие. Ткани значительно различаются по размерам клеток и гистоархитектонике, они имеют уникальные физиологические функции и подвергаются различным физическим, химическим и биологическим изменениям. Нет веских оснований предполагать, что эволюция «оснастила» каждый из наших органов универсальным механизмом поддержания целостности тканей. Более вероятно наличие индивидуальных «смарт»-стратегий функционирования стволовых клеток в каждом компартменте.
Источники:
- Buenrostro J.D. et al. Integrated Single-Cell Analysis Maps the Continuous Regulatory Landscape of Human Hematopoietic Differentiation. Cell.2018;173:1535–1548.
- Haas S., Trumpp A., Milsom M.D. Causes and Consequences of Hematopoietic Stem Cell Heterogeneity. Cell Stem Cell. 2018;22:627–638.
- Clevers H., Watt F.M. Defining Adult Stem Cells by Function, not by Phenotype. Annu Rev Biochem. 2018;87:1015-1027.
- Clayton E.et al. A single type of progenitor cell maintains normal epidermis. Nature.2007;446:185–189.
- Post Y., Clevers H. Defining Adult Stem Cell Function at Its Simplest: The Ability to Replace Lost Cells through Mitosis. Cell Stem Cell.2019;25(2):174-183.
- Blokzijl F. et al. Tissue-specific mutation accumulation in human adult stem cells during life. Nature.2016;538:260–264.
- Hu H. et al. Long-Term Expansion of Functional Mouse and Human Hepatocytes as 3D Organoids. Cell. 2018;175:1591–1606.
- Huch M. et al. Long-term culture of genome-stable bipotent stem cells from adult human liver. Cell. 2015;160:299–312.
