PICS — коварный убийца
На современном этапе развития медицина сделала огромный скачок вперед. Многие заболевания, считавшиеся фатальными, сегодня вполне поддаются лечению. Но есть проблема, которая была актуальна как в античности, так и сегодня. Речь идет о тяжелом сепсисе, который часто осложняется полиорганной недостаточностью.
Гомер писал о «заражении крови» в своих поэмах, а Гиппократ даже пытался вылечить «аутоинтоксикацию организма» крепкими алкогольными напитками. Конечно, удавалось это крайне редко и дело было в банальной удаче, а отнюдь не в чудодейственных свойствах этанола.
По сей день патогенез сепсиса окончательно не установлен, и одна из основных задач — понять, как именно развивается полиорганная недостаточность и почему поражаются различные органы и ткани, находящиеся вдали от очага инфекции.
Сам сепсис в современной медицине рассматривается как системный иммунный ответ на инфекцию. При этом «сепсис» не тождественен «септицемии»: возбудителю вовсе не обязательно постоянно циркулировать в крови, чтобы вызвать этот самый иммунный ответ. В связи с этим гораздо чаще говорят о синдроме системного иммунного ответа — SIRS, по этой же причине посев гемокультуры может не дать нужного результата. Сущность сепсиса не в поражающем действии микроорганизма, а в нарушенном ответе на инфекцию [1].
Как же получается, что при септическом поражении страдает весь организм? Все дело в том, что при сепсисе одновременно происходит распознавание множества паттернов опасности и активация огромного количества сигнальных путей.
Патоген-ассоциированные молекулярные паттерны (PAMPs) и паттерны, ассоциированные с повреждением (DAMPs), распознаются комплементом, Toll-, NOD-, RIG-подобными рецепторами различных иммунных клеток, эпителиальных и клеток эндотелия. Все это приводит к активации разных сигнальных путей — MAPK, JAK, STAT, факторов транскрипции (например, NF-κΒ), происходит активация воспаления, но не локально, а на системном уровне [1].
Разбор механизмов развития сепсиса — тема для отдельной статьи, сейчас нас больше интересует, что такого происходит в организме, что все органы один за другим начинают выходить из строя.
Ранее считалось, что вследствие сепсиса развиваются два состояния, идущие одно за другим: синдром системного воспалительного ответа — знакомый нам SIRS, а также синдром компенсаторного противовоспалительного ответа — CARS. Вначале возникает мощный иммунный ответ — SIRS, со временем наступает иммуносупрессия: организм пытается восстановить гомеостаз, но слишком в этом «усердствует», и возникает CARS. Последний проявляется угнетением клеточного иммунитета (лимфопенией), преимущественно страдает Т-звено [2].
Такая модель предполагает, что, после жизнеугрожающего SIRS (когда имеется наибольшая опасность для жизни) наступает компенсаторная реакция (CARS), что свидетельствует о выздоровлении. Но это в корне неверно.
Согласно современным данным, SIRS и CARS возникают одновременно. При этом оказалось, что CARS не имеет никакого отношения к компенсаторным явлениям, да и вообще не является следствием SIRS. Напротив, происходит одновременная гиперактивация факторов врожденного иммунитета (цитокиновый шторм, нейтрофилия) и угнетение Т-клеточного иммунитета с лимфопенией. В результате мы имеем дизрегуляцию иммунной системы [3].
.
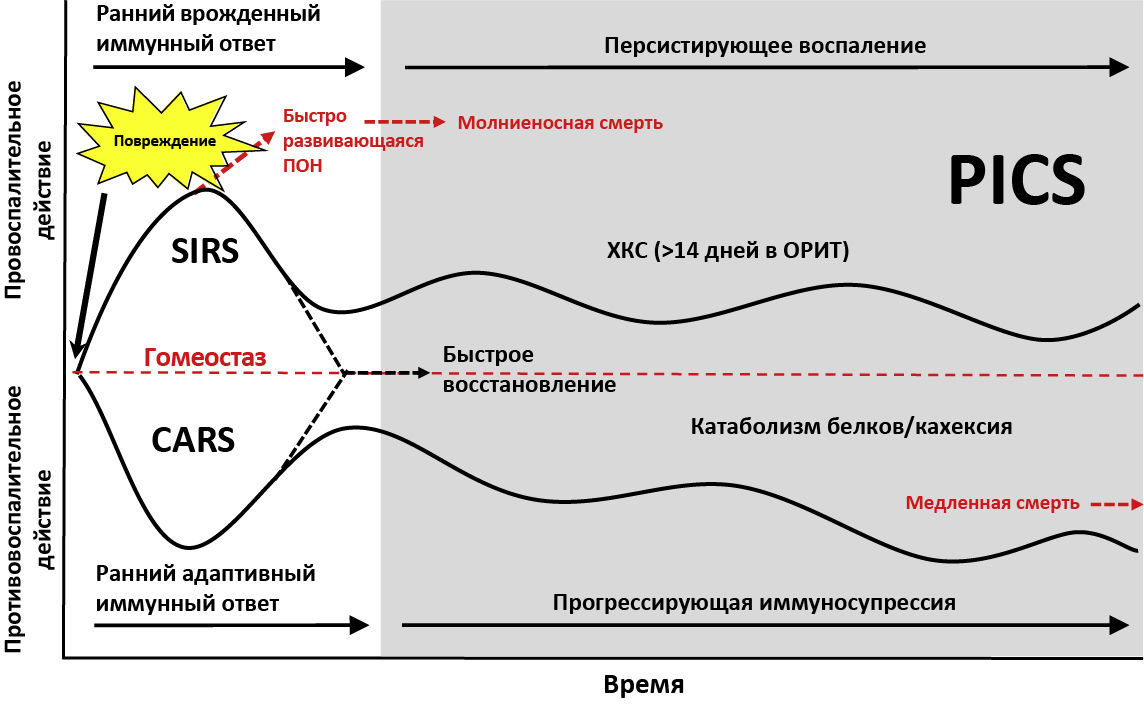
Эта концепция помогла найти объяснение следующей проблеме. В случае если SIRS будет преобладать, возникнет полиорганная недостаточность (ПОН), что может привести к летальному исходу. Об этом мы хорошо осведомлены, и современные методы лечения позволяют предотвратить нежелательные последствия SIRS (см. рис.1).
Но к сожалению, на этом проблемы не заканчиваются. Если пациент не умер вследствие ПОН, далее может быть всего два варианта развития событий: либо гомеостаз иммунной системы восстановится, либо нет. В первом случае все, в общем-то, понятно: пациент выздоравливает, наступает ремиссия.
Но бывает так, что иммунная система никак не может прийти в норму. И тогда возникает синдром персистирующего воспаления, иммуносупрессии и катаболизма — PICS [2]. Если человек более 14 дней находится в отделении интенсивной терапии и у него имеется хроническая полиорганная недостаточность (или одного органа — наиболее часто страдают почки), то говорят о хроническом критическом состоянии (ХКС). ХКС — термин, широко применяющийся за рубежом к пациентам, организм которых никак не может нормализоваться. PICS является таким ХКС вследствие перенесенного сепсиса [4].
Почему так происходит? Окончательного и полного ответа на этот вопрос нет. Предполагается, что в ответ на сепсис (или травму) к очагу повреждения устремляются иммунные клетки из костного мозга, позволяя гемопоэтическим клеткам делиться и заполнять освободившееся пространство (emergency myelopoiesis — «экстренный миелопоэз»).
Но повреждение так быстро устранить не получается, поэтому в кровоток выбрасываются незрелые миелоидные клетки, не способные полноценно защитить организм, но тем не менее поддерживающие воспаление. Также экстренный миелопоэз запускает продукцию большого количества супрессорных клеток миелоидного происхождения (myeloid-derived suppressor cells — MDSCs). MDSCs как раз и обеспечивают основные эффекты PICS: сохраняют врожденный иммунитет, угнетают приобретенный (в основном Т-клеточный), продуцируют большое количество провоспалительных цитокинов [2], [3].
Как всегда, вся проблема в нарушении гомеостаза. MDSCs крайне важны в начальные сроки, когда происходит цитокиновый шторм и активация всех защитных систем организма, чтобы предотвратить чрезмерно буйную реакцию иммунитета, которая тут же приведет к полиорганной недостаточности.
Но слишком длительное действие MDSCs оказывает организму медвежью услугу: незрелые лейкоциты вкупе с ингибированием макрофагов и Т-лимфоцитов приводят к высокому риску развития нозокомиальных инфекций. Также нарастает анемия и кахексия [5].
Причина последней — в преобладании процессов катаболизма. Снижается синтез белка, ускоряется его распад, а скелетная мускулатура является наиболее объемным хранилищем белка. По пока неизвестным причинам нарушается работа митохондрий в миофибриллах, а далее запускается апоптоз (в других случаях — аутофагия).
Самое забавное, что детрит, образовавшийся вследствие гибели миофибрилл, сам является фактором, инициирующим воспаление. ДНК, АТФ, фрагменты мембраны — все они являются эндогенными DAMРs, замыкая таким образом порочный круг [4].
Диагностировать PICS можно по следующим критериям [2], [6]:
- нахождение в ОРИТ более 14 дней;
- уровень СРБ более 50 мкг/дл;
- лимфопения — менее 0,8×109/л;
- снижение массы тела на 10 % в период нахождения в стационаре или ИМТ < 18;
- креатинино-ростовой индекс < 80 %;
- альбумин < 3,0 г/дл;
- преальбумин < 10 г/дл;
- ретинол-связывающий белок < 10 мкг/дл.
Критерии все еще разрабатываются и постоянно обновляются. Но если с вопросом «кто виноват?» более-менее разобрались, то «что делать?» — пока не совсем ясно. Некоторые авторы предлагают использовать препараты, ингибирующие экспансию MDSCs или некоторые иммуноадъюванты [2]. Конечно, без грамотных РКИ рекомендовать что-то конкретное невозможно.
Однозначно можно сказать, что не стоит расслабляться при кажущемся затишье после сепсиса — это затишье перед бурей.
Источники:
- R. S. Hotchkiss, L. L. Moldawer, S. M. Opal, K. Reinhart, I. R. Turnbull, and J.-L. Vincent, ‘Sepsis and septic shock’, Nat. Rev. Dis. Prim., vol. 2, pp. 1–21, 2016.
- J. C. Mira, S. C. Brakenridge, L. L. Moldawer, and F. A. Moore, ‘Persistent Inflammation, Immunosuppression and Catabolism Syndrome’, Crit. Care Clin., vol. 33, no. 2, pp. 245–258, 2017.
- M. D. Rosenthal and F. A. Moore, ‘Persistent inflammation, immunosuppression, and catabolism: Evolution of multiple organ dysfunction’, Surg. Infect. (Larchmt)., vol. 17, no. 2, pp. 167–172, 2016.
- R. B. Hawkins, S. L. Raymond, and J. A. Stortz, ‘Chronic Critical illness and the Persistent inflammation, immunosuppression, and Catabolism Syndrome’, Front. Immunol., vol. 9, pp. 1–9, 2018.
- H. Horiguchi et al., ‘Innate immunity in the persistent inflammation, immunosuppression, and catabolism syndrome and its implications for therapy’, Front. Immunol., vol. 9, no. APR, pp. 1–20, 2018.
- L. F. Gentile et al., ‘Persistent inflammation and immunosuppression: A common syndrome and new horizon for surgical intensive care’, J. Trauma Acute Care Surg., vol. 72, no. 6, pp. 1491–1501, 2012.
