Гидроксихлорохин и хлорохин в сочетании с макролидом или без него для лечения COVID-19: анализ многонационального реестра

Резюме
Введение
Гидроксихлорохин и хлорохин, часто в комбинации с макролидами второго поколения, широко используются для лечения COVID-19, несмотря на отсутствие убедительных доказательств их эффективности. Хотя в целом они безопасны при использовании по утвержденным показаниям, таким как аутоиммунные заболевания или малярия, безопасность и преимущества таких схем для лечения COVID-19 пока недостаточно подробно проанализированы научным сообществом.
Методы
Авторы провели анализ многонационального реестра использования гидроксихлорохина и хлорохина совместно с макролидами или без них для лечения COVID-19. Реестр включал в себя данные 671 больницы на шести континентах. Авторы включили в анализ пациентов, госпитализированных в период с 20 декабря 2019 года по 14 апреля 2020 года, с положительным лабораторным результатом на SARS-CoV-2. Пациенты, которых лечили по одной из интересующих авторов схем в течение 48 ч после постановки диагноза, были разделены на четыре группы: лечение только хлорохином, хлорохином с макролидом, только гидроксихлорохином или гидроксихлорохином с макролидом; пациенты, не получавшие ни одного из этих препаратов, составили контрольную группу исследования. В анализ не были включены пациенты, лечение которых было начато более чем через 48 ч после постановки диагноза, а также те, кто получал ремдесивир или находился на искусственной вентиляции легких. Основными исходами, интересующими авторов, были внутрибольничная летальность и возникновение желудочковых аритмий de novo (устойчивая или неустойчивая желудочковая тахикардия, фибрилляция желудочков).
Результаты
96 032 пациента (средний возраст 53,8 лет; 46,3 % женщин) с COVID-19 были госпитализированы в течение периода исследования и соответствовали критериям включения. Из них 14 888 пациентов находились в группах лечения (1868 получали только хлорохин, 3783 — хлорохин с макролидом, 3016 — только гидроксихлорохин и 6221 — гидроксихлорохин с макролидом), а 81 144 пациента составили контрольную группу. В больнице было зарегистрировано 10 698 летальных исходов (11,1 %). После учета множества сопутствующих факторов (возраст, пол, этническая принадлежность, индекс массы тела, сопутствующие сердечно-сосудистые заболевания и их факторы риска, сахарный диабет, сопутствующие заболевания легких, курение, иммуносупрессивные состояния и исходная тяжесть заболевания) были подсчитаны показатели внутрибольничной летальности для четырех групп исследования: для гидроксихлорохина 18,0 % (соотношение рисков 1,335; доверительный интервал (ДИ) 95 % 1,223–1,457), для гидроксихлорохина с макролидом — 23,8 % (1,447; 1,368–1,531), для хлорохина — 16,4 % (1,365; 1,218–1,531), для хлорохина с макролидом — 22,2 % (1,368; 1,273–1,469). По результатам проведенного анализа, каждый из них независимо ассоциировался с повышенным риском внутрибольничной летальности по сравнению с контрольной группой (9,3 %). Что касается риска развития желудочковой аритмии de novo во время госпитализации, то и здесь он был повышен в четырех группах исследования по сравнению с контрольной группой: для гидроксихлорохина он составил 6,1 % (2,369; 1,935–2,900), для гидроксихлорохина с макролидом — 8,1 % (5,106; 4,106–5,983), для хлорохина — 4,3 % (3,561; 2,760–4,596), для хлорохина с макролидом — 6,5 % (4,011; 3,344–4,812); риск в контрольной группе составил 0,3 %.
Обсуждение
В результате исследования не было подтверждено преимущество использования гидроксихлорохина или хлорохина (с макролидами или без) на основании исходов госпитализации пациентов с COVID-19. Каждая из этих терапевтических схем была связана с повышенной летальностью в стационаре, а также с увеличением частоты развития желудочковых аритмий de novo.
Финансирование
Исследование было финансировано организацией Тhe William Harvey Distinguished Chair in Advanced Cardiovascular Medicine в Бирмингеме and Women’s Hospital.
Введение
Отсутствие эффективного лечения тяжелого острого респираторного синдрома, вызванного новым коронавирусом SARS-CoV-2, привело к тому, что клиницисты стали применять при COVID-19 препараты, эффективные против других заболеваний. Среди всех «перепрофилированных» препаратов ключевыми оказались хлорохин и его аналог гидроксихлорохин, которые используются для лечения малярии и аутоиммунных заболеваний, таких как системная красная волчанка и ревматоидный артрит [1,2]. В лабораторных условиях было показано, что эти препараты обладают противовирусными, а также иммуномодулирующими свойствами [3,4]. Однако использование этого класса препаратов для лечения COVID-19 основано лишь на небольшом количестве разрозненных данных, которые показали вариабельные результаты в неконтролируемых обсервационных исследованиях, а также в небольших открытых рандомизированных исследованиях, которые в значительной степени не обладали статистической доказательностью [5,6]. Комбинация гидроксихлорохина с макролидом второго поколения, таким как азитромицин (или кларитромицин), также была принята на вооружение клиницистами, несмотря на ограниченные доказательства эффективности [7].
Предыдущие исследования показали, что лечение хлорохином, гидроксихлорохином или любым другим препаратом в сочетании с макролидом может неблагоприятно влиять на сердечно-сосудистую систему: в результате возможно удлинение интервала QT, что может быть предрасполагающим механизмом развития желудочковых аритмий [8,9]. Хотя в настоящее время проводится несколько многоцентровых рандомизированных контролируемых исследований на эту тему, существует острая необходимость в точном клиническом руководстве, поскольку использование хлорохина или гидроксихлорохина совместно с макролидами широко распространено, причем зачастую без учета потенциального риска. У некоторых стран имеются запасы этих препаратов, что приводит к их нехватке у тех, кто нуждается в них по утвержденным клиническим показаниям [10]. Цель настоящего исследования состояла в оценке использования хлорохина или гидроксихлорохина по отдельности или в комбинации с макролидом для лечения COVID-19 путем анализирования большого многонационального реестра, чтобы понять, насколько они распространены в реальной клинической практике. В основном авторы стремились проанализировать связь между этими схемами лечения и внутрибольничной летальностью. Кроме того, авторы оценивали частоту возникновения клинически значимых желудочковых аритмий de novo.
Контекст исследования
Данные, полученные до настоящего исследования
Авторы предприняли масштабный поиск статей в базе данных MEDLINE (через PubMed), опубликованных до 21 апреля 2020 года, используя ключевые слова «новый коронавирус», «2019-nCoV», «COVID-19», «SARS-CoV-2», «терапия», «гидроксихлорохин», «хлорохин» и «макролид». Кроме того, на предмет наличия соответствующих данных были проверены серверы ненапечатанных статей, такие как Medrxiv; также авторы ознакомились с веб-страницами Национального института здравоохранения США и Всемирной организации здравоохранения (ВОЗ). Гидроксихлорохин и хлорохин (совместно с макролидом или без него) широко рекомендуются для лечения COVID-19 на основании данных in vitro о противовирусном действии в отношении тяжелого острого респираторного синдрома, вызванного SARS-CoV-2. Применение этих препаратов основано на результатах небольших неконтролируемых исследований, доказательств же из рандомизированных контролируемых исследований представлено не было. Стоит отметить, что были высказаны опасения о повышенном риске возникновения электрической нестабильности миокарда и развития у пациентов желудочковых аритмий в результате применения этих препаратов в комбинации с макролидами. Улучшают ли они исход или, напротив, вредны при лечении COVID-19, остается неизвестным.
Дополнительная ценность этого исследования
В отсутствие данных рандомизированных исследований существует острая необходимость в оценке реальной клинической практики относительно применения гидроксихлорохина или хлорохина (совместно с макролидами или без них) при лечении COVID-19. Используя международную обсервационную базу данных, содержащую информацию с шести континентов, авторы проанализировали терапию 96 032 пациентов с COVID-19; 14 888 из них лечили гидроксихлорохином, хлорохином или их комбинацией с макролидом. После поправок на возраст, пол, этническую принадлежность, коморбидность и тяжесть заболевания в исходном состоянии было установлено, что применение всех четырех схем лечения ассоциируется с повышенным риском развития желудочковой аритмии de novo и летальным исходом в больнице. Это исследование предоставляет реальные доказательства исходов при использовании данных терапевтических схем, т. к. в него было включено большое количество пациентов со всего мира. Таким образом, на данный момент эти результаты дают наиболее убедительные данные касаемо использования гидроксихлорохина и хлорохина (с макролидом или без него) при лечении COVID-19.
Значение всех имеющихся доказательств
Авторы не обнаружили в литературе никаких доказательств эффективности гидроксихлорохина или хлорохина при использовании как в монотерапии, так и в сочетании с макролидом. Предыдущие данные были получены либо из небольших разрозненных исследований, либо из маломасштабных рандомизированных исследований без доказательной убедительности. Данное же исследование включало в себя большое количество пациентов из разных географических регионов и предоставило наиболее надежные на сегодняшний день объективные характеристики этих схем лечения. Хотя в обсервационных исследованиях невозможно в полной мере учесть неконтролируемые сопутствующие факторы, результаты данного исследования свидетельствуют не только об отсутствии терапевтической пользы, но и о потенциальном вреде применения гидроксихлорохина или хлорохина (совместно с макролидом или без него) у госпитализированных пациентов с COVID-19.
Методы
Особенности реестра и сбор данных
Мы провели анализ многонационального реестра использования гидроксихлорохина или хлорохина в качестве монотерапии или в сочетании с макролидом для лечения COVID-19. В реестре состояла 671 больница, все они были расположены на шести континентах (см. приложение, стр. 3). The Surgical Outcomes Collaborative (корпорация Surgisphere, Чикаго, Иллинойс, США) состоит из деидентифицированных данных, полученных с помощью автоматизированного извлечения информации из стационарных и амбулаторных электронных медицинских карт, баз данных поставщиков и финансовых отчетов. Реестр использует «облачную» платформу для данных системы здравоохранения, которая включает в себя специальные модули для сбора, хранения, анализа данных и отчетности. Для обеспечения качества и валидации используется неавтоматизированный процесс ввода данных, чтобы гарантировать, что количество недостающих ключевых значений сведено к минимуму. The Surgical Outcomes Collaborative (далее — Collaborative) обеспечивает соблюдение рекомендаций Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) в отношении рекомендаций, основанных на данных реальной клинической практики.
Данные со всего мира собираются с помощью автоматизированных механизмов, которые обеспечивают сбор 100 % данных от каждой организации здравоохранения через регулярные, заранее определенные интервалы времени, таким образом уменьшая влияние смещения выборок и пропущенных значений, а также гарантируя, что данные являются актуальными, надежными и релевантными. Исходная документация, доступная проверке, включает электронные стационарные и амбулаторные медицинские записи, и в соответствии с руководством FDA по релевантности фактических данных, сбор информации осуществляется с использованием стандартизированного словаря данных «Health Level Seven-compliant data dictionary» (далее — словарь данных); данные собираются на постоянной основе. Процедура верификации реестра относится к стандартным операционным процедурам, действующим для каждой из четырех сертифицированных по стандартам ISO 9001:2015 и ISO 27001:2013 функций реестра: сбор, хранение, аналитика и представление данных. Словарь данных, используемый Collaborative, служит координационным центром для всех видов сбора и хранения данных. После согласования данных, полученных из электронных медицинских карт, с этим словарем сбор информации завершается с использованием автоматизированных интерфейсов для ускорения передачи данных и обеспечения их неприкосновенности.
Сбор полной выборки из каждой организации здравоохранения проверяется на соответствие финансовым отчетам и внешним базам данных, чтобы свести к минимуму предвзятость отбора. Чтобы снизить риск непреднамеренного раскрытия конфиденциальной медицинской информации, все подобные данные удаляются перед помещением основного массива в «облачное» хранилище. Работа Collaborative направлена на минимизацию последствий необъективности и предвзятости отбора: сбор данных осуществляется по всем направлениям, пациенты последовательно включаются в число исследуемых путем сбора 100 % данных посредством электронных систем с гарантией того, что результаты можно будет обобщить для более широкой популяции. Это сотрудничество соответствует требованиям Агентства США по исследованиям в области здравоохранения и Руководящим принципам качества реестров. С началом эпидемии COVID-19 этот реестр использовался для сбора данных из больниц в США (в соответствии с эпидемиологическими характеристиками населения США) и на международном уровне, чтобы обеспечить представительство в нем данных о различных группах населения на шести континентах. Данные были собраны из различных городских и сельских больниц, университетских и государственных клиник, а также коммерческих и некоммерческих учреждений здравоохранения. Сбор и анализ данных считаются исключенными из рассмотрения по вопросам этики.
Дизайн исследования
Авторы включили в исследование всех пациентов, госпитализированных в период с 20 декабря 2019 года по 14 апреля 2020 года в больницы, присутствующие в реестре, с ПЦР-подтвержденной инфекцией SARS-CoV-2, для которых были зарегистрированы следующие клинические исходы: выписка из больницы или летальный исход во время госпитализации. Положительным лабораторным результатом на SARS-CoV-2 считался положительный результат при высокоэффективном секвенировании или количественной ПЦР с обратной транскрипцией образцов мазков из носа или глотки; этот результат был использован для определения пациента в группу положительных по COVID-19. В каждом случае COVID-19 был диагностирован на основании рекомендаций ВОЗ [11]. В исследование не включались пациенты, не имевшие записи о результате тестирования в базе данных больницы, а также получившие отрицательный результат. Для включения пациента необходим был только один положительный тест. В группу лечения были включены пациенты, получавшие гидроксихлорохин или хлорохин (монотерапия или в сочетании с макролидом второго поколения).
В исследование не включались пациенты, начавшие получать лечение по этим схемам более чем через 48 ч после постановки диагноза. Авторы также исключили данные о пациентах, лечение которых было начато, когда они находились на искусственной вентиляции легких (ИВЛ) или получали терапию противовирусным препаратом ремдесивир. Эти критерии исключения были установлены для того, чтобы регистрировать только тех пациентов, лечение которых было начато в схожую фазу их болезни, а также исключить случаи, когда терапия началась в критической фазе болезни, что могло бы исказить интерпретацию результатов. Таким образом, авторы выделили четыре различные группы терапии, в которых лечение всех пациентов началось в течение 48 ч после установленного диагноза COVID-19: только хлорохин, хлорохин с макролидом, только гидроксихлорохин или гидроксихлорохин с макролидом. Все остальные включенные пациенты составили контрольную группу.
Сбор данных
Для проведения исследования были получены демографические данные пациентов, включая возраст, индекс массы тела (ИМТ), пол, этническую принадлежность, а также континент происхождения. Была собрана информация об основных сопутствующих заболеваниях (на основании МКБ-10 и кодов клинических модификаций), которая содержалась в стационарной или в амбулаторной электронной медицинской карте: сердечно-сосудистые заболевания (включая ишемическую болезнь сердца, застойную сердечную недостаточность и аритмию в анамнезе), курение (в том числе в анамнезе), артериальная гипертензия, сахарный диабет, гиперлипидемия, хроническая обструктивная болезнь легких (ХОБЛ), а также иммуносупрессивные состояния (употребление стероидов, ранняя иммунокомпрометированность или текущая химиотерапия у лиц с онкологическими заболеваниями). Авторы также собрали данные о применении пациентами лекарственных препаратов, включая средства, влияющие на сердечно-сосудистую систему (ингибиторы ангиотензинпревращающего фермента [АПФ], блокаторы рецепторов ангиотензина [БРА] и статины), противовирусные препараты, не входящих в изучаемые схемы лечения. Начало приема гидроксихлорохина или хлорохина во время госпитализации регистрировалось с точностью до часа. Аналогично фиксировалось использование макролидов второго поколения (азитромицина и кларитромицина). Перед началом терапии состояние пациентов оценивалось по шкале оценки тяжести полиорганной недостаточности у больных с септическим синдромом (qSOFA) (включая балльный расчет психического статуса, частоты дыхания и систолического артериального давления) и фиксировалась сатурация (SPO2) при комнатной температуре; эти показатели использовались для оценки тяжести заболевания.
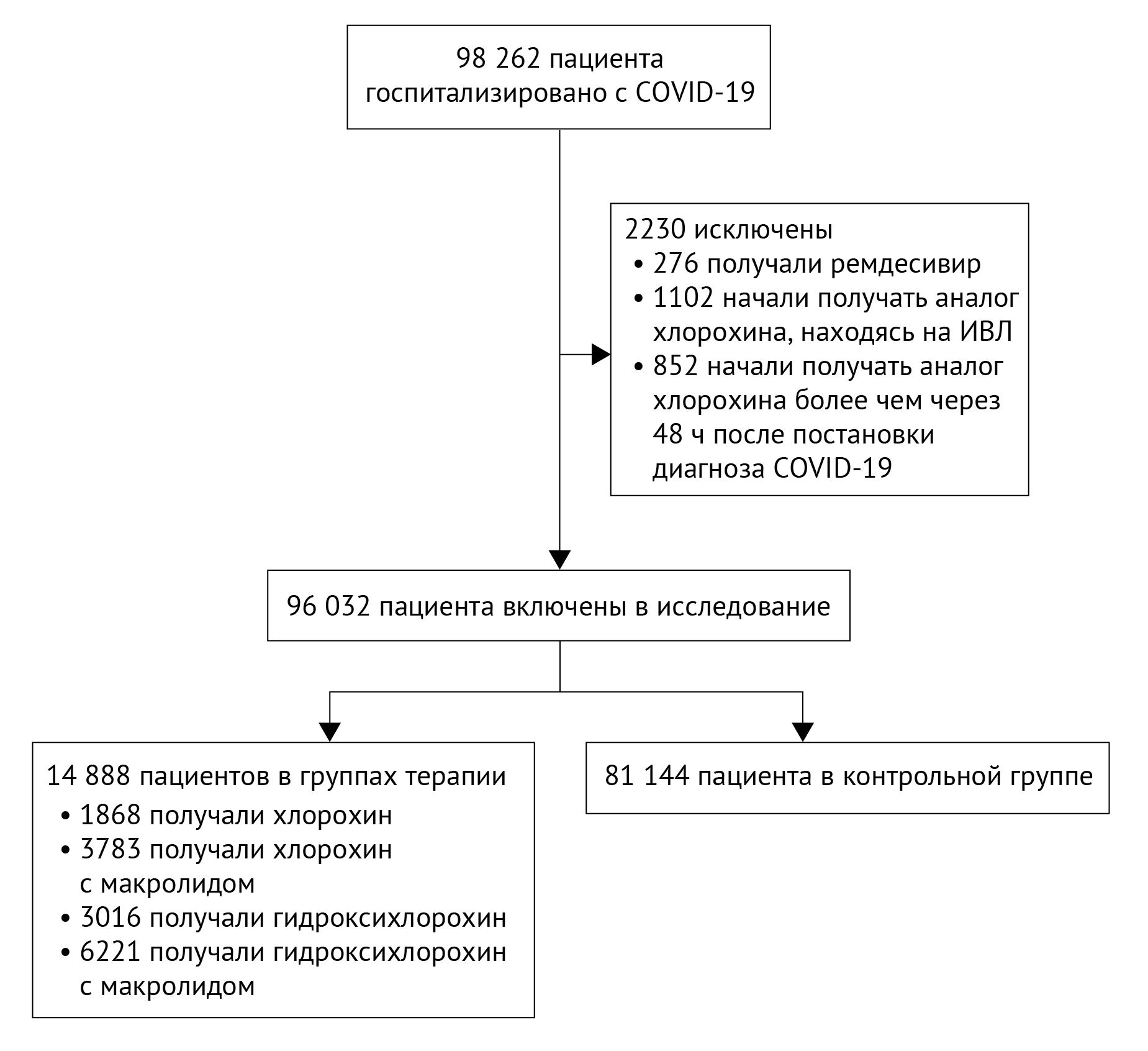
Рисунок 1 | Профиль исследования
Исходы
Первым результатом, представляющим интерес для авторов, была связь между использованием одной из вышеописанных схем лечения (хлорохин или гидроксихлорохин в сочетании с макролидом второго поколения или в монотерапии), начатой на ранней стадии после постановки диагноза COVID-19, и результатом в виде внутрибольничного летального исхода. Вторым результатом, представляющим интерес, была связь между этими схемами лечения и развитием клинически значимых желудочковых аритмий (определяемых как первое появление неустойчивой (не менее 6 сек) или устойчивой желудочковой тахикардии или фибрилляции желудочков) во время госпитализации. Авторы также проанализировали темпы перехода на ИВЛ, а также общую продолжительность пребывания пациентов в отделении интенсивной терапии (в днях) в каждой группе.
Статистический анализ
Для первичного анализа внутрибольничной летальности авторы учитывали наличие сопутствующих факторов, включая демографические показатели, коморбидность, тяжесть состояния при поступлении и другие применяемые препараты (кардиотропные и противовирусные средства). Качественные переменные показаны в виде частот и процентов, а непрерывные переменные — в виде средних значений со стандартным отклонением (SD). Сравнение непрерывных переменных между группами проводилось с помощью t-критерия Стьюдента, а качественные данные сравнивались с помощью критерия Фишера. Значимыми признавались результаты, p которых было менее 0,05. Многократное внесение в систему отсутствующих значений было невозможно, поскольку для обозначения болезни и лекарств не существовало таких кодов, которые бы указывали на отсутствие данных; если электронная медицинская карта пациента не включала информацию о клиническом состоянии, то предполагалось, что эта информация отсутствует.
Регрессионный анализ пропорциональных рисков Кокса был проведен для оценки влияния возраста, пола, этнической принадлежности (европеоидная раса была принята в качестве референтной группы), коморбидности (ИМТ, наличие ишемической болезни сердца, застойной сердечной недостаточности, сердечной аритмии в анамнезе, сахарного диабета или ХОБЛ, курения (в том числе в анамнезе), артериальной гипертензии, иммунокомпрометированного состояния и гиперлипидемии), лекарственных препаратов (кардиотропные, противовирусные и некоторые другие интересные авторам препараты), а также балльной оценки тяжести заболевания (qSOFA < 1 и SPO2 < 94 %) на риск развития клинически значимой желудочковой аритмии (за временной промежуток от дня поступления до первого случая или, если событие не наступило, до момента выписки), а также на риск летального исхода (за временной промежуток от дня поступления до смерти в стационаре или выписки пациента). Возраст и ИМТ рассматривались как непрерывные, а все остальные данные — как качественные переменные. На основе этой модели было оценено соотношение рисков (HR) с ДИ 95 % для включенных переменных, чтобы определить их влияние на риск внутрибольничной смерти (первичная конечная точка) или на риск последующего перехода на ИВЛ или смерти после выписки (комбинированная конечная точка).
Была подтверждена независимость такой переменной, как время выживаемости (или временной промежуток до развития первой желудочковой аритмии). Пропорциональность между предикторами и опасностью была подтверждена с помощью оценки остатков Шенфельда, которая обнаружила p > 0,05; тем самым и была доказана пропорциональность. Чтобы свести к минимуму влияние сопутствующих факторов, анализ соответствия баллов предрасположенности был проведен индивидуально для каждой из четырех групп лечения по сравнению с контрольной группой, которая не получала никакой из перечисленных выше форм лечения. Для каждой группы лечения был определен отдельный согласованный контроль с использованием точных критериев и критериев сопоставления предрасположенности с шагом в 0,001. Этот метод был использован для обеспечения точного сопоставления демографических показателей, коморбидности, тяжести заболевания и исходной терапии всех пациентов. Оценка предрасположенности основывалась на следующих переменных: возраст, ИМТ, пол, этническая принадлежность, коморбидность, применение ингибиторов АПФ или БРА, применение статинов, лечение другими противовирусными препаратами, оценка qSOFA менее 1 и SPO2 менее 94 % при комнатной температуре. Пациенты были сгруппированы так, чтобы средние оценки различий для всех сопоставимых параметров составляли не более 10 %. Были проведены дополнительные анализы для изучения надежности первоначально полученных оценок. Также были проведены индивидуальные исследования по континентам происхождения пациентов и анализы с поправкой на пол с использованием моделей пропорциональных рисков Кокса. Кроме того, был проведен анализ критической точки (это анализ, который показывает влияние и распространенность неизмеряемых сопутствующих факторов, которые могут сдвинуть верхнюю границу ДИ в сторону нуля). Все статистические анализы проводились с использованием программ R (версия 3.6.3) и SPSS (версия 26).
Роль источника финансирования
Представители компании, финансирующей исследование, не играли никакой роли в разработке исследования, сборе данных, их анализе и интерпретации, а также в написании статьи. Первый автор и соавтор ANP имели полный доступ ко всем данным исследования и несли окончательную ответственность за предоставление их для публикации.
Результаты
У 96 032 госпитализированных пациентов из 671 больницы был диагностирован COVID-19 в период с 20 декабря 2019 года по 14 апреля 2020 года; все пациенты соответствовали критериям включения в данное исследование (рис. 1). Все включенные пациенты закончили курс лечения (выписались или умерли) к 21 апреля 2020 года. Пациенты, которые были госпитализированы в течение периода исследования, но не завершили курс лечения, не были включены в анализ. Когорта исследования включала 63 315 (65,9 %) пациентов из Северной Америки, 16 574 (17,3 %) — из Европы, 8101 (8,4 %) — из Азии, 4402 (4,6 %) — из Африки, 3577 (3,7 %) — из Южной Америки и 63 (0,1 %) — из Австралии (приложение, стр. 3). Средний возраст пациентов составил 53,8 лет (SD 17,6); 44 426 из них (46,3 %) были женщинами; средний индекс массы тела составлял 27,6 кг/м2 (SD 5,5; 29 510 [30,7 %] страдали ожирением с индексом массы тела ≥ 30 кг/м2); 64 220 (66,9 %) были светлокожими, 9054 (9,4 %) были темнокожими, 5978 (6,2 %) были латиноамериканцами и 13 519 (14,1 %) были азиатского происхождения (приложение, стр. 4). Что касается сопутствующих заболеваний, то у 30 198 (31,4 %) была гиперлипидемия в анамнезе, 25 810 (26,9 %) — болели артериальной гипертензией, у 13 260 (13,8 %) был сахарный диабет, у 3177 (3,3 %) — ХОБЛ, у 2868 (3,0 %) — сопутствующее иммуносупрессивное состояние, у 16 553 (17,2 %) — курение в анамнезе и 9488 (9,9 %) были курильщиками в текущий момент времени.
Что касается ранее имевшихся сердечно-сосудистых заболеваний, то 12 137 (12,6 %) пациентов в анамнезе имели ишемическую болезнь сердца, 2368 (2,5 %) — застойную сердечную недостаточность и 3381 (3,5 %) — аритмию. Средняя продолжительность пребывания в стационаре составила 9,1 дней (SD 6,4), при этом общее количество летальных исходов в стационаре составило 10 698 (11,1 %) из 96 032. Применение других противовирусных препаратов для лечения COVID-19 было зарегистрировано у 38 927 (40,5 %) пациентов. Наиболее распространенными противовирусными препаратами были лопинавир и ритонавир (12 304 [31,6 %]), рибавирин (7904 [20,3 %]), а также осельтамивир (5101 [13,1 %]). Комбинированная терапия с более чем одним из этих противовирусных препаратов применялась у 6782 (17,4 %) пациентов. Группы лечения включали 1868 пациентов, которым давали только хлорохин, 3016 — только гидроксихлорохин, 3783 — хлорохин с макролидом и 6221 — гидроксихлорохин с макролидом. Медиана времени от госпитализации до постановки диагноза COVID-19 составила два дня (межквартильный размах 1–4). Средняя суточная доза и продолжительность применения различных схем приема препаратов были следующими: только хлорохин — 765 мг (SD 308) и 6,6 дней (2,4); только гидроксихлорохин — 596 мг (126) и 4,2 дня (1,9); хлорохин с макролидом — 790 мг (320) и 6,8 дней (2,5); и гидроксихлорохин с макролидом — 597 мг (128) и 4,3 дня (2,0). С дополнительной информацией о проведенном когортном исследовании можно ознакомиться в приложении (стр. 4–5).
Демографические показатели и коморбидность были сопоставлены между выжившими и умершими пациентами (табл. 1). Умершие пациенты, как правило, были старше, чаще страдали ожирением, чаще были мужчинами, чаще были чернокожими или латиноамериканцами, а также страдали сахарным диабетом, гиперлипидемией, ишемической болезнью сердца, застойной сердечной недостаточностью и аритмиями. У тех, кто не выжил, также чаще болели ХОБЛ и сообщали о том, что являются курильщиками. Распределение демографических показателей, коморбидности и исходов между четырьмя группами лечения показано в таблице 2. Никаких существенных различий между группами по исходным характеристикам или сопутствующим заболеваниям обнаружено не было. Желудочковые аритмии встречались чаще в группах лечения по сравнению с контрольной группой; летальность также была выше в группах лечения по сравнению с контрольной группой (p < 0,0001; приложение стр. 15–18). Независимые прогностические факторы внутрибольничной летальности представлены на рисунке 2. Возраст, индекс массы тела, негроидная раса или латиноамериканская этническая принадлежность (по сравнению с белой расой), ишемическая болезнь сердца, застойная сердечная недостаточность, аритмия в анамнезе, сахарный диабет, артериальная гипертензия, гиперлипидемия, ХОБЛ, курение в настоящее время и иммуносупрессивное состояние были связаны с более высоким риском смерти в стационаре. Женский пол, азиатская этническая принадлежность, применение ингибиторов АПФ (но не блокаторов рецепторов ангиотензина) и применение статинов ассоциировались со снижением риска летального исхода в стационаре.
По сравнению с контрольной группой (9,3 %), гидроксихлорохин (18,0 %; отношение рисков 1,335; 95 % ДИ; 1,223–1,457), гидроксихлорохин с макролидом (23,8 %; 1,447; 1,368–1,531), хлорохин (16,4 %; 1,365; 1,218–1,531) и хлорохин с макролидом (22,2 %; 1,368; 1,273–1,469) были независимо связаны с повышенным риском внутрибольничного летального исхода. Регрессивный анализ пропорциональных рисков Кокса по континентам приведен в приложении (стр. 6–11), также там содержатся данные многофакторного логистического регрессионного анализа с поправкой на пол (стр. 12–13) и сепарационного регрессионного анализа Кокса для комбинированной конечной точки (искусственная вентиляция легких или смерть) (стр. 14). Независимые предикторы желудочковой аритмии показаны на рисунке 3. Ишемическая болезнь сердца, застойная сердечная недостаточность, аритмия в анамнезе и ХОБЛ независимо ассоциировались с повышенным риском развития новых желудочковых аритмий во время госпитализации. По сравнению с контрольной группой (0,3 %), гидроксихлорохин (6,1 %; отношение рисков 2,369; 95 % ДИ; 1,935–2,900), гидроксихлорохин с макролидом (8,1 %; 5,106; 4,106–5,983), хлорохин (4,3 %; 3,561; 2,760–4,596) и хлорохин с макролидом (6,5 %; 4,011; 3,344–4,812) были независимо связаны с повышенным риском развития желудочковой аритмии de novo во время госпитализации. Анализы с использованием сопоставления баллов предрасположенности по группам лечения приведены в приложении (стр. 15–18). Полученные результаты показали, что связь между вышеописанными лекарственными схемами и летальностью, потребностью в искусственной вентиляции легких, длительностью пребывания в стационаре и возникновением желудочковых аритмий de novo согласуется с первичным анализом. Для оценки влияния неизмеряемых переменных на значимые результаты в отношении гидроксихлорохина или хлорохина был проведен анализ критической точки (см. приложение стр. 19–20).
Для хлорохина, гидроксихлорохина и хлорохина с макролидом гипотетический ненаблюдаемый бинарный вмешивающийся фактор с распространенностью 50 % в популяции должен был бы иметь отношение рисков 1,5, чтобы сделать этот результат анализа несущественным (на уровне 5 %). Для сравнения с наблюдаемыми вмешивающимися факторами в этом исследовании: если бы застойная сердечная недостаточность (которая имеет отношение рисков 1,756) была исключена из модели, она должна была бы иметь распространенность приблизительно 30 % в популяции, чтобы вмешаться в результат анализа. Аналогично для гидроксихлорохина с макролидом гипотетический ненаблюдаемый бинарный вмешивающийся фактор с распространенностью 37 % в открытой популяции должен был бы иметь отношение рисков 2,0, чтобы сделать результат этого анализа несущественным (на уровне 5 %). Опять же, застойная сердечная недостаточность (которая имеет отношение рисков 1,756) должна была бы иметь распространенность приблизительно 50 % в популяции, чтобы вмешаться в результат анализа (если бы она не была скорректирована в модели пропорциональных рисков Кокса).
Таблица 1 | Демографические данные и сопутствующие заболевания выживших/умерших пациентов в период госпитализации
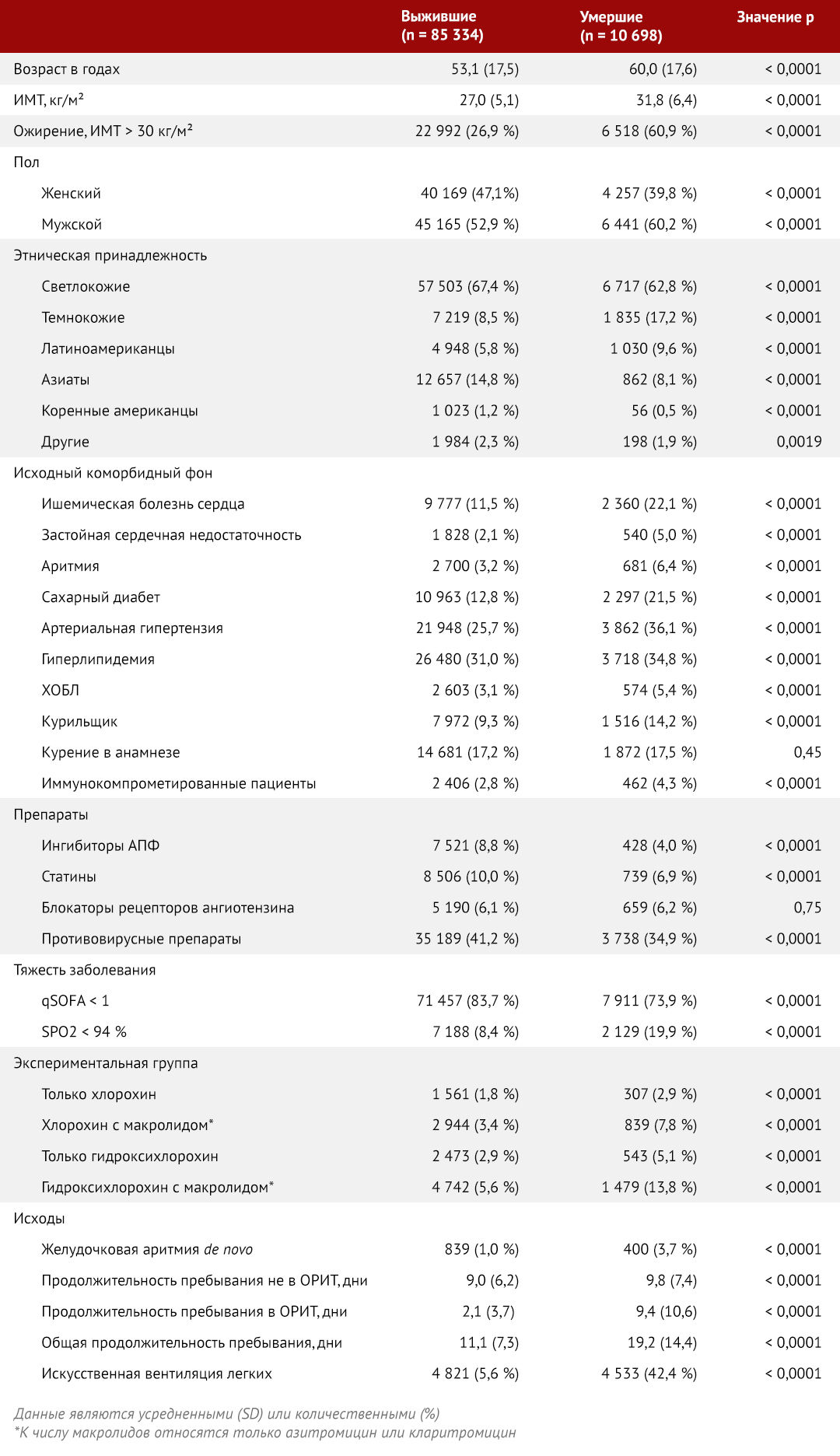
Таблица 2 | Демографические данные и характеристики пациентов в зависимости от группы лечения
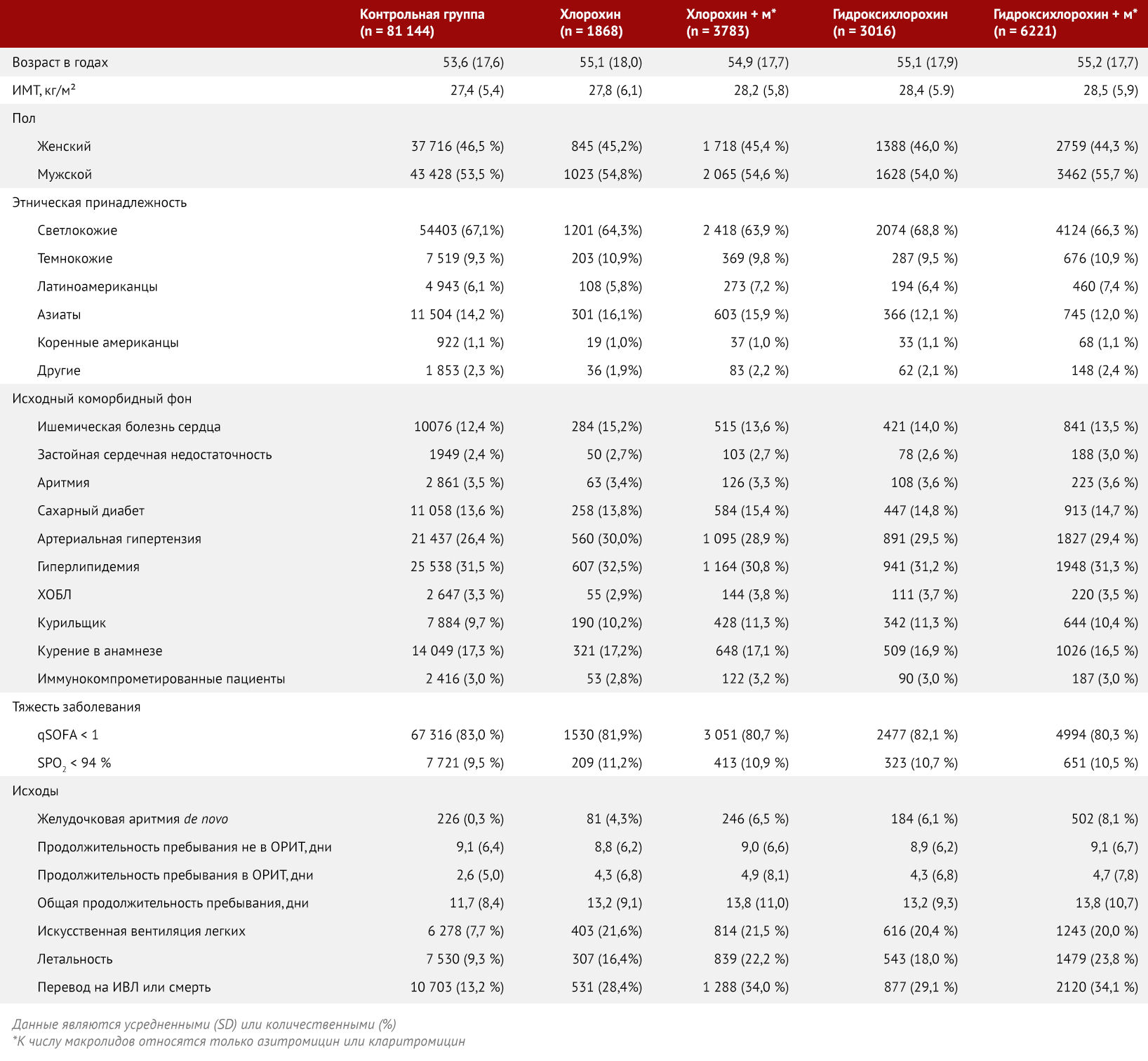
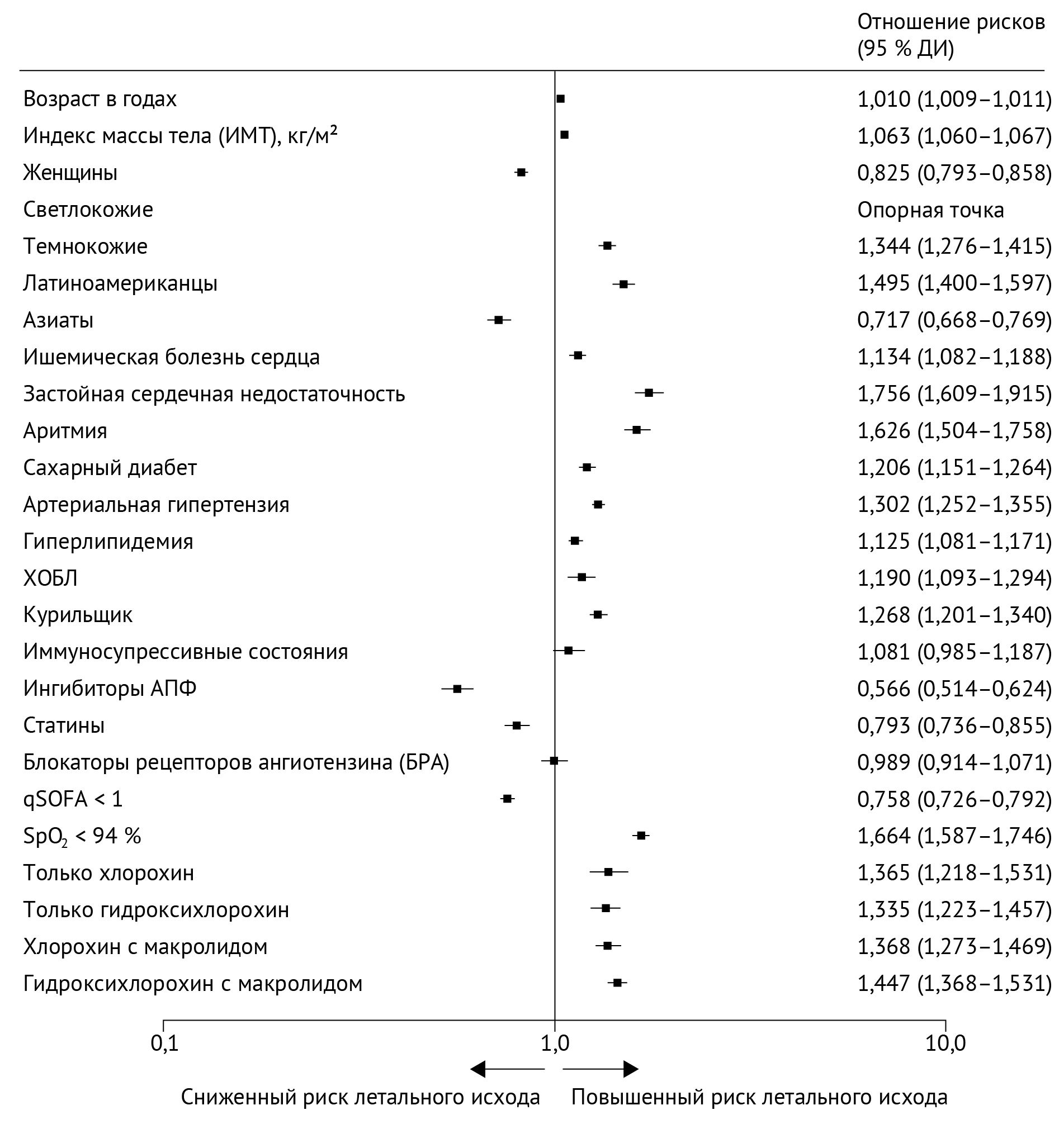
Рисунок 2 | Независимые прогностические факторы внутрибольничной летальности
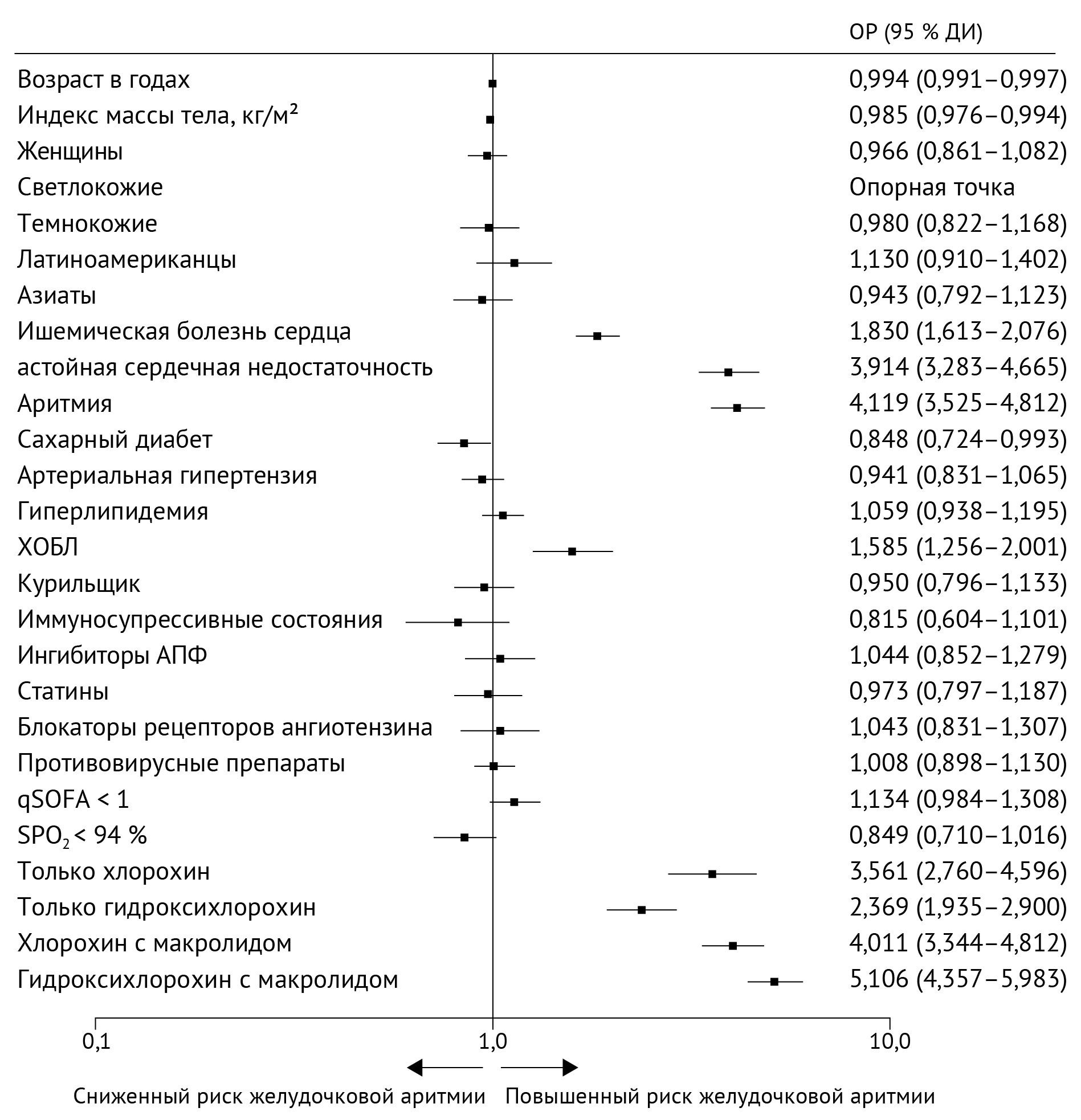
Рисунок 3 | Независимые прогностические факторы развития желудочковых аритмий во период госпитализации
Обсуждение
В ходе этого крупного многонационального исследования авторы не обнаружили никакого позитивного влияния гидроксихлорохина или хлорохина (в комбинации с макролидом или без него) на результаты стационарного лечения, начатого на ранних стадиях после постановки диагноза COVID-19. Применение каждой из терапевтических схем (хлорохин или гидроксихлорохин в комбинации с макролидом или без) ассоциировалось с повышенным риском развития клинически значимых желудочковых аритмий и повышенным риском внутригоспитальной летальности при лечении COVID-19. Использование гидроксихлорохина или хлорохина при COVID-19 основано на широко известных врачебному сообществу небольших неконтролируемых исследованиях, которые показали, что комбинация гидроксихлорохина с азитромицином успешно препятствует вирусной репликации [7]. 28 марта 2020 года FDA выдало разрешение на экстренное применение этих препаратов у пациентов, если проведение клинических испытаний недоступно [12]. Другие страны, такие как Китай, выпустили руководства, разрешающие использование хлорохина при лечении COVID-19 [13]. Некоторые страны создают у себя запасы этих препаратов, что вызывает их нехватку для применения по утвержденным показаниям, таким как аутоиммунные заболевания и ревматоидный артрит [10].
Ретроспективное обсервационное исследование 368 пациентов с COVID-19, получавших лечение в Госпитале ветеранов США, вызвало обеспокоенность тем, что применение гидроксихлорохина было связано с большим риском летального исхода; однако входные характеристики среди представителей проанализированных групп были неодинаковыми, и нельзя исключать возможность предвзятости данных результатов [14]. В другом обсервационном исследовании, проведенном с участием 181 пациента из Франции, сообщалось, что применение гидроксихлорохина в дозе 600 мг в день не было связано со значимой клинической пользой у пациентов с пневмонией коронавирусной этиологии [15]. Данный крупномасштабный международный анализ подтверждает отсутствие клинической пользы хлорохина и гидроксихлорохина и указывает на потенциальный вред при лечении этими препаратами госпитализированных пациентов с COVID-19. Хлорохин и гидроксихлорохин вызывают токсический эффект в отношении сердечно-сосудистой системы, особенно посредством генерации электрической нестабильности, характеризующейся удлинением интервала QT (время, необходимое для деполяризации и реполяризации желудочков). Этот механизм связан с блокадой калиевого канала hERG [16], работа которого способствует увеличению длительности реполяризации и потенциала действия клеток желудочков. При определенных условиях ранняя постдеполяризация может спровоцировать развитие желудочковых аритмий [9].
Подобная склонность к провокации аритмии чаще наблюдается у лиц со структурными сердечно-сосудистыми заболеваниями; сообщается, что течение COVID-19 с высокой частотой осложняется повреждением сердца [17,18]. Кроме того, люди с сердечно-сосудистыми заболеваниями представляют собой наиболее уязвимую популяцию, исходы которой при инфицировании SARS-CoV-2 являются наихудшими среди всех возможных [19,20]. Патологоанатомические исследования показали наличие нарушений в сосудистом эндотелии и диффузного эндотелиита в различных органах при COVID-19 [21]. Вопрос о том, имеют ли пациенты с уже существующим или приобретенным de novo сердечно-сосудистым заболеванием большую склонность к развитию желудочковых аритмий при использовании хлорохина или его аналогов, остается неопределенным, но такая вероятность есть. Развитие COVID-19 характеризуется начальной вирусной репликацией, за которой следует усиленная системная воспалительная реакция [22]. Применение хлорохина или гидроксихлорохина в сочетании с макролидом направлено на синергическое использование их антимикробных свойств. Макролиды, такие как азитромицин и кларитромицин, являются антибиотиками с иммуномодулирующим и противовоспалительным эффектами [24]. Однако эти препараты удлиняют интервал QT и повышают риск внезапной сердечной смерти [8,9]. Борба и его коллеги [25] сообщили о предварительном анализе в ходе двойного слепого рандомизированного исследования с участием 81 взрослого пациента, госпитализированных с тяжелым течением COVID-19 в учреждение медицинской помощи третьего уровня в Бразилии. Это исследование показало, что более высокая доза хлорохина представляет опасность для здоровья, особенно при одновременном приеме с азитромицином и осельтамивиром. В другом когортном исследовании 90 пациентов с пневмонией коронавирусной этиологии Меркуро и его коллеги [26] обнаружили, что применение макролидов ассоциировалось со значительным изменением скорректированного интервала QT. В данном исследовании не изучалась длительность интервала QT, а вместо этого непосредственно анализировался риск развития клинически значимых желудочковых аритмий. Авторы показали независимую ассоциацию применения гидроксихлорохина или хлорохина с развитием желудочковых аритмий de novo. Авторы продемонстрировали наличие независимой связи между применением гидроксихлорохина или хлорохина и возникновением желудочковых аритмий de novo. Авторы также отметили, что опасность возникновения желудочковых аритмий de novo повышалась при применении этих препаратов в комбинации с макролидом.
В данном анализе по количеству превалировали пациенты из Северной Америки, авторы отметили, что более высокий ИМТ стал маркером риска снижения выживаемости в стационаре. Известно, что ожирение является фактором риска развития сердечных аритмий и внезапной сердечной смерти [27,28]. Среди всех видов аритмий наиболее часто регистрировались фибрилляция предсердий и желудочковая тахикардия. Хотя возраст, этническая принадлежность и ИМТ являются предикторами повышенного риска смерти при COVID-19 в данном анализе, они не были связаны с повышением риска желудочковых аритмий при многофакторном регрессионном анализе. Единственными переменными, независимо предсказывающими развитие желудочковых аритмий, были четыре вышеописанные схемы лечения, а также наличие сердечно-сосудистых заболеваний и ХОБЛ. Таким образом, сердечно-сосудистая коморбидность в исследуемой популяции может частично объяснить наблюдаемый риск повышения токсического эффекта в отношении сердечно-сосудистой системы при применении хлорохина или гидроксихлорохина, особенно в комбинации с макролидами. В данном исследовании, результаты которого согласуются с предыдущими выводами авторов на меньшей когорте из 8910 пациентов [20], было обнаружено, что женщины и пациенты, получавшие ингибиторы АПФ (но не блокаторы рецепторов ангиотензина) или статины, имели более низкую летальность при COVID-19. Эти результаты дают основание предполагать, что препараты, стабилизирующие сердечно-сосудистую функцию и снижающие дисфункцию эндотелиальных клеток, могут улучшить прогноз, независимо от использования кардиотоксических комбинаций препаратов [21].
Данное исследование имеет несколько ограничений. К связи сниженной выживаемости со схемами лечения гидроксихлорохином или хлорохином следует относиться с определенной долей настороженности. Из-за дизайна обсервационного исследования авторы не могут исключить возможность наличия неизмеряемых сопутствующих факторов, хотя они обнадеживающе отметили согласованность между результатами первичного анализа и соответствующими данными по шкале предрасположенности. Тем не менее, нельзя утверждать однозначно наличие причинно-следственной связи между лекарственной терапией и выживаемостью. Эти данные не относятся к применению какой-либо схемы лечения, используемой в амбулаторных условиях. Прежде чем можно будет прийти к точному заключению относительно пользы или вреда этих препаратов у пациентов с COVID-19, потребуются дальнейшие рандомизированные клинические испытания. Авторы также отмечают, что хотя они и оценивали связь схем медикаментозного лечения с развитием желудочковых аритмий, они не измеряли интервалы QT и не стратифицировали картину аритмии (например, torsade de pointes). Авторы также не установили, связано ли повышение риска внутрибольничной смерти при использовании данных схем приема лекарственных препаратов непосредственно с их токсическим действием на сердечно-сосудистую систему; также не был проведен анализ рисков в зависимости от дозы препарата. Даже если все эти ограничения предполагают довольно консервативную интерпретацию полученных результатов, авторы считают, что отсутствие какой-либо наблюдаемой пользы все же может представлять собой разумное объяснение.
Таким образом, это многонациональное обсервационное исследование госпитализированных пациентов с COVID-19 показало, что использование схемы, содержащей гидроксихлорохин или хлорохин (совместно с макролидом или без него), не связано с какими-либо доказательными преимуществами, а напротив ассоциировано с увеличением риска развития желудочковых аритмий и большей опасностью внутригоспитальной смерти. Эти результаты свидетельствуют о том, что данные схемы лечения не должны использоваться вне клинических испытаний, и требуется срочное подтверждение их безопасности и эффективности посредством проведения рандомизированных клинических исследований.
Участники проекта
Исследование было создано и разработано авторами MRM и ANP. Сбор данных и их статистический анализ выполнялись и контролировались SSD. МРМ подготовил проект черновика, и все авторы приняли участие в критической доработке интеллектуального содержания статьи. МРМ и ANP руководили исследованием. Все авторы одобрили окончательную версию статьи и несут ответственность за принятие решения о ее публикации.
Декларация интересов
МРМ передает информацию о личных сборах от компаний Abbott, Medtronic, Janssen, Mesoblast, Portola, Bayer, Baim Institute for Clinical Research, NupulseCV, FineHeart, Leviticus, Roivant и Triple Gene. SSD является основателем корпорации Surgisphere Corporation. Автору FR был заплачено за работу в качестве члена комитета по клиническим испытаниям, за консультативные советы, другие формы консультирования и лекции; эти платежи были переведены непосредственно в Цюрихский университет, и никакие личные платежи не были получены за эти исследования или другую деятельность. ANP не декларирует никаких конкурирующих интересов.
Благодарности
Разработка и ведение совместной базы данных Тhe Surgical Outcomes Collaborative финансировалась корпорацией Surgisphere Corporation (Чикаго, Иллинойс, США). Это исследование было поддержано Тhe William Harvey Distinguished Chair в области передовой сердечно-сосудистой медицины в Brigham and Women’s Hospital (Бостон, Массачусетс, США). Авторы благодарят Jide Olayinka (Surgisphere) за полезный статистический обзор работы.
