Двигательные расстройства при паранеопластических и аутоиммунных заболеваниях

Множество двигательных расстройств, которые первоначально рассматривались как идиопатические или дегенеративные, со временем приобрели статус иммуноопосредованных. Некоторые из них были отнесены к группе паранеопластических синдромов: хорея, ассоциированная с анти-CV2/CRMP-5-антителами, анти-Ma2-ассоциированные гипокинезия и ригидность, анти-Yo мозжечковые атаксия и тремор, анти-Hu атаксия и псевдоатетоз. Другие заболевания, такие как ревматическая хорея (хорея Сиденгама), хорея при системной красной волчанке (СКВ) и антифосфолипидном синдроме (АФС), связаны с выработкой множества аутоантител, которые не являются паранеопластическими, а активируются вследствие молекулярной мимикрии либо с помощью иных механизмов развития иммунной аутоагрессии.
Введение
Иммуноопосредованные двигательные нарушения могут возникать в ходе паранеопластических или аутоиммунных процессов. Известно, что классические паранеопластические синдромы, а также СКВ и АФС могут приводить к двигательным аномалиям, однако в последнее время возникает новая расширяющаяся группа синдромов, связанных с образованием антител к белкам клеточной поверхности или синаптическим белкам, что приводит к заметным моторным нарушениям. Эти расстройства могут быть паранеопластическими, а могут и не являться таковыми. К ним относят: анти-NMDA-рецепторный энцефалит (вызванный образованием антител к NMDA), синдром «ригидного человека» (антитела к глутаматдекарбоксилазе, амфифизину, ГАМКА-рецептор-ассоциированному белку или рецептору глицина), нейромиотонию (антитела к CASPR-2), синдром опсоклонуса-миоклонуса-атаксии (антитела часто не выявляются) и др. В этом обзоре основное внимание уделяется всем этим расстройствам с упором на клинико-иммунологические ассоциации, новые антигены и основные стратегии лечения.
Паранеопластические неврологические заболевания обычно обнаруживают до распознавания самой опухоли, часто их проявление способствует диагностике онкопатологии (табл. 1). В данном случае симптомы прогрессируют быстрее, чем при невоспалительных дегенеративных заболеваниях; важным диагностическим критерием является наличие воспалительных изменений в цереброспинальной жидкости (ЦСЖ) на протяжении всего заболевания. На ранних стадиях множества иммуноопосредованных двигательных расстройств в ЦСЖ наблюдается лимфатический плеоцитоз, также возможно увеличение количества белка, IgG, частые олигоклональные полосы. Наиболее специфичные находки — антинейрональные антитела. Их наличие показывает, что синдром является иммуноопосредованным; в зависимости от вида антител определяется вероятность наличия ассоциированного новообразования и его тип [1, 2].
Таблица 1 | Клинико-лабораторные характеристики паранеопластических и аутоиммунных двигательных синдромов [1, 2]
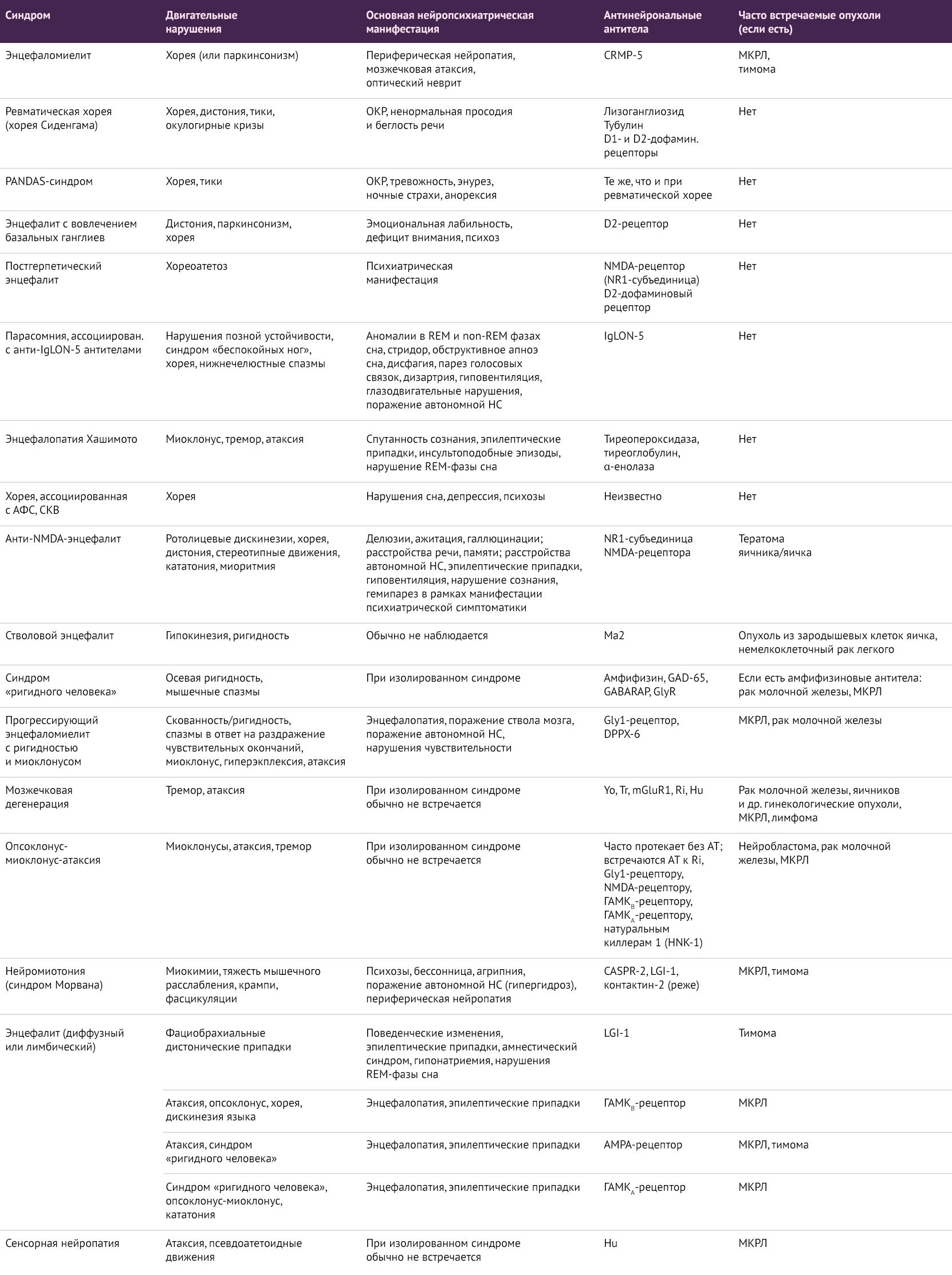
Далее рассмотрим более подробно конкретные примеры паранеопластических и аутоиммунных заболеваний, ассоциированных с развитием двигательных нарушений.
Паранеопластическая хорея, вызванная образованием CRMP-5-антител
Хорея, ассоциированная с антителами к CRMP-5, почти всегда паранеопластическая. Хореиформные движения обычно выявляются в рамках более распространенных повреждений нервной системы, которые могут включать лимбический энцефалит, мозжечковую атаксию, периферическую нейропатию, увеит, оптический неврит, ретинит.
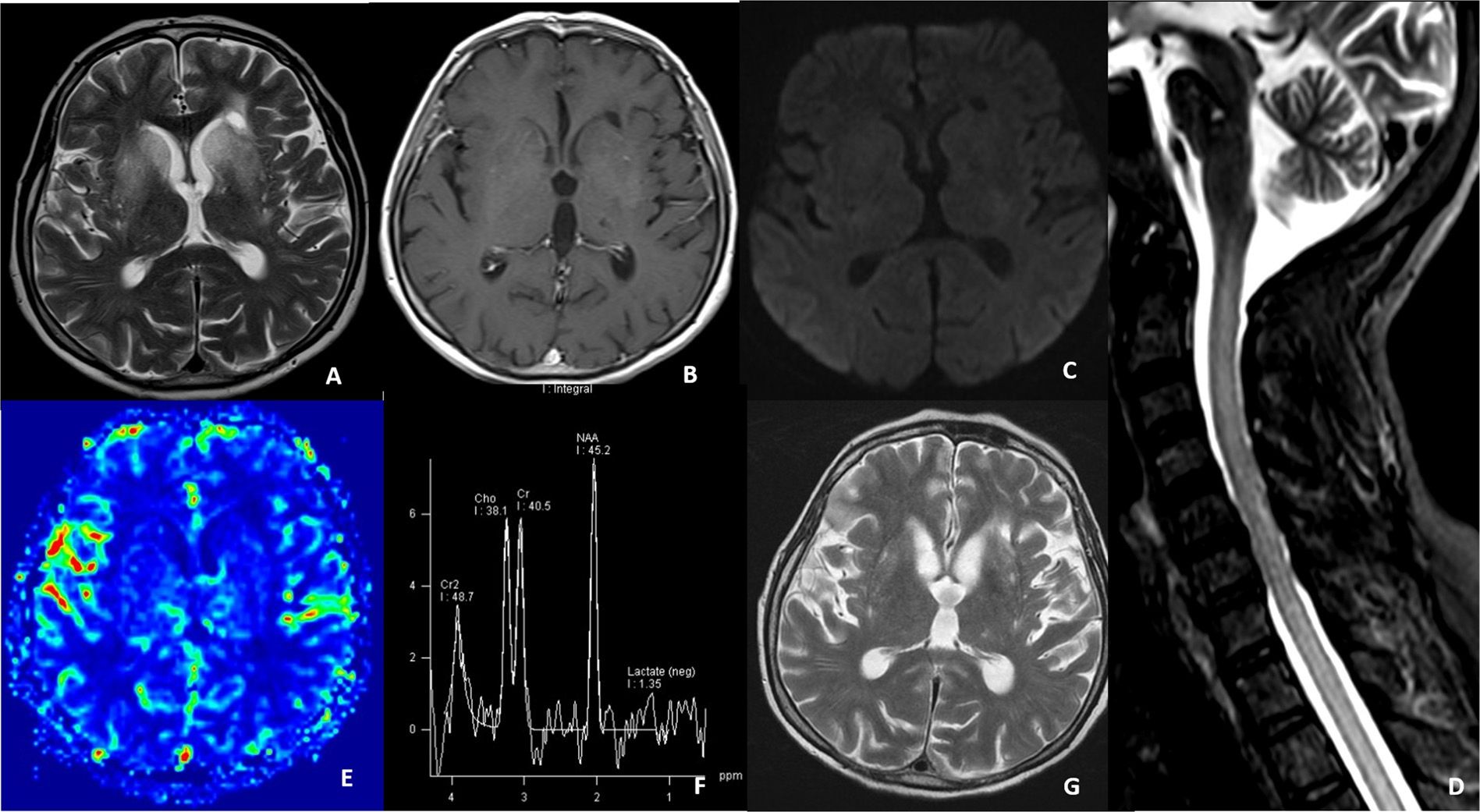
МРТ головного мозга в режиме FLAIR демонстрирует гиперинтенсивность структур лимбической системы, стриатума, базальных ганглиев, ствола мозга, а также белого вещества. В качестве первопричины данного состояния чаще всего выделяют МКРЛ и тимому. Для лечения используются хирургические методы, а также иммунотерапия, направленная на вовлеченные в патологический процесс T-клеточные механизмы. Средняя выживаемость среди пациентов с МКРЛ и анти-CRMP-5 паранеопластическим энцефалитом выше, чем у пациентов с раком легкого и анти-Hu энцефалитом.
Пример визуализации при паранеопластическом синдроме, ассоциированном с CRMP-5-антителами, представлен на рис. 1 [3].
Хорея Сиденгама
Хорея Сиденгама является результатом аутоиммунного ответа, сопровождающего инфекционные заболевания, вызываемые БГСА. Хорея Сиденгама — по-прежнему самая распространенная хорея в педиатрической практике, хотя в последнее время в развитых странах ее частота значительно снизилась. Это заболевание может развиваться в течение часов или дней, а может манифестировать и через несколько месяцев после инфицирования БГСА; процесс может быть односторонним. Сопутствующие симптомы включают тревогу, навязчивые идеи, компульсии, снижение внимания и паранойю. У пациентов наблюдаются скудость речи, дизартрия, гипомимия, тики и дистония. Двигательные проявления в литературе описываются как «хватка доярки» и «стремительный язык».
МРТ головного мозга обычно не демонстрирует патологических изменений, хотя возможно небольшое увеличение базальных ганглиев и гиперинтенсивность в режимах FLAIR и T2. Пациенты должны быть обследованы на наличие других проявлений ревматической лихорадки, включая шумы сердца, артриты и специфические аномалии на ЭКГ или ЭхоКГ. Выявляются антистрептолизин О (АСО) и антитела к ДНКазе В, однако корреляция между титрами антител и тяжестью заболевания или количеством курсов лечения не обнаружена. У большинства детей с хореей Сиденгама идентифицируются антитела к базальным ганглиям, но они также могут присутствовать и при болезнях Гентингтона и Паркинсона, а также в норме у здоровых людей. При хорее Сиденгама вырабатываются антитела к нейрональному тубулину в результате перекрестной реакции с мембранными белками БГСА. Более того, некоторые поверхностные антигены БГСА (M-белок и N-ацетил-D-глюкозамин) могут спровоцировать аутоиммунную активность, направленную на клетки нервной системы.
Профилактика пенициллинами предотвращает обострения хореи при повторном инфицировании БГСА и снижает риск развития ревматической болезни сердца. Симптомы заболевания обычно разрешаются за 3–4 месяца, но у некоторых пациентов могут персистировать годами. Примерно у половины пациентов случаются рецидивы, которые могут состояться, в частности, во время беременности («хорея беременных»). В случаях тяжелых или длительно текущих симптомов может быть применена иммунная терапия, включающая кортикостероиды, внутривенное введение иммуноглобулинов или плазмаферез. В качестве симптоматической терапии часто применяют бензодиазепины, вальпроевую кислоту или нейролептики.
Хорея, ассоциированная с АФС и СКВ
АФС проявляется артериальными или венозными тромбозами с персистенцией антифосфолипидных антител (таких как волчаночный антикоагулянт, антитела к кардиолипину и к бета-2-гликопротеиду). АФС и СКВ могут вызывать широкий спектр неврологических симптомов, включая хорею. По статистике, хорея наблюдается у 2 % пациентов с СКВ; в некоторых случаях СКВ манифестирует именно хореей. Последняя чаще проявляется у женщин, она также может быть спровоцирована беременностью. Патофизиология АФС- или СКВ-индуцированной хореи точно не известна. Можно лишь сказать, что ишемическая этиология маловероятна, учитывая отсутствие изменений на МРТ в базальных ганглиях и «восковую», ослабевающую природу хореи (дело в том, что флуктуация экстрапирамидной симптоматики в течение дня обычно не характерна для заболеваний сосудистого генеза). Антифосфолипидные антитела связываются с богатыми фосфолипидами зонами базальных ганглиев и могут привести к нейрональному повреждению; также они способны непосредственно деполяризовывать нейроны.
У пациентов с психиатрической симптоматикой СКВ обнаруживаются многие антитела, специфичные к нейронам, включая антитела к ганглиозидам, нейрофиламентам, NR2-субъединице NMDA-рецепторов; белкам, ассоциированным с микротрубочками 2, триозофосфатизомеразой, рибосомальным P-протеином и глиальным фибриллярным кислым белком. Являются ли эти антитела патогенными, пока неясно.
Несмотря на то, что СКФ и АФС ассоциированы с тромбозами, нет данных об эффективности терапии антикоагулянтами у пациентов с хореей. Чаще всего помогают иммунотерапия и симптоматическое лечение.
Энцефалит с вовлечением базальных ганглиев
При этом заболевании часто отмечается вовлечение в патологический процесс таламуса; собственно, поэтому его полное название звучит так: энцефалит с вовлечением таламуса и/или базальных ганглиев. Заболевание поражает в основном детей и молодых взрослых. Энцефалит часто развивается после инфекционных заболеваний (чаще всего после респираторных вирусных инфекций, реже — в результате инфицирования возбудителем туберкулеза, герпес-вирусами, в исходе болезни Крейтцфельда-Якоба), также может (в редких случаях) возникнуть и в рамках генетического, аутоиммунного или паранеопластического заболевания, а также ишемического инсульта [4].
Лимбический энцефалит
Паранеопластический лимбический энцефалит (ПЛЭ) является редким неврологическим синдромом, который избирательно поражает структуры лимбической системы, включая гиппокамп, гипоталамус и миндалевидное тело (рис. 2). Среди симптомов часто проявляются когнитивные расстройства, изменение личности, нарушение кратковременной памяти и судороги. Классический лимбический энцефалит с судорогами из височной доли вызывается онконейрональными антителами к внутриклеточным антигенам, включая анти-Hu2, анти-Ma2, анти-амфифизин и анти-CRMP-5. Пациенты, у которых вышеназванные антитела не обнаруживаются, могут давать положительный результат на аутоантитела к нейрональным внеклеточным эпитопам, таким как комплекс потенциал-управляемых калиевых каналов (VGKC), N-метил-D-аспартатный рецептор (NMDAR), рецептор α-амино-3-гидрокси-5-этил-4-изоксазолпропионовой кислоты (AMPAR) и B-рецептор γ-аминомасляной кислоты (GABABR).
ПЛЭ чаще всего ассоциируется с раком легкого (примерно половина случаев ПЛЭ), в 80 % случаев это МКРЛ.
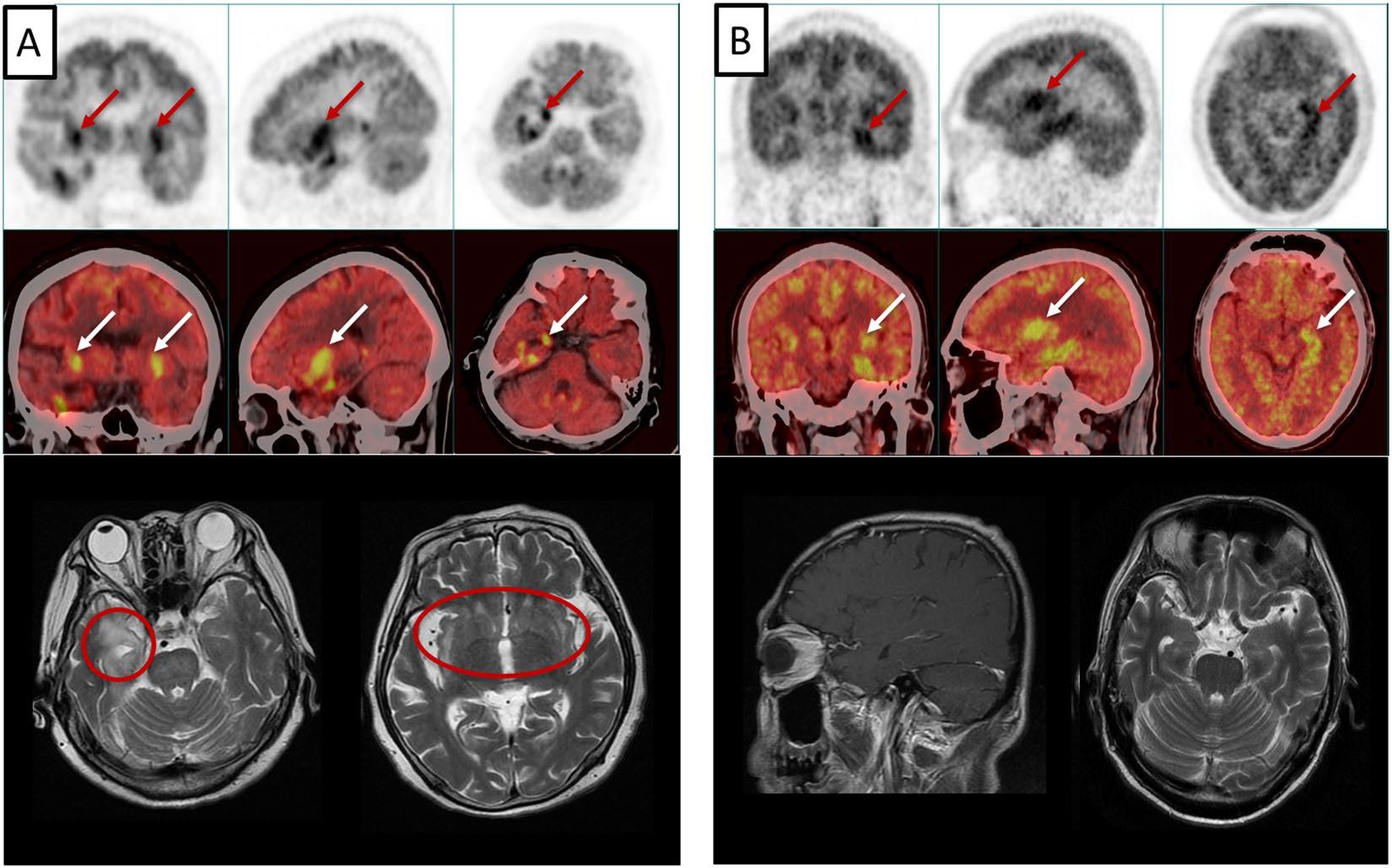
B: 54-летний мужчина, ПЭТ-КТ демонстрирует повышение метаболизма в левой височной доле (показано стрелками), тогда как на МРТ патологии не выявляется [5].
Дискинезии и двигательные нарушения при анти-NMDA энцефалите
Первоначально это заболевание выявляли только у молодых женщин с тератомой яичника; теперь же ясно, что оно сопутствует всем демографическим группам и считается наиболее распространенным иммуноопосредованным энцефалитом. Обычно все начинается с изменений личности, а также расстройств настроения и поведения, напоминающих острый психоз. Затем развиваются судороги, нарушается сознание, появляются дискинезии, жар, вегетативная дисфункция, гиповентиляция. У некоторых пациентов заболевание может продолжиться неконвульсивным эпилептическим статусом или дебютировать с него. Пациентам часто необходима интенсивная терапия, в том числе искусственная вентиляция легких.
Дискинезии наблюдаются у 80 % пациентов; они вовлекают лицо, тело, живот и конечности, особенно заметными являются ротощекоязычные дискинезии. Также наблюдаются хорея, баллизм или опистотонические позы. Избыточные движения могут чередоваться с периодами кататонии, каталепсии, дистонии и ригидности. Сочетание полуритмичных и дискинетичных движений с моторными приступами может привести либо к гиподиагностике судорог, либо к ненужной эскалации назначения противоэпилептических препаратов при отсутствии эпилептических симптомов.
Антитела к NR1-субъединице NMDA-рецептора вызывают интернализацию и снижение межсинаптической глутаматергической нейротрансмиссии. Почти половину пациентов составляют дети. Около 50 % взрослых женщин из числа пациентов имеют тератому яичника, у девочек-подростков она выявляется примерно в трети случаев. Опухоль редко выявляется у девочек до 14 лет, мальчиков и взрослых мужчин.
В 50 % случаев на МРТ головного мозга не выявляется никаких особенностей. Самые частые находки включают слабую гиперинтенсивность в режимах Т2 и FLAIR в гиппокампе, мозжечке, коре мозга, субкортикальных зонах, базальных ганглиях или стволе мозга. На ЭЭГ обнаруживается медленная дезорганизованная активность. В фазе кататонии преобладает ритмичная δ-θ активность, иногда с электрографическими компонентами судорог. Дифференциальную диагностику следует проводить с вирусным энцефалитом, злокачественным нейролептическим синдромом, летаргическим энцефалитом, поздним аутизмом и детским дезинтегративным расстройством.
Лечение состоит в элиминации опухоли и иммунотерапии, которая обычно проводится кортикостероидами, внутривенным введением иммуноглобулинов или плазмаферезом. У 75 % пациентов наблюдается полное или частичное неврологическое восстановление. Пациентов, рефрактерных к вышеназванным препаратам, можно вести на циклофосфамиде или ритуксимабе. Рецидив возможен в четверти случаев, в особенности в отсутствие опухоли или у пациентов, получавших недостаточно оптимальную иммунотерапию. Симптомы могут снова проявиться через месяцы или даже годы после первоначального восстановления.
Для более простого запоминания симптоматики анти-NMDA-энцефалита существует мнемоническое правило: «SEARCH For NMDAR-A», где:
- S — sleep dysfunction — тяжелая бессонница, которая в начале заболевания встречается куда чаще, чем гиперсомния, однако последняя превалирует в фазе ремиссии заболевания (вероятность возвращения симптоматики после лечения составляет в среднем 12 %); иногда она ассоциирована с гиперфагией и гиперсексуальностью;
- E — excitement — возбуждение, растормаживание или маниакальное поведение, чередующееся с депрессией, гиперсексуальностью, также возможно бродяжничество; депрессии и суицидальные наклонности проявляются реже;
- A — agitation — ажитация или агрессия. Проявляется с одинаковой частотой как у взрослых, так и у детей (у последних возможны истерики);
- R — rapid onset — острое начало. Симптомы развиваются в течение дней или недель; психиатрические заболевания, напротив, чаще всего развиваются медленно. Кроме того, их началу обычно предшествуют изменения в поведении (как в случае острого психоза);
- C — children and young adult predominance — к заболеванию наиболее предрасположены дети и молодые взрослые (средний возраст начала составляет 21 год). Соотношение женщин и мужчин 8:2. Напротив, в случае шизофрении средний возраст начала у мужчин составляет 18–25 лет, у женщин — 25–35 лет (с пиком после менархе и после 40 лет), соотношение женщин и мужчин 0,92:1;
- H — history of psychiatric disease absent — отсутствие поведенческих изменений в анамнезе (со слов родственников пациента) обычно наводит на мысль об анти-NMDA-энцефалите;
- F — fluctuating catatonia — кататония может чередоваться с эпизодами выраженной ажитации;
- N — negative and positive symptoms at presentation — продуктивная (визуальные или слуховые галлюцинации; бред преследования, отношения, величия; религиозный бред; дезорганизованные мысли) и негативная симптоматика (когнитивный дефицит, апатия или ангедония). Обычно все эти симптомы проявляются в начале заболевания. При шизофрении же в начале заболевания продуктивная симптоматика встречается чаще негативной;
- M — memory deficit — нарушение запоминания, которое может быть обусловлено выраженной ажитацией, изменениями в поведении, проблемами с речью; большинство пациентов не могут после восстановления вспомнить длительный период своей болезни;
- D — decrease of verbal output and mutism — резкое снижение общительности, в частности, у детей; этому могут предшествовать эпизоды быстрой импульсивной речи;
- A — antipsychotic intolerance — непереносимость антипсихотиков (как типичных, так и атипичных). Частота побочных явлений в среднем выше при лечении типичными антипсихотиками;
- R — rule out neuroleptic malignant syndrome — исключить злокачественный нейролептический синдром, который характеризуется гипертермией, комой, мышечной ригидностью, высокой концентрацией креатинкиназы в сыворотке или рабдомиолизом. У пациентов, принимающих нейролептики, а также у лиц с доказанным психиатрическим заболеванием в анамнезе возможна гиподиагностика на предмет наличия злокачественного нейролептического синдрома;
- A — antibodies and additional paraclinical tests (EEG, MRI, CSF) — NMDAR-аутоантитела всегда проявляются в ликворе, 80 % пациентов имеют плеоцитоз [6].
Анти-Ma2 энцефалиты и гипокинезии
Это заболевание поражает лимбическую систему, средний мозг и верхнюю часть мозгового ствола. Заболевание может проявиться снижением кратковременной памяти, судорогами, гиперсомнией, нарколепсией-катаплексией, гипертермией, гиперфагией, гипоталамо-гипофизарной дисфункцией, паркинсонизмом, вертикальным парезом взора. Паркинсонизм включает брадикинезию, гипомимию, гипофонию, ригидность; тремор встречается реже. Также могут наблюдаться принудительное открывание и закрывание челюсти и окулогирный криз. Ствол мозга вовлекается постепенно в ростро-каудальном направлении, приводя к черепной нейропатии, горизонтальному офтальмопарезу, атаксии. Дифференциальную диагностику следует проводить с болезнью Уиппла и прогрессивным надъядерным параличом. На МРТ в режимах T2 и FLAIR часто обнаруживают гиперинтенсивность средневисочных долей, гипоталамуса, таламуса и верхней части ствола мозга, иногда с усилением накопления контрастного вещества.
При данном заболевании у мужчин старше 50 лет почти всегда имеется опухоль из зародышевых клеток яичка. Кроме того, у мужчин и женщин старше 50 лет возникают ассоциации с НМКРЛ, раком молочной железы и толстой кишки, лимфомой. Около 35 % пациентов выздоравливают в результате лечения опухоли и иммунотерапии. Паркинсонизм может купироваться карбидопой/леводопой, дистония лица же обычно уменьшается при использовании мышечных релаксантов и инъекций ботулотоксина.
Синдром мышечной скованности (СМС)
СМС может сопровождаться присутствием опухоли и соответствующих антител. Симптомы включают мышечную скованность, ригидность и болезненные спазмы, вызванные чувствительными или эмоциональными стимулами. Электрофизиологические исследования демонстрируют постоянную двигательную активность с одновременным вовлечением мышечных агонистов и антагонистов, которая смягчается приемом бензодиазепинов.
В 85 % случаев причина СМС остается идиопатической, пациенты обычно имеют антитела к GAD-65. GAD-65-антитела могут также выявляться у пациентов с мозжечковой атаксией и рефрактерной эпилепсией, которые отчасти напоминают СМС. В редких случаях у пациентов с СМС и антителами к GAD-65 обнаруживаются тимома или другие опухоли. Несмотря на то, что эти антитела ассоциированы с сахарным диабетом 1 типа, их обнаружение в ликворе специфично для неврологических заболеваний. Паранеопластическая форма СМС выявляется совместно с антителами к амфифизину; опухолями, часто вовлеченными в данный патологический процесс, являются МКРЛ и рак молочной железы. Паранеопластические случаи СМС чаще встречаются у пожилых пациентов, симптомы имеют асимметричный характер, с частым вовлечением шеи, спинальным миоклонусом и зудом.
GAD-65-антитела приводят к функциональному нарушению в ГАМК-ергических интернейронах серого вещества спинного мозга, тогда как антитела к амфифизину способствуют снижению ГАМК-ергического торможения. Другие антитела направлены против ГАМКА-рецептор-ассоциированного белка (GABAARAP); 70 % пациентов с СМС и GAD-65-антителами также имеют GABAARAP-антитела, что вызывает сложный вопрос: какие же антитела являются патогенными?
Некоторые пациенты с прогрессивным энцефаломиелитом, ригидностью и миоклонусом, то есть заболеваниями, входящими в спектр СМС, имеют антитела к α1-субъединице глицинового рецептора.
Терапия СМС включает лечение опухоли и применение кортикостероидов. Для лечения непаранеопластической формы заболевания успешно применяется внутривенное введение иммуноглобулинов, что, впрочем, не имеет доказательной базы в случае паранеопластических состояний. Симптоматическая терапия включает средства, повышающие ГАМК-ергическую трансмиссию (диазепам, баклофен, вальпроат натрия, тиагабин, вигабатрин).
Паранеопластическая мозжечковая дегенерация и тремор
Заболевание обычно манифестирует с головокружения, далее остро развиваются атаксия, дизартрия, бьющий вниз нистагм и тремор. В педиатрической практике паранеопластическая мозжечковая дегенерация может протекать под маской постинфекционного церебеллита. Почти все известные на сегодняшний день паранеопластические антитела могут быть ассоциированы с развитием мозжечковой атаксии, однако в патогенезе заболевания отчетливо доминируют три вида антител: анти-Yo (антитела к клеткам Пуркинье 1) у пациенток с раком молочной железы или яичников, анти-Tr у пациентов с лимфомой Ходжкина и антитела к потенциал-зависимым кальциевым каналам (VGCCs) у пациентов с МКРЛ. Идиопатические VGCC-антитела могут выявляться и в некоторых случаях спорадической мозжечковой атаксии, которая ранее рассматривалась как дегенеративная.
Антитела к метаботропному глутаматному рецептору I типа (mGluR1) находят у некоторых пациентов с идиопатической или паранеопластической мозжечковой атаксией, ассоциированной с лимфомой Ходжкина.
Лечение данного заболевания представляет собой сложную задачу, так как иммунотерапия эффективна только у пациентов с анти-Tr и антителами к mGluR; большинство же пациентов с паранеопластической мозжечковой дегенерацией к ней рефрактерны.
Синдром опсоклонус-миоклонус-атаксии (СОМА)
Опсоклонус представляет собой череду непроизвольных, аритмичных, хаотично направленных саккад без межсаккадного промежутка. СОМА может быть постинфекционным или паранеопластическим. У половины детей с СОМА диагностируют нейробластому. Во взрослом возрасте к числу ассоциированных опухолей относятся МКРЛ, а также рак молочной железы или яичников. У подавляющего большинства пациентов паранеопластические антитела не выявляются, хотя небольшая группа пациенток с раком молочной железы или яичников может иметь анти-Ri-антитела. Некоторые педиатрические пациенты имеют антитела против клеточной поверхности гранулярных нейронов мозжечка и клеточных рядов нейробластомы. Проточная цитометрия ЦСЖ показывает B-клеточную экспансию, выраженность которой коррелирует с лечением заболевания.
Лечение детей с СОМА включает резекцию нейробластомы, если таковая присутствует, а также иммунотерапию (кортикостероиды, АКТГ, ритуксимаб, циклофосфамид, внутривенное введение иммуноглобулинов). В результате глазодвигательные нарушения часто смягчаются или исчезают совсем, но у пациентов зачастую остаются моторные, речевые и поведенческие нарушения, а также расстройства сна. Нередко возникают рецидивы, особенно при интеркуррентных заболеваниях или в результате недостаточной иммунотерапии. Применение кортикостероидов или внутривенное введение иммуноглобулинов может ускорить выздоровление у взрослых пациентов в случаях идиопатического заболевания, но при паранеопластическом СОМА иммунотерапия эффективна только после элиминации опухоли.
Приобретенная нейромиотония, синдром гиперактивности моторных волокон, синдром Исаакса
Пациенты с этим заболеванием испытывают крампи (мышечные судороги в икроножных мышцах) и мышечную скованность, а также подергивания (фасцикуляции или миокимии), псевдомиотонию (замедленное мышечное расслабление) и спазмы кистей или стоп. На электромиограмме выявляются фибрилляции, фасцикуляции и двойные или множественные одиночные высокочастотные разряды. Некоторые пациенты отмечают парестезии, спутанность сознания, перемены настроения, а также синдром Морвана (включает в себя нейромиотонию, боль, гипергидроз, потерю массы тела, нарушения сна и галлюцинации — прим ред.). В качестве этиологического фактора у некоторого числа пациентов встречаются тимома, МКРЛ, реже — другие опухоли. Синдром гиперактивности моторных волокон обычно встречается у людей старшего возраста, при этом в большей степени выражены слабость и миокимия, а в меньшей — крампи, дизавтономия; изредка может вовлекаться центральная нервная система.
Синдром Исаакса может протекать в рамках аутоиммунного заболевания. Описан случай нейромиотонии Исаакса с антителами к VGKC, CASPR-2, LGI-1 в сочетании с псориазом. Пациенты с аутоантителами к CASPR-2 и LGI-1 часто имеют и другие аутоиммунные заболевания, что дает основания предполагать общий аутоиммунный патогенез [7].
CASPR-2 признаны фактором развития нескольких заболеваний, которые ранее считались проявлением выработки аутоантител к потенциал-зависимым калиевым каналам, включая синдром гиперактивности моторных волокон, синдром Морвана и энцефалит. Однако у многих пациентов антитела не обнаруживаются. Лечение синдрома гиперактивности мышечных волокон включает терапию новообразований, когда это возможно, а также плазмаферез и симптоматическую терапию фенитоином или карбамазепином.
Парасомния, ассоциированная с анти-IgLON-5 антителами
Это заболевание характеризуется нарушением REM и non-REM фаз сна с сопутствующими дыхательными расстройствами (апноэ сна). Заболевание чаще имеет хроническое течение, с динамикой от среднетяжелой до тяжелой; симптомы гетерогенны — бульбарные (дизартрия, дисфагия, сиалорея, острая дыхательная недостаточность), двигательные (постуральная неустойчивость, скованность, дистония, хорея), окуломоторные расстройства (нистагм, паралич взора, замедленные саккады следящих движений глаз), когнитивные нарушения и автономная дисфункция (ортостатическая дисрегуляция, сексуальная дисфункция, брадикардия, гипергидроз).
Функциональная диагностика, как правило, малоинформативна; МРТ, ЭНМГ, ЭЭГ у большинства пациентов не демонстрируют каких-либо специфичных для данной патологии изменений. Основным методом, позволяющим точно установить диагноз, является выявление аутоантител IgLON-5 в ЦСЖ и/или сыворотке крови [8].
Сенсорная нейропатия и псевдоатетоз
Это заболевание вызвано дегенерацией нейронов ганглиев задних корешков спинного мозга, опосредованной T-клеточным иммунным ответом. При этом нарушаются все виды чувствительности, что сопровождается нейропатической болью и арефлексией. В результате чувствительного дефицита появляются атаксия, дистония или псевдоатетоидные движения конечностей. В качестве этиологического фактора чаще всего встречается МКРЛ, при котором вырабатываются анти-Hu антитела. Заболевание тяжело поддается лечению, возможна лишь стабилизация состояния пациентов или его небольшое улучшение в результате элиминации опухоли и проведения иммунотерапии.
Важно научиться отличать атетоз от псевдоатетоза, для этого рассмотрим следующий показательный клинический случай.
40-летний мужчина в течение трех недель испытывает парестезии и неспособность контролировать верхние конечности. В ходе физикального обследования были выявлены генерализованная арефлексия, нарушение проприоцепции, потеря чувствительности по типу «перчаток» и «носков» при сохранной мышечной силе. Также обратило на себя внимание то, что пациент широко ставил шаг при походке. Наблюдалась дисметрия всех четырех конечностей. Проба Ромберга положительна. При вытягивании рук вперед наблюдались медленные непроизвольные извивающиеся движения пальцев, которые усилились при закрывании глаз. Также отмечались движения пальцев ног, но в меньшей степени. Эти движения как раз и обозначаются термином «псевдоатетоз». Он клинически неотличим от истинного атетоза, однако этиология у этих двух процессов разная: атетоз обусловлен структурными нарушениями в определенных областях мозга, поэтому проявления не усиливаются при закрывании глаз, а причиной псевдоатетоза является потеря проприоцепции, именно поэтому он усиливается при закрывании глаз ввиду потери зрительного контроля над движениями. Псевдоатетоз отмечается при поражениях спинного мозга, но чаще всего встречается при патологии центральной и периферической нервной системы. МРТ головного и спинного мозга, а также исследование ЦСЖ в данном клиническом случае не помогли поставить пациенту правильный диагноз. Первоначально подозрение пало на диагноз «идиопатическая сенсорная атаксическая невропатия», был назначен курс иммуноглобулинов внутривенно, клинического эффекта не наблюдалось. После этого пациенту вводили метилпреднизолон в течение пяти дней с последующим коротким курсом пероральных глюкокортикоидов, в результате отмечалось частичное восстановление в течение пяти месяцев после манифестации заболевания. В течение последующих 11 месяцев какой-либо динамики в неврологическом статусе не отмечалось [9].
Если подозревается паранеопластический синдром, первоначально необходимо обнаружить и вылечить опухолевое заболевание. Для этого большинству пациентов рутинно проводятся ФДГ-ПЭТ и КТ грудной клетки, брюшной полости и малого таза. В зависимости от возраста, пола, типа паранеопластического синдрома и наличия антинейрональных антител могут применяться и другие методы исследования. Если у пациента с классическими онконейрональными антителами не удается выявить первичную опухоль, необходимо провести повторный скрининг в течение ближайших 3–6 месяцев, а затем повторять его каждые шесть месяцев в течение четырех лет.
Иммунотерапия должна применяться у большинства пациентов с паранеопластическими неврологическими заболеваниями и прогрессирующими неврологическими болезнями в том же объеме, как и при идиопатических или постинфекционных синдромах. Заболевания, ассоциированные с внутриклеточными антигенами (Hu, CRMP-5, Yo, Ri), часто рефрактерны к терапии кортикостероидами, плазмаферезом, иммуноглобулинами внутривенно; хотя в литературе отмечается возможная эффективность ритуксимаба. Такие препараты, как циклофосфамид, действуют против цитотоксического T-клеточного иммунного ответа. Заболевания же, ассоциированные с антителами к поверхностным антигенам (например, NMDA и CASPR-2), в целом лучше отвечают на лечение, направленное на выведение циркулирующих аутоантител (плазмаферез, иммуноглобулины внутривенно). Однако стоит отметить, что эти мероприятия эффективны лишь на начальных стадиях; на поздних стадиях заболевания или при образовании большого количества аутоантител интратекально существенного улучшения не происходит. Таким пациентам необходима более агрессивная иммунотерапия ритуксимабом или циклофосфамидом при неэффективности терапии первой линии.
Итак, подведем небольшой промежуточный итог. Важно отметить, что в группе паранеопластических заболеваний чаще остальных двигательных расстройств встречается мозжечковая атаксия, ассоциированная с образованием множества аутоантител, в частности: ANNA-1 (анти-Hu), ANNA-2 (анти-Ri), PCA-1 (анти-Yo), PCA-2, PCA-Tr, ZIC-4. Вышеназванные антитела образно называют «горгонейрональными» (рис 3.), чаще всего в ассоциации с их образованием обнаруживается МКРЛ. Такие расстройства клинически протекают острее, чем аутоиммунная мозжечковая атаксия, дают слабый ответ на иммунотерапию и характеризуются худшим прогнозом.
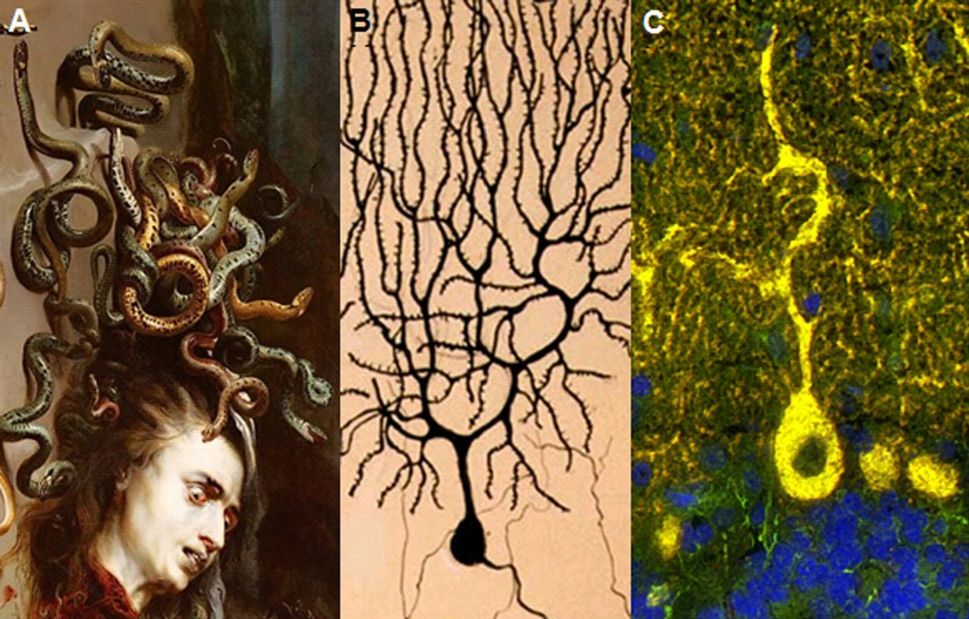
В. Изображение клетки Пуркинье — рисунок испанского патолога, гистолога, нейробиолога и лауреата Нобелевской премии Сантьяго Фелипе Рамон-и-Кахаля (1852–1934).
С. Тела и дендриты клеток Пуркинье, инфильтрированные IgG, у пациента с аутоиммунной мозжечковой атаксией [10].
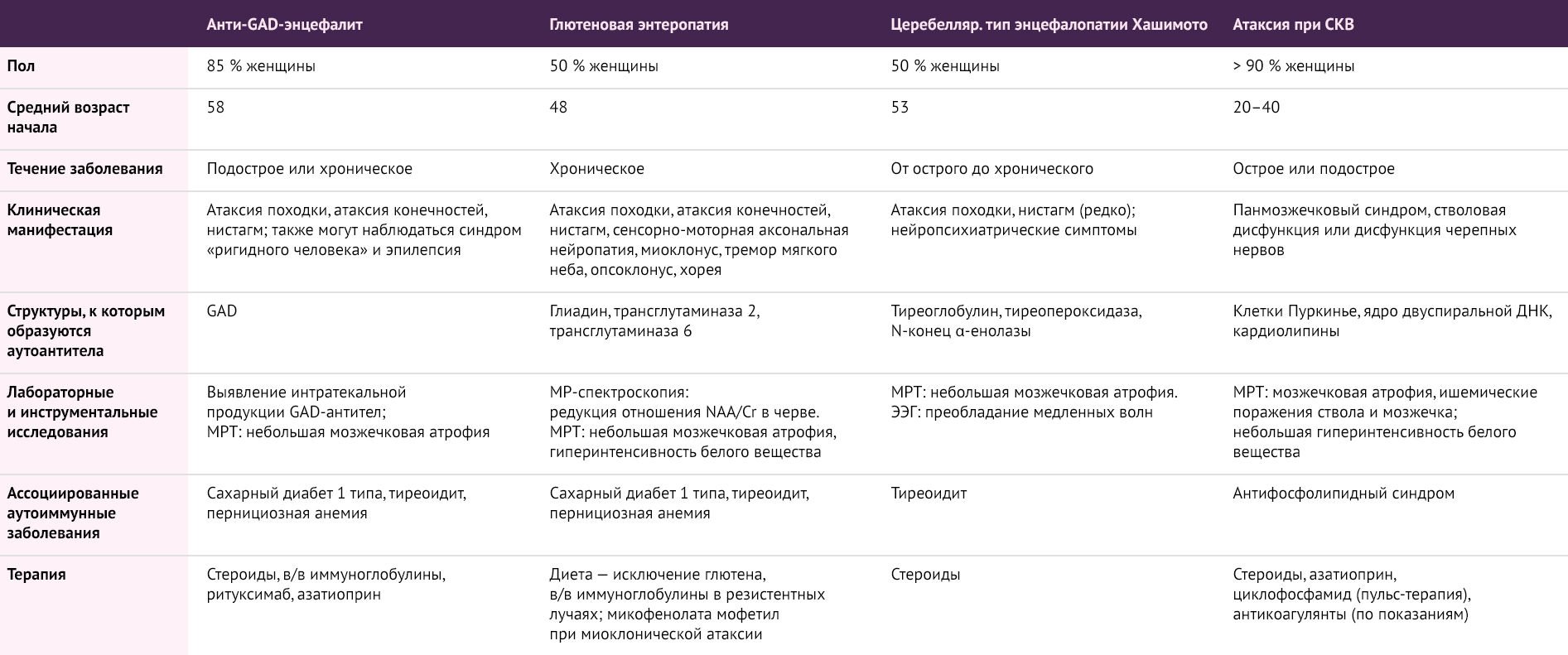
Некоторые важные аспекты дифференциальной диагностики мозжечковых атаксий при аутоиммунных заболеваниях обзорно представлены в таблице 2.
Таблица 2 | Дифференциальная диагностика мозжечковых атаксий при аутоиммунных заболеваниях
Паркинсонизм обычно отмечают при наличии Ma1/Ma2 аутоантител, в клинической картине иногда отмечается тяжелая гипокинезия. У пациентов с данными антителами развивается лимбический, диэнцефалический или стволовой энцефалит, чаще всего в сочетании с надъядерным параличом взора, со временем прогрессирующим до полной офтальмоплегии, расстройством REM фазы сна или нарколепсией. При наличии Ma1/Ma2 аутоантител чаще всего обнаруживают герминогенные опухоли.
Паранеопластическая хорея в большинстве случаев встречается у пациентов с ауто-CRMP-5-IgG, сопровождаемых аутоантителами ANNA-1. Кроме хореи, также возможно развитие полинейропатии и других гиперкинезов, таких как дистония и оробуккальные дискинезии. В данном случае преобладающей опухолью является МКРЛ.
Для синдрома «ригидного человека» характерно наличие антител к амфифизину, которые идентифицируются примерно у 5 % пациентов. В основном это женщины с раком молочной железы.
Ключевые положения
- Иммуноопосредованные двигательные расстройства могут быть паранеопластическими, постинфекционными или идиопатическими.
- Cимптомы прогрессируют гораздо быстрее, чем при невоспалительных нейродегенеративных синдромах. Клинически отмечается острое начало, сопровождающееся воспалительными изменениями в ЦСЖ, а также наличием антинейрональных аутоантител в крови и/или в ЦСЖ, что дает основания предполагать иммуноопосредованный механизм развития. Вероятность наличия ассоциированного новообразования и его тип определяются в зависимости от вида обнаруженных антител.
- Антитела к компонентам клеточной стенки или синаптическим белкам все чаще признаются причиной развития серьезных неврологических расстройств, которые могут возникать как в ассоциации с опухолями, так и вне ее.
- При подозрении на иммуноопосредованное двигательное расстройство необходимо провести исследование предполагаемых антинейрональных антител для подтверждения диагноза, а также определения вероятности и типа ассоциированного новообразования.
- Важно точное определение типа иммуноопосредованного двигательного расстройства, поскольку такие состояния способны реагировать на иммунотерапию; кроме того, их обнаружение может помочь в диагностике скрытого онкологического заболевания.
Источники:
- Jessica Panzer and Josep Dalmau. Movement disorders in paraneoplastic and autoimmune disease. Curr Opin Neurol. 2011 Aug; 24(4): 346–353. doi: 10.1097/WCO.0b013e328347b307
- José Fidel Baizabal-Carvallo, Joseph Jankovic. Autoimmune and paraneoplastic movement disorders: An update. Journal of the Neurological Sciences 385 (2018) 175–184.
- Nese Dericioglua, Rahsan Gocmen, Ersin Tana. Paraneoplastic striatal encephalitis and myelitis associated with anti-CV2/CRMP-5 antibodies in a patient with small cell lung cancer. Clinical Neurology and Neurosurgery 170 (2018) 117–119.
- G. C. Beattie, et al. Encephalitis With Thalamic and Basal Ganglia Abnormalities: Etiologies, Neuroimaging, and Potential Role of Respiratory Viruses. Clinical Infectious Diseases 2013;56(6):825–32. DOI: 10.1093/cid/cis990
- Kaini Shen, et al. Paraneoplastic limbic encephalitis associated with lung cancer. Sci Rep. 2018 May 1;8(1):6792. doi: 10.1038/s41598-018-25294-y.
- Josep Dalmau,et al. An update on anti-NMDA receptor encephalitis for neurologists and psychiatrists: mechanisms and models. Lancet Neurol 2019 Published Online July 17, 2019. http://dx.doi.org/10.1016/
- Qian M, Qin L, Guan H. A Case of Muscle Twitching With Psoriasis. JAMA Neurol. Published online July 15, 201976(9):1119–1120. doi:10.1001/jamaneurol.2019.1937
- Anna Heidbreder, MD, Konstanze Philipp, MD. Anti-IgLON 5 Disease. Curr Treat Options Neurol (2018). DOI 10.1007/s11940-018-0515-4.
- Yew Long Lo, Siewju See. Pseudoathetosis. The New England Journal of Medicine. December 10, 2014. 10.1056/NEJMicm0907786.
- S. Jarius and B. Wildemann. Medusa head ataxia’: the expanding spectrum of Purkinje cell antibodies in autoimmune cerebellar ataxia. Part 1: Anti-mGluR1, anti-Homer-3, anti-Sj/ITPR1 and anti-CARP VIII. Jarius and Wildemann Journal of Neuroinflammation (2015) 12:166. DOI 10.1186/s12974-015-0356-y.
