Молекулярные связи свидетельствуют о наследственной природе болезни Крона

Мутации гена NOD2 являются факторами риска болезни Крона. Многие аспекты того, как они влияют на состояние человека при данной болезни, неизвестны. Обнаружение вовлеченных в патогенез заболевания популяций клеток выдвигает новые терапевтические возможности.
Болезнь Крона — хроническое воспалительное заболевание кишечника, поражающее многих людей. Например, более 0,3 % населения Канады и Германии страдают от этого заболевания, а частота выявления случаев возрастает во всем мире [1]. Существует острая потребность в новых методах лечения, однако их эволюции препятствует отсутствие четкого понимания того, как возникает болезнь. Своей статьей в «Naturе» Nayar с соавт. [2] проливают свет на давнюю загадку одного фактора риска болезни Крона; выводы ученых имеют важное клиническое значение.
Болезнь Крона может поражать любой отдел кишечника. Чаще всего это подвздошная кишка, где развивается воспалительный процесс, который часто приводит к фиброзу (отложению волокнистой соединительной ткани как реакция на повреждение). Это приводит к сужению (стриктуре) просвета подвздошной кишки, что требует хирургического вмешательства [3]. Болезнь Крона представляет собой удобную для изучения модель, отображающую заболевания, развитие которых опосредовано комбинацией генетической предрасположенности и влияния окружающей среды. В данном случае, генетическая предрасположенность лежит в основе развития воспалительных реакций на воздействие микроорганизмов кишечника, что в итоге приводит к заболеванию.
Генетические вариации гена NOD2 (полиморфизм) являются самым сильным фактором риска болезни Крона; примерно 20 % от этого всего риска развития болезни связано с тремя однонуклеотидными полиморфизмами данного гена [4]. Кроме того, мутации NOD2 являются сильными прогностическими факторами для развития стриктур подвздошной кишки и, как следствие, необходимости хирургического вмешательства при болезни Крона. Это свидетельствует о сильной взаимосвязи между генетической основой этого состояния и проявлениями болезни [3].
Однако взаимосвязь гена NOD2 и восприимчивость к болезням представляют собой интересный парадокс. NOD2 — это внутриклеточный рецептор (см. рис. 1), который распознает молекулу мурамилдипептида (MDP) — распространенного компонента стенок бактериальных клеток. До того, как NOD2 был описан как ген риска развития болезни Крона, функция его была лучше всего изучена на примере иммунных клеток, обеспечивающих функционирование врожденного звена иммунитета. Активация NOD2 в этих клетках приводит к экспрессии воспалительных молекул, называемых цитокинами, а аномально интенсивный воспалительный ответ может опосредовать повреждение тканей кишечника при болезни Крона [5, 6]. Следовательно, можно предполагать, что мутации NOD2, известные как мутации, приводящие к потере функции (которые не приводят к образованию полноценного кодируемого геном белка), будут защищать от болезни Крона. Тем не менее, такие мутации NOD2, приводящие к потере функции, идентифицируются как факторы риска заболевания. Поэтому последующие исследования были сосредоточены на другом аспекте функции и метаболизма NOD2 в кишечнике — поддержании гомеостаза в кишечнике и роли NOD2 в этом процессе. Ведь именно здесь самая большая биомасса иммунокомпетентных клеток организма постоянно подвергается воздействию MDP кишечных микроорганизмов, а мутации NOD2 нарушают равновесие между микробиомом и иммунной системой, что ведет к болезни [5].
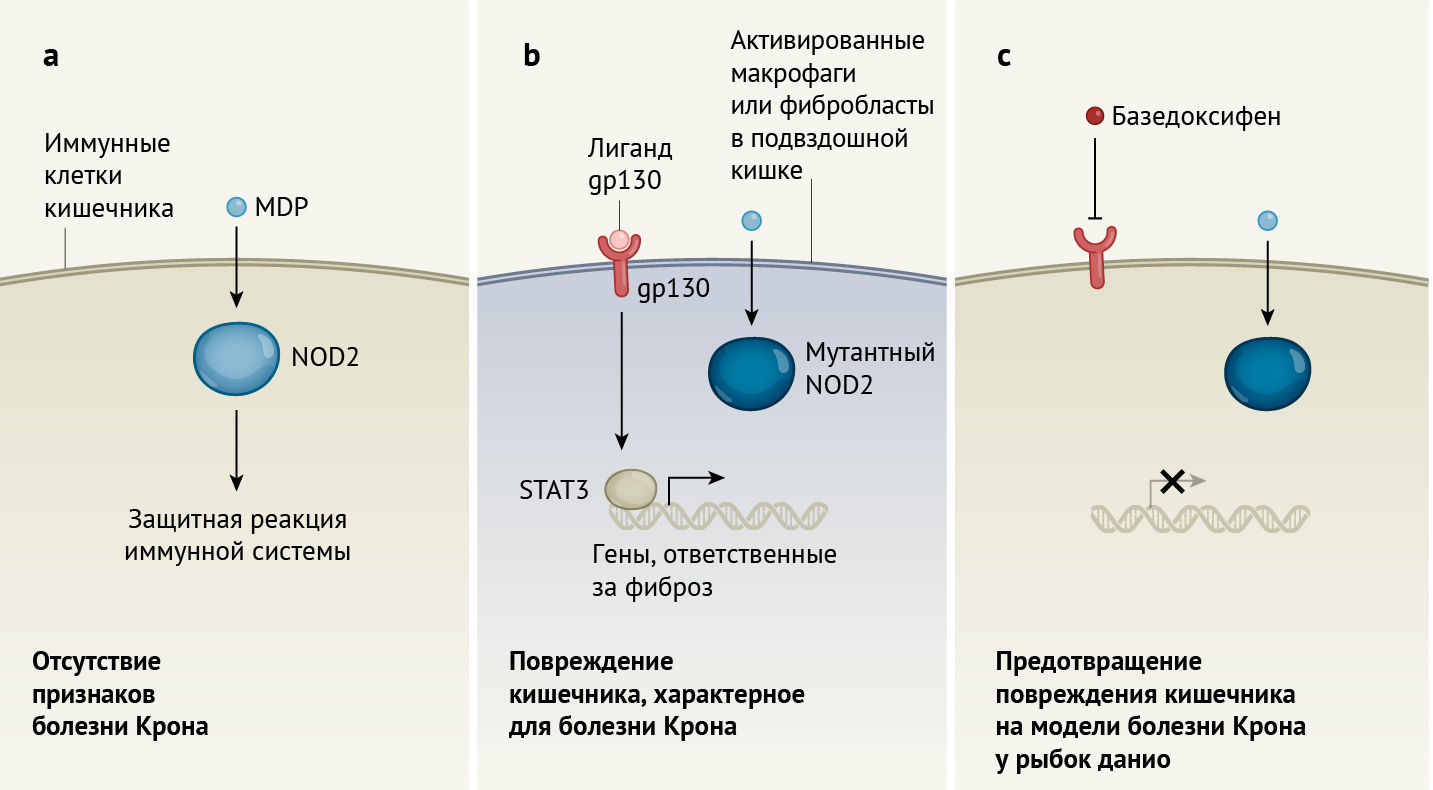
a. NOD2 — внутриклеточный белок, распознающий бактериальную молекулу мурамилдипептида (MDP), которая очень распространена в кишечнике. Это часть нормальной защитной реакции иммунных клеток для поддержания гомеостаза кишечника.
b. Мутации, приводящие к образованию нефункциональной версии NOD2, являются фактором риска болезни Крона [4]. Изучая рыбок данио и клинические образцы тканей кишечника человека, Nayar с соавт. [2] раскрывают детали процессов, связанных с мутантным NOD2, что лежит в основе данного заболевания. Авторы определяют популяции активированных иммунных клеток, называемых макрофагами и фибробластами, как ответственные за развитие фиброза, тканевой аномалии в подвздошной кишке, что возникает при болезни Крона. Связывание лиганда с рецептором gp130 этих иммунных клеток запускает путь экспрессии гена, опосредованный фактором транскрипции STAT3.
c. Согласно сообщению авторов, молекула ингибитора gp130, называемая базедоксифеном, предотвращает экспрессию гена, ведущую к повреждению кишечника (показано на модели болезни Крона — рыбках данио).
Роль мутаций NOD2 в возникновении фиброза подвздошной кишки до настоящего исследования была неизвестна. Авторы стремились понять, что запускает воспаление и фиброз при болезни Крона. Пытаясь обнаружить взаимосвязь между этими патологическими процессами и NOD2, они применили для исследования человеческие клетки, ткани кишечника человека и рыбок данио.
Во-первых, авторы использовали секвенирование РНК одиночных клеток, взятых из образцов воспаленной ткани подвздошной кишки во время операций у людей с болезнью Крона. В этих клетках обнаружилась сигнатура экспрессии генов, связанных с функциями активированных макрофагов и фибробластов. Авторам также удалось идентифицировать ключевую популяцию клеток, которая экспрессирует маркеры как миелоидных клеток, так и фибробластов. В соответствии с данными сведениями, популяция воспалительных макрофагов в подвздошной кишке дифференцируется для превращения в активированные фибробласты во время болезни.
Поразительно, но авторам удалось обнаружить факт эволюционной консервации этих клеточных популяций на экспериментальной модели воспаления тканей кишечника — на рыбках данио, обработанных декстраном сульфата натрия (DSS). Это вещество уже давно используется для индукции повреждения и воспаления кишечника на стандартных моделях грызунов. При моделировании воспалительных заболеваний кишечника человека in vivo предпочтение отдается именно мышиным моделям. Однако, как демонстрируют Nayar с соавт., рыбки данио представляют собой удобную альтернативу для исследований, от которых ожидается высокая степень результативности и быстрая оценка корреляции с заболеваниями человека. Действительно, кишечник рыбок данио и млекопитающих имеет сходную морфологию. Более того, как и у людей, у рыбок данио имеются звенья врожденного и адаптивного иммунитета, а воспаление тканей кишечника у рыбок данио также зависит от кишечного микробиома [7]. Методики редактирования генов, такие как CRISPR, помогают быстро модифицировать интересующие гены у рыбок данио.
Авторы изучили воспаление кишечника у рыбок данио, генетически модифицированных с дефицитом nod2. У этих рыб, обработанных DSS, было обнаружено повышенное содержание лейкоцитов в кишечнике, что является признаком воспаления, по сравнению с рыбками данио с нормальным количеством nod2. Но модель рыбок данио актуальна только в том случае, если можно найти корреляцию с организмом человека. Соответственно, используя сведения, полученные от детей с впервые диагностированной болезнью Крона, авторы демонстрируют, что увеличение количества копий мутации NOD2 (что связывается с риском развития болезни Крона) действительно коррелировало с сигнатурой экспрессии генов активированных макрофагов и фибробластов в тканях подвздошной кишки.
Чтобы понять функцию NOD2 в клетках человека, дифференцирующихся in vitro, авторы использовали моноциты периферической крови здоровых добровольцев и определили, есть или нет в клетках одна или две копии мутации NOD2, связанные с восприимчивостью к болезни Крона. Затем клетки дифференцировались in vitro в присутствии MDP и без него. Результатом стало большее количество активированных фибробластов в пропорции к клеткам с двумя копиями мутаций NOD2 по сравнению с клетками с нативным NOD2. Кроме того, увеличение количества мутаций NOD2 было связано с соответствующим увеличением количества фибробластов с сигнатурой экспрессии генов, характерной для активированных клеток. Интересно, что рыбки данио с дефицитом nod2, которые испытали воздействие MDP, обладали характеристикой экспрессии генов, характерной для активированных фибробластов, которая сохранялась даже во время восстановления после повреждения, опосредованного DSS. Рыбки данио с нативным типом nod2 таковой характеристикой не обладали. Исходя из этого, можно предположить, что дефицит nod2 препятствует эффективному разрешению фиброза и воспаления.
Для дальнейшего выяснения молекулярных основ связанной с риском мутаций NOD2 сигнатуры экспрессии генов, ответственных за развитие фиброза, авторы решили найти регуляторы транскрипции этого пути, стоящие выше на ступени контроля. Ученым удалось определить, что ген, кодирующий белок STAT3, в большей степени экспрессируется в активированных фибробластах и макрофагах. STAT3 является регулятором транскрипции ключевых компонентов воспалительных реакций и фиброза при воспалительных заболеваниях кишечника и действует через цитокиновый рецептор gp130. Анализ клинических данных, полученных от людей с болезнью Крона (у которых обнаружилось отсутствие реакции на антиФНО-терапию), выявил усиленную экспрессию генов, регулируемых gp130 и кодирующих белки IL-6, онкостатин M и IL-11 (терапия, основанная на антиФНО-антителах [ФНО — фактор некроза опухоли] — наиболее распространенный способ лечения болезни Крона). Это открытие подтверждает роль сигнализации посредством gp130 в этой группе лиц, устойчивых к упомянутой форме терапии.
Авторы предположили, что блокада gp130 может снизить частоту аномалий, возникающих при мутации NOD2. Они проверили эту гипотезу посредством использования базедоксифена (ингибитор gp130) на обработанных MDP клетках человека с мутациями NOD2. Базедоксифен действительно привел к снижению сигнатуры экспрессии генов, связанных с фибротическими процессами и обратил вспять изменения конфигурации клеток, являющихся характерными для активированных фибробластов. Этот препарат также снижал степень повреждения тканей кишечника, что было обнаружено у мутантных по отношению к nod2 рыбок данио, подвергшихся обработке DSS.
Начиная с описания клинических характеристик фиброза при болезни Крона, в данной работе описан молекулярный путь, связанный с мутациями NOD2, характерными для этого заболевания. Работа завершается предложением потенциальных подходов терапии для разрешения настоящих проблем лечения фиброза и лекарственной устойчивости к антиФНО-препаратам. Опираясь на генетику и клинические результаты этого внутриклеточного и молекулярного пути, исследование представляет собой «дорожную карту» для осуществления настоящих и будущих методов лечения.
Остается еще много интересных направлений исследования. Путь NOD2 — единственный описанный путь различения MDP, но в этой работе показаны индуцированные MDР клеточные и молекулярные изменения и в отсутствие nod2 на примере рыбок данио. Это означает, что существуют еще не описанные пути сигнализации MDР. Изначально характеристикой базедоксифена была формулировка «селективный ингибитор рецептора эстрогена» [8]. Это вызывает опасения, что в случае применения препарата в качестве терапевтического средства при болезни Крона он может оказывать побочное воздействие на другие сигнальные пути. У рецептора gp130 имеется множество аналогов связывания лиганда, влияющих на широкий спектр иммунных ответов. Следовательно, определение конкретных лигандов gp130, управляющих молекулярными событиями, опосредованными NOD2, может привести к селективному, более эффективному и безопасному терапевтическому воздействию, нежели чем полное ингибирование сигнализации gp130 или воздействие на иные клинически значимые молекулярные пути сигнализации, такие как ферменты Janus-киназы (ингибиторы которых находятся на поздней стадии клинической разработки для применения при болезни Крона).
Не у всех лиц с болезнью Крона существуют мутации NOD2, связанные с риском развития заболевания. Действительно, у людей определенных этнических групп (китайцев, малайцев, индусов) поражение подвздошной кишки является ведущим клиническим проявлением болезни Крона, однако NOD2 не связан с риском развития заболевания в этой популяции [5, 9]. Возможно, молекулярная сигнатура экспрессии генов активированных макрофагов и фибробластов является актуальной ключевой особенностью для людей с поражением подвздошной кишки при болезни Крона. Вероятно, различный генетический ландшафт может привести к сходным клиническим и молекулярным исходам. Следовательно, результаты Nayar с соавт. продвигают эту область на шаг ближе к молекулярной классификации болезни Крона, что может прояснить аспекты этого тяжелого состояния, насчитывающего около 200 генетических областей, связанных с риском развития заболевания [10] и его различными клиническими проявлениями.
