Усовершенствованные липидные везикулы могут стать ключом к созданию нового поколения мРНК-вакцин

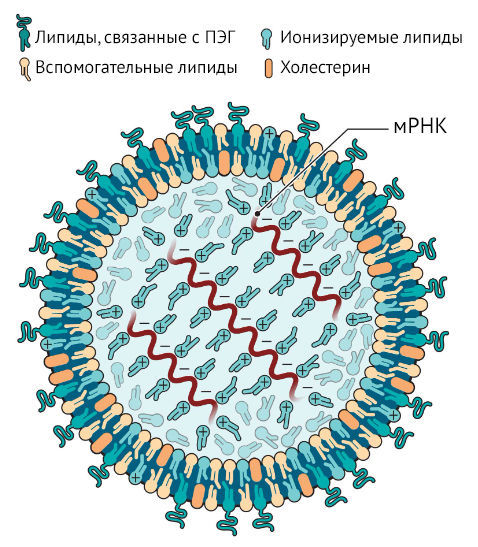
Любой диетолог скажет, что некоторые виды жиров полезны, и это, безусловно, верно в отношении маленьких липидных везикул, являющихся компонентами двух наиболее широко используемых в мире вакцин против COVID-19. Эти крошечные жировые пузырьки, известные как липидные наночастицы (ЛНЧ), содержат в себе информационную РНК (мРНК), которая кодирует вирусный белок, и помогают доставить ее в клетки и защитить от разрушительного воздействия внутриклеточных ферментов. Эта технология стала ключом к успеху вакцин против COVID-19, разработанных компаниями Moderna и Pfizer-BioNTech. Однако, несмотря на все положительные стороны уже существующих вакцин, предел совершенства еще не достигнут.
▶ Читайте также: Стартапы способствуют запуску новой волны мРНК-терапии
Наночастицы служат основной причиной нежелательных побочных эффектов при их распространении по организму, вызывая болевой синдром и воспалительные реакции, которые многие люди испытывают после вакцинации. Проблема заключается в затруднении высвобождения содержимого этих наночастиц уже внутри клеток, ведь это — необходимый этап для запуска механизма синтеза белка, который превращает нуклеотидные последовательности мРНК в непосредственный субстрат иммунных реакций. А поскольку ЛНЧ при нагревании распадаются, их приходится хранить при низких температурах, что ограничивает их использование по миру.
По словам биохимика Питера Каллиса из Университета Британской Колумбии (UBC) в Ванкувере, создателя первых ЛНЧ, у данной системы есть еще потенциал для развития, и необходимо повышать эффективность ЛНЧ.
В настоящее время крупные фармацевтические и биотехнологические стартапы ведут разработки нового поколения ЛНЧ с повышенной стабильностью и большей тканеспецифичностью, эффективность которых была бы выше, а количество побочных эффектов — меньше. Многое поставлено на карту: эти усовершенствованные наночастицы могут привести к созданию нового поколения мРНК-вакцин против COVID-19 и других заболеваний. Также с их помощью планируется использовать мРНК уже в качестве инструмента для лечения болезней. По словам Филипа Сантанджело, инженера-биомедика из Технологического института Джорджии, существующие в теоретической сфере новшества систем доставки [лекарственных или вакцинных компонентов], безусловно, изменят правила этой игры. Сантанджело сотрудничал с несколькими компаниями, производящими мРНК.
Первые ЛНЧ Каллис с коллегами разработали около 20 лет назад; изначально эти наночастицы предназначались для транспортировки в клетки препаратов, подавляющих работу генов. Впоследствии ему и другим исследователям удалось адаптировать четыре липидных компонента ЛНЧ для доставки в поврежденные клетки последовательностей мРНК, корректирующих течение патологии. Теперь, как заявляет Анна Блэкни (биоинженер UBC, соучредитель компании-производителя РНК-вакцин VaxEquity), когда была обнаружена новая сфера применения — вакцины — предстоит еще так много разработок и оптимизаций. И когда дело доходит до понимания того, как клетки взаимодействуют с наночастицами, это, по ее словам, просто один огромный вопрос.
Ранее в этом году появилась одна подсказка, когда ученые компании Genentech продемонстрировали, как наночастицы активируют определенный воспалительный путь — ось интерлейкина-1. Он является ключевым при инициации защитных иммунных реакций, однако также может быть причиной побочных эффектов. Одна из изученных ЛНЧ, в составе которой был т. н. «ионизируемый» липид SM-102, помогающий связывать и упаковывать мРНК в ЛНЧ, оказалась в выраженной степени способной активировать этот путь. Это может объяснять, почему вакцина компании Moderna, в составе которой присутствует SM-102, в равной степени и эффективна, и склонна у вызывать у людей плохое самочувствие.
Команда Genentech не проводила оценку аналогичного липида из вакцины Pfizer-BioNtech. Однако Мохамад-Габриэль Аламе и его коллеги из Медицинской школы Перельмана Пенсильванского университета протестировали сходный вакцинный препарат и обнаружили, что он инициирует появление широкого спектра воспалительных молекул, как желательных [для развития иммунного ответа], так и нежелательных. На данный момент, как поясняет Аламе, цель состоит в разработке таких ионизируемых липидов, которые активировали бы нужные иммунные реакции, не запуская при этом вредные; это сложно, но возможно, — продолжает он. Аламе вместе с биоинженером Майклом Бушманном из Университета Джорджа Мейсона и другими основал AexeRNA Therapeutics.
Бушманн умер в марте 2022 года; до этого он возглавлял группу, которая в 2021 году продемонстрировала ключевое влияние электрического заряда на ЛНЧ и, как следствие, успех применения вакцины. Отрицательный заряд снижает вероятность, что наночастица останется в мышечной ткани и лимфатических узлах мышей (куда ввели исследуемый препарат), где она могла бы способствовать развитию необходимых иммунных реакций; вместо этого ЛНЧ начинают широко распространяться по тканям, повышая риск лихорадки, озноба и других побочных эффектов.
Для создания наночастицы с меньшим по модулю отрицательным зарядом исследователи изменили химический состав ионизируемого липида. Согласно данным, опубликованным в прошлом году в формате препринта (в настоящее время они находятся на рассмотрении в Nature Communications), после включения в состав мРНК-вакцины против COVID-19 новой везикулы ЛНЧ (переносчика мРНК) у мышей вырабатывалось большее количество антител по сравнению со стандартными системами доставки, а также уменьшилось количество побочных эффектов.
Дэн Пир, биохимик из Университета Тель-Авива и соучредитель стартапа по доставке вакцин NeoVac, также разработал библиотеки новых ионизируемых липидов с нетипичным химическим составом. Как свидетельствуют результаты неопубликованных исследований, по-видимому, это позволяет создавать более качественные мРНК-вакцины с меньшим количеством побочных эффектов, а также продлевает срок их хранения при комнатной температуре.
Иные способы добиться повышения эффективности вакцин включают усиление захвата ЛНЧ клетками, а затем — высвобождения ЛНЧ из впячиваний клеточной мембраны, известных как эндосомы, которые транспортируют наночастицы внутрь клетки. Подавляющее большинство ЛНЧ попадают в эти клеточные образования, а впоследствии уничтожаются или распадаются, не доставляя свой полезный вакцинный «груз». Как поясняет Гаурав Сахай, биоинженер из Oregon Health & Science University, это означает, что огромный массив РНК из состава вакцины не используется клеткой.
Форма ионизируемых липидов влияет на способность ЛНЧ разрушать эндосомы подобно тому, как это делает холестерин, входящий в состав ЛНЧ наряду с молекулами других жиров. Вместе с учеными из компании Moderna Сахай с соавт. в 2020 году сообщали, что использование различных форм холестерина может повысить скорость высвобождения ЛНЧ из эндосомного компартмента. Сахай основал компанию Enterx Biosciences для коммерциализации открытий своей команды.
Исследователи компании Sanofi начали проводить испытания некоторых усовершенствованных ими ЛНЧ на людях. Например, в исследовании, которое было начато в 2021 году, компания оценила два варианта ЛНЧ для доставки разрабатываемой ей мРНК-вакцины против гриппа. Согласно предварительным данным, одна липидная структура оказалась намного эффективнее для запуска иммунитета против гриппа. Об этом заявил в декабре 2021 года на мероприятии для инвесторов Фрэнк ДеРоса, руководитель отдела исследований и биомаркеров в Инновационном Центре мРНК компании Sanofi. Но та же ЛНЧ также провоцировала и более частые побочные эффекты при более высоких дозах.
Другие фирмы, такие как BioNTech и Arcturus Therapeutics, исследуют способы отказаться от полиэтиленгликоля — соединения, которое стабилизирует ЛНЧ. Однако это вещество также связывают с развитием некоторых типов побочных реакций на вакцинные препараты. Тем временем, другие компании сосредоточены на оптимизации структуры липидов [для доставки мРНК] в составе препаратов для лечения болезней, а не средств профилактики последних. Для этого необходимо транспортировать внутрь клеток мРНК, кодирующую белки, которые корректировали бы само заболевание. Однако перенос мРНК необходим именно в те клетки и ткани, где они требуются, а не только в печень, в которой, как правило, современные ЛНЧ-препараты оказываются после инфузии. По словам Доминика Витцигманна, соучредителя и исполнительного директора стартапа NanoVation Therapeutics, основанного Каллисом, совершенствование системы транспортировки мРНК посредством ЛНЧ станет ключом к реальному расширению влияния технологии мРНК на различные ткани.
Повышенное внимание к технологиям ЛНЧ наряду с прибылью, полученной от вакцин против COVID-19, вылилось в увеличение числа судебных разбирательств. Представители компании Alnylam, которая занималась разработкой первого одобренного препарата с технологией транспортировки ЛНЧ (это был препарат, вышедший на рынок в 2018 году и подавляющий экспрессию генов для лечения редкого нейродегенеративного заболевания) утверждают, что именно им принадлежат патенты на ключевые липидные компоненты вакцин компаний Moderna и Pfizer-BioNTech. А юристы компании Arbutus BioPharma — еще одной канадской фирмы, соучредителем которой является Каллис — требуют от Moderna возмещения убытков за нарушение патента на ЛНЧ с определенным химическим составом липидов.
Тем не менее, Джейкоб Шеркоу, патентный адвокат в области биотехнологий из Юридического Колледжа Университета Иллинойса, полагает, что эти тяжбы об интеллектуальной собственности вряд ли окажут тормозящее влияние на развитие технологии ЛНЧ. Он считает, что в эту затею уже вложено слишком много денег.
