История о любви к витамину С

Наследием для любого поколения врачей становятся препараты, которые, как кажется современникам, обладают не одними лишь сугубо биологическими функциями. Для моряков в XVIII веке это были цитрусовые, в которых буквально заключалась разница между жизнью и смертью на корабельной палубе. Романтические воззрения конца XX века нашли выражение в кристальной вере Лайнуса Полинга в аскорбат. А для многих пациентов в США, находящихся в реанимационных отделениях в наши дни, витамин С стал редкостью — вроде бы хорошо известной молекулой, однако с новыми загадками. Это история любви к идее, рассказанная посредством испытаний и множества доказательств.
Действие Первое — моряки, цинга и первое «рандомизированное» исследование
Знаменитая работа Джеймса Линда 1747 года, в которой он сравнивал разные лекарства и цитрусовые в контексте лечения цинги, часто рассматривается как первый пример рандомизированного клинического исследования, хотя само включение в выборку не подпадало под описание истинной рандомизации в современном смысле. Тем не менее, по прежнему метод Линда — сравнение подобного с подобным, где варьирует лишь одна переменная — был революционным. Моряки, которым давали апельсины и лимоны, восстанавливались очень быстро, а те же, кому давали сидр, винный уксус, морскую воду или же крепкие спиртные напитки — нет. Эксперимент попал в благодатную почву клинической традиции: врачам в своих выводах необходимо опираться не на единичные случаи, а на строгое сравнение; физиологические теории проверяются лишь многократно повторяемыми свидетельствами.
Действие Второе — обещания Полинга
Двумя столетиями позже дважды Нобелевский лауреат Лайнус Полинг утверждал, что применение витамина С способно предотвратить развитие простудных заболеваний и улучшать самочувствие, стимулируя широко распространенное восхищение, которое едва ли можно затмить какими-то данными. Заявление Полинга опережало время, однако в одном ученый был прав: биологическое влияние аскорбиновой кислоты невероятно разнообразно — от ее роли в качестве кофактора при синтезе катехоламина до функции буфера-восстановителя в условиях стресса. Интерес к витамину С пришел и в сферу онкологии, где, согласно рекомендациям Национального института онкологии США, по-прежнему поддерживается введение витамина С внутривенно в качестве средства вспомогательной терапии. Это многообещающая гипотеза, в сути которой переплетены данные клинических испытаний, нерешенные вопросы дозирования и способов введения самого вещества.
Витамин С вскоре твердо установит свое присутствие в схемах лечения в области интенсивной терапии. Молекулы аскорбата в составе дофамин-β‑гидроксилазы (фермента, который опосредует превращение дофамина в норадреналин, поддерживает функционирование эндотелия и обезвреживает свободные радикалы) выступают в качестве «физиологических крючков», идеально подходящих для состояния септического шока, когда наблюдается усиленная потребность организма в катехоламинах, а среда биохимических реакций изобилует окислителями.
Действие Третье — искра: этап экспериментального применения в условиях реанимационного отделения и клинических испытаний
В начале 2017 года Марик с соавт. опубликовали результаты одноцентрового исследования «до и после» в Chest (47 пациентов за один период исследования), в котором было показано, что применение гидрокортизона, витамина С и тиамина в значительной степени снижает больничную летальность при тяжелом сепсисе/септическом шоке (8,5 % против 40,4 %; скорректированная вероятность летального исхода 0,13, 95 % ДИ 0,04–0,48) [5]. Затем эта история попала в издание Critical care reviews («Обзоры по интенсивной терапии»), а выступление самого Марика на конференции ССR в Белфасте в 2017 году привлекло всеобщее внимание и вызвало скептицизм [6].
В течение двух лет Фаулер с соавт. сообщили о результатах CITRIS-ALI, многоцентровом рандомизированном контролируемом исследовании пациентов с сепсисом и РДСВ (респираторным дистресс-синдромом взрослых), рандомизированных на группы приема высоких доз витамина С (50 мг/кг каждые 6 часов в течение 96 часов) и плацебо.
В качестве трех конечных первичных точек были взяты изменения параметров шкалы SOFA, С-реактивного белка и тромбомодулина спустя 96 часов; все три конечные первичные точки оказались отрицательными. Номинально более низкая смертность на 28-ой день наблюдалась среди тех, кому вводили витамин С (смертность на 28-ой день — вторичная конечная точка), однако исследование не было скорректировано по множественные сравнения; авторы справедливо рекомендовали соблюдать осторожность [7].
Затем последовала рандомизация самого «коктейля» Марика. В исследовании VITAMINS, проведённом Фуджи и соавт. и представленном в формате live [57] на конференции CCR20, сравнивали гидрокортизон + витамин C + тиамин с одним лишь гидрокортизоном при септическом шоке. Первичной конечной точкой служили часы жизни и отсутствие необходимости введения вазопрессоров спустя 7 дней: различий в экспериментальных группах выявлено не было (медиана 122,1 против 124,6 ч; разница — 2,5 ч, 95% ДИ от −10,0 до 5,1) [8]. В то же время в ходе исследования ACTS (n = 200) не было обнаружено снижения параметра SOFA спустя 72 ч (разница между группами −0,8, 95 % ДИ −1,7 до 0,2), а сигнал по смертности оказался нейтральным (HR 1,3, 95 % ДИ 0,8–2,2) [9]. Исследование VICTAS (n = 501) было остановлено по причине трудностей в финансировании (и проблем со сроками): различий во времени, проведенном без аппарата ИВЛ/вазопрессоров спустя срок в 30 дней обнаружено не было (медиана 25 против 26; разница −0,2 дня, 95 % ДИ −3,5 до 3,8) [10]. ATESS — тщательно проведенное рандомизированное контролируемое исследование из Кореи — также дало нейтральные результаты [11].
Наконец, исследование LOVIT, опубликованное в NEJM, поставило отрезвляющий вопрос: может ли витамин С оказаться вредным веществом для больных в тяжелом состоянии? У 872 взрослых пациентов с сепсисом, принимавших вазопрессоры, введение высоких доз витамина С (50 мг/кг каждые 6 часов в течение 96 часов) увеличило совокупное число случаев летального исхода или стойкой дисфункции органов на 28-й день по сравнению с плацебо (44,5 % против 38,5 %; абсолютная разница 6,0 процентных пунктов, 95 % ДИ 0,8–11,2; ОР 1,21, 95 % ДИ 1,04–1,40) [12].
К 2023 году тщательный метаанализ монотерапии внутривенным витамином С у тяжелобольных взрослых пациентов показал отсутствие влияния на смертность. Также была отмечена неоднородность данных, но не было выявлено убедительных сигналов к применению этой терапии за пределами клинических исследований [13].
Важное замечание о разногласиях
В марте 2022 года в СМИ появились статистические сообщения о том, что исходное исследование «до и после» 2017 года могло основываться на сфальсифицированных данных; эти данные не были отрецензированы, были оспорены авторами, и, что особенно важно, статья из Chest до сих пор опубликована без опровержения или комментариев со стороны редакции [5, 14]. Независимо от точки зрения, этот эпизод с обвинениями еще раз подчеркнул необходимость отдавать предпочтение нейтральным, хорошо проведённым рандомизированным контролируемым испытаниям, а не драматичным результатам наблюдений.
Интерлюдия — парадокс антиоксидантов: когда витамин С превращается в прооксидант
Существует соблазн сосредоточиться только на потенциальной пользе, когда применение вещества физиологически обосновано. Однако вопросы окислительно-восстановительных процессов — это палка о двух концах, как и применение аскорбата. При фармакологических концентрациях в плазме, достигаемых только при внутривенном введении, аскорбат может восстанавливать переходные металлы (например, Fe3+ → Fe2+), катализируя реакцию Фентона и генерируя перекись водорода (H2O2) во внеклеточной среде; благодаря точным исследованиям in vivo на животных и людях было продемонстрировано образование в данных условиях радикалов аскорбата и H2O2 [15]. Согласно современным исследованиям, аскорбат — это «двоякое» соединение: он может выступать как антиоксидант в физиологических концентрациях и как потенциальный прооксидант в миллимолярных концентрациях, в зависимости от доступности каталитического металла и компартмента клетки, где протекает реакция [16].
Почему это важно применительно к интенсивной терапии? Потому что сепсис — это состояние, характеризующееся в том числе высоким содержанием свободного железа, воспалением и нарушением регуляции метаболизма. Терапия, способствующая донации электронов и генерации H2O2, может, вопреки здравому смыслу, усугубить окислительное повреждение или изменить микрососудистый сигналинг в восприимчивых тканях. Добавьте к этому ятрогенные риски, такие как оксалатная нефропатия (витамин C метаболизируется до оксалата и способствует образованию камней) и аналитические артефакты (помехи в работе некоторых глюкометров, используемых непосредственно «у постели больного»), и аргументы в пользу баланса уже звучат убедительно. Подтвержденная биопсией оксалатная нефропатия уже описана после внутривенного введения высоких доз витамина С тяжелобольным пациентам. Например, засвидетельствованы два случая при инфекции COVID-19 (ОПН с отложением оксалата кальция) и еще несколько аналогичных случаев в период пандемии [17, 18]. Высокие концентрации аскорбата также могут провоцировать ложную гипергликемию на некоторых глюкометрах (работающих на основе глюкозодегидрогеназы; такие глюкометры используют в местах оказания неотложной помощи, особенно при почечной недостаточности), что создает риск введения инсулина и развития гипогликемии, если гипергликемия не будет подтверждена в лаборатории [19, 20].
Терапевтическое размышление требует симметрии: возможность необходима, однако недостаточна; необходимо с равной серьезностью взвесить возможный вред, прежде чем приступать к масштабной терапии. Витамин С воплощает этот баланс.
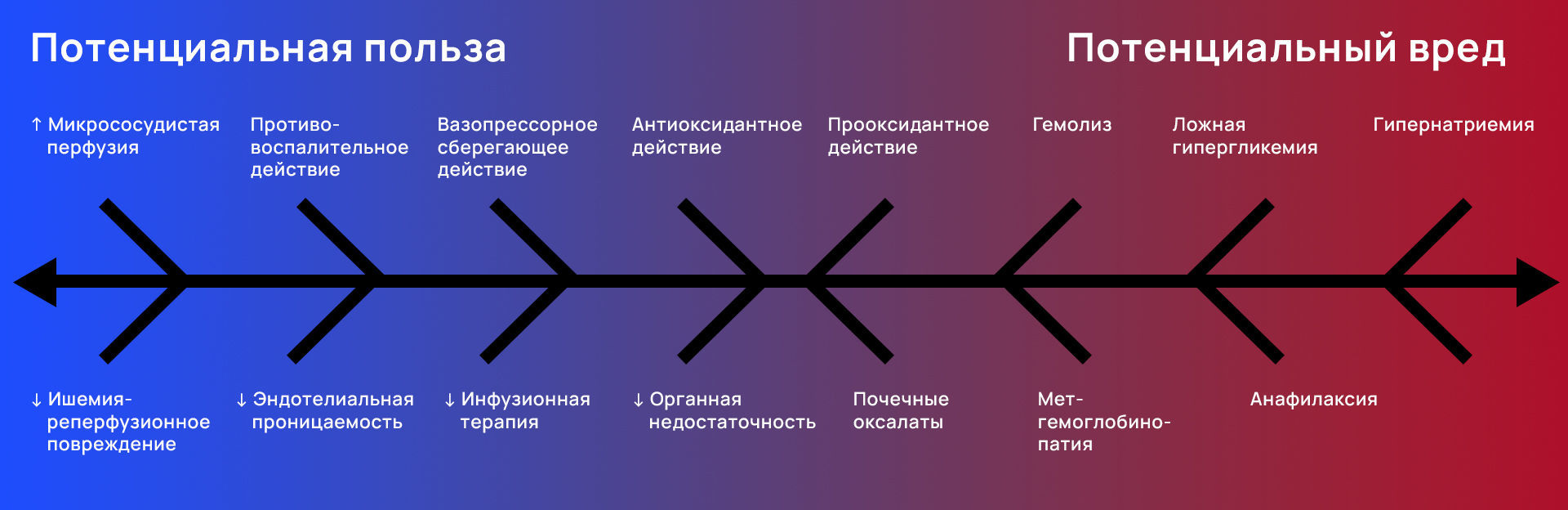
Рис. 2 | Потенциальные преимущества и потенциальный вред от применения витамина С при жизнеугрожающих состояниях (схематично)
Потенциально возможные механизмы действия витамина С
Если наш «роман» с витамином С начался с моряков и возродился благодаря сепсису, то молекулярно-биологический сценарий не менее драматичен. В эндотелии аскорбат накапливается посредством транспортеров SVCT (от англ. sodium-vitamin C cotransporters — натриево-аскорбатный котранспортер; существует в двух изоформах: SVCT1 and SVCT2, прим. перев.), усиливает NO-сигналинг и стабилизирует проницаемость клеточного барьера в условиях воспалительного стресса [21]. Один из хорошо известных путей — тетрагидробиоптериновый (BH4): аскорбат увеличивает внутриклеточную активность BH4, восстанавливая связь с эндотелиальной синтазой оксида азота (eNOS) и физиологическую выработку NO, когда окислительный стресс в противном случае сдвинул бы работу фермента в сторону супероксида [22, 23, 24].
Витамин С также является классическим кофактором для нескольких Fe2+/2-оксоглутарат-зависимых гидроксилаз. К ним относятся пролил- и лизилгидроксилазы, участвующие в биосинтезе коллагена (который составляет основу целостности сосудов и скорости заживления ран), а также две гидроксилазы биосинтеза карнитина, которые способствуют поступлению жирных кислот в митохондрии во время стресса [25, 26]. В нейрогуморальном взаимодействии аскорбат позволяет пептидилглицин-α-амидирующей монооксигеназе (ПАМ) преобразовывать глицин-удлиненные предшественники в амидированные гормоны (например, пептиды семейства вазопрессина) и поддерживает синтез катехоламинов через дофамин-β-гидроксилазу — механизмы, которые естественным образом связаны с физиологией шока [4, 27].
Помимо классической энзимологии, аскорбат модулирует гипоксию и регуляцию генов. Будучи восстанавливающим кофактором для пролилгидроксилаз, мишенью которых является HIF-α, аскорбат способствует деградации HIF и может смягчить взаимодействие гипоксии и воспаления; он также усиливает диоксигеназы TET/JmjC, которые управляют активным деметилированием ДНК и гистонов — путями, которые, как выяснилось, чувствительны к аскорбату в иммунокомпетентных и эпителиальных клетках [28, 29].
С иммунологической точки зрения витамин С накапливается в нейтрофилах, поддерживает хемотаксис и фагоцитоз, а также может модулировать нетоз; дефицит витамина С нарушает некоторые из этих функций in vivo [30]. На микрососудистом уровне у животных и клеточных моделях удалось продемонстрировать улучшение капиллярной перфузии, снижение проницаемости барьеров и сохранность соединительных белков во время воспалительного стресса; данные эффекты связаны с ингибированием сигналинга НАДФН-оксидазы и защитой фосфорилированного состояния плотных контактов [31, 32, 33, 34].
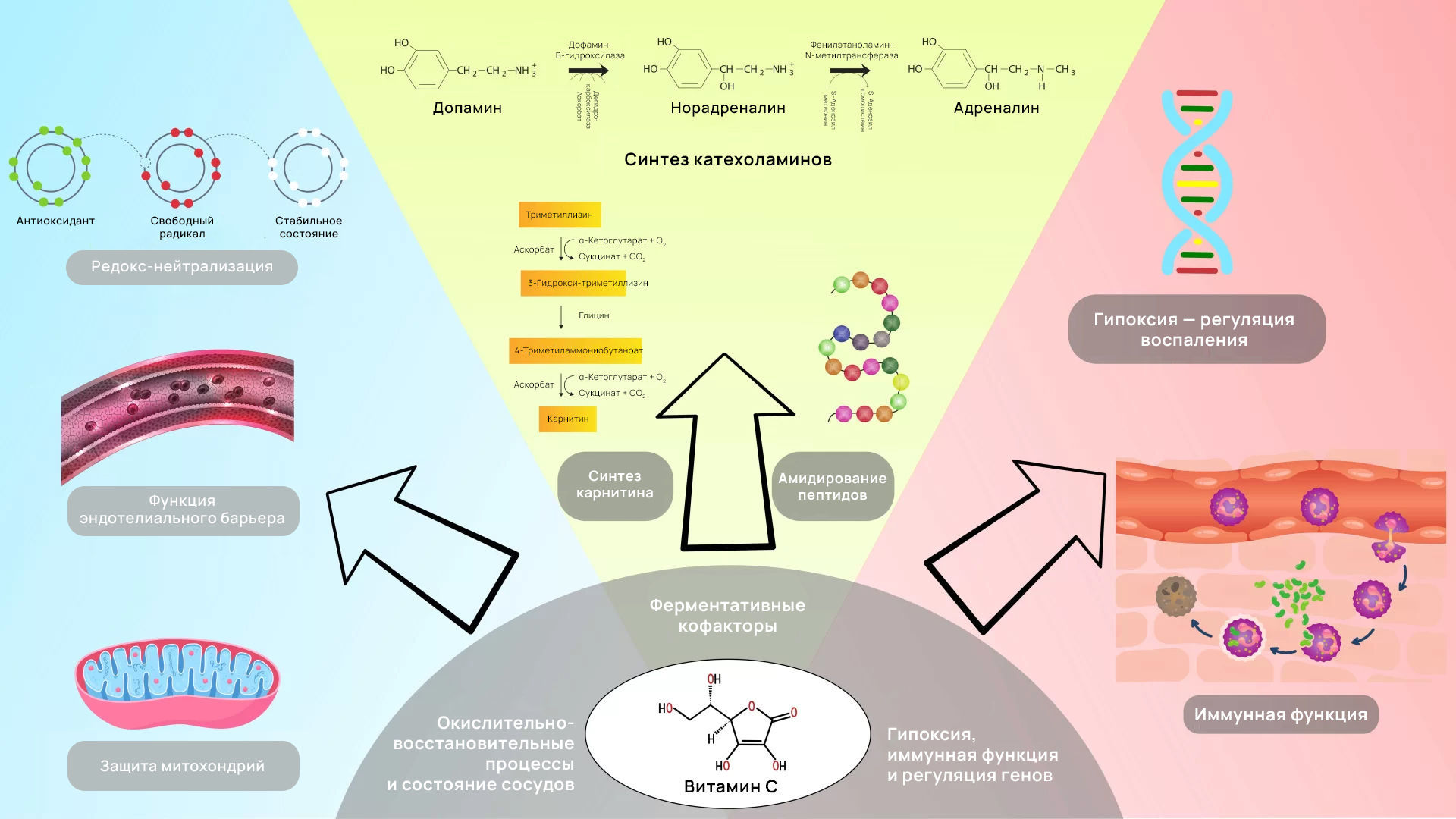
Рис. 1 | Механизмы действия витамина С в условиях жизнеугрожающих состояний.
Потенциальные преимущества и недостатки — подводим итоги
На что, учитывая представленную физиологическую картину, можно надеяться и чего опасаться в условиях отделения интенсивной терапии? В перечень потенциальных преимуществ входят:
- улучшение микрососудистой перфузии и стабильности эндотелиального барьера, что неоднократно наблюдалось в доклинических моделях сепсиса и ишемии-реперфузии [31, 32, 33];
- противовоспалительный сигналинг посредством ингибирования NF-κB [36];
- снижение потребности в вазопрессорах, определенный в рамках небольшого рандомизированного контролируемого исследования при хирургическом септическом шоке [35].
В одноцентровом исследовании раннее применение высоких доз витамина С снижало объемы реанимационных мероприятий, хотя на данный момент какое-либо серьезное обобщение осуществить невозможно [43]. Тем не менее, в современных РКИ итоги применения витамина С в отделениях интенсивной терапии при тяжелых исходах можно описать как «без изменений» или даже «стало лишь хуже» — без учета вторичных данных о смертности, полученных в рамках исследования CITRIS-ALI, — что подчеркивает разрыв между механизмами и эффектами [7, 12, 13].
Потенциальный вред заключается в «двуличной природе» аскорбата:
- прооксидантной биохимии (как образование радикала аскорбата/H2O2 в миллимолярных концентрациях [15,16]);
- оксалатной нефропатии [17,18];
- ложной гипергликемии, которая срабатывает на некоторых глюкометрах [19,20];
- гемолизе и даже метгемоглобинемии при инфузии высоких доз, зафиксированных у некоторых у пациентов с дефицитом G6PD [37, 38].
Стратегии применения «мегадоз» аскорбата натрия также связаны с нагрузкой натрием; в пилотных исследованиях наблюдалась гипернатриемия [39].
Действие Четвертое — почему сепсис не поддался лечению?
Нейтральные и неблагоприятные результаты не являются загадочными, если рассматривать их в совокупности с патофизиологией и методом исследования. Во-первых, кортикостероиды являются эффективными средствами вспомогательной терапии при некоторых фенотипах септического шока; в двух ключевых исследованиях кортикостероиды уже широко применялись или же были обязательным средством в контрольной группе (в исследовании VITAMINS применялся только гидрокортизон; в исследовании VICTAS открыто применялись в ~32 % случаев), а в ACTS их применение было разрешено, однако они использовались в меньшинстве случаев (~14%) — все это могло «смазать» клиническую картину в контексте добавления витамина С или тиамина к терапии [8, 9, 10]. Во-вторых, время играет решающую роль в исследованиях сепсиса: молекулярные пути, чувствительные к реакциям восстановления, могут оказаться в наибольшей степени подвержены модификации на очень ранних стадиях — до того, как наступит повреждение органов, — однако многие участники были рандомизированы уже после того, как физиологические проявления шока сохранялись в течение нескольких часов [7, 12, 13]. В-третьих, дозировка и фармакокинетика играют значимую роль. Витамин С, принимаемый перорально, быстро насыщает кишечные транспортеры, тогда как внутривенное введение может способствовать достижению уровней в плазме на порядок выше; распределение, почечный транспорт и окислительно-восстановительная среда в значительной степени различаются у разных пациентов [13].
Руководящие группы изменили свое решение: в 2021 году кампания «Выживание при сепсисе» (Surviving Sepsis Campaign) выпустила «мягкую» рекомендацию, выступая против рутинного внутривенного введения витамина С при сепсисе/септическом шоке вне клинических испытаний, ссылаясь на доказательства с низкой степенью достоверности и отсутствие доказанной пользы [40].
Небольшое замечание о дозе
Доза часто трактуется довольно расплывчато, поэтому в источниках применительно к применению препаратов в условиях отделения интенсивной терапии используется практико-ориентированная таксономия. При потреблении витамина С из продуктов питания, обычном для сбалансированного рациона — около 75 мг/сут для женщин и 90 мг/сут для мужчин — всасывание витамина С из кишечника происходит очень эффективно, превышая 80 %, а его концентрация в плазме стабилизируется на уровне около 60 мкмоль/л. Эти дозы соответствуют физиологическому диапазону, удовлетворяющему метаболическим потребностям в кофакторах ферментов и антиоксидантной регенерации.
При увеличении общего потребления до сотен миллиграммов в день при пероральном приеме эффективность абсорбции начинает снижаться, однако уровень в плазме крови умеренно повышается до плато ≈ 70–80 мкмоль/л. Это определяет обычный диапазон доз добавок, за пределами которого прием per os витамина в более высоких дозах дает лишь незначительный прирост, поскольку кишечные транспортеры и почечная система оказываются уже в насыщенном состоянии.
При приеме витамина свыше 1 г/сут усваивается менее половины витамина С, а его концентрация в плазме существенно не повышается. Только внутривенное введение позволяет обойти эти ограничения, кратковременно создавая миллимолярные концентрации в плазме — то есть на порядки выше, чем при пероральном приеме [41].
«Высокодозовые» схемы внутривенного введения в условиях сепсиса в различных исследованиях обычно предусматривали введение 6–16 г/день (например, в случае исследований CITRIS-ALI и LOVIT 50 мг/кг каждые 6 ч в течение 96 ч) [7,12]. Применение «мегадоз» (≥30 г/день) изучалось в доклинических исследованиях и небольших трансляционных исследованиях при глубокой вазоплегии; биологическое обоснование (включая потенциальный прооксидантный сигналинг) является провокационным и не доказанным при сепсисе [42].
Действие Пятое — помимо сепсиса: другие рубежи интенсивной терапии
Что касается условий интенсивной терапии, изучалось применение витамина С не только при сепсисе, но и при ожогах. В более раннем одноцентровом исследовании предполагалось снижение потребности в жидкости при высоких дозах витамина С в случае обширных ожогов, однако внешняя обоснованность и различия в современных методах лечения ограничивают возможность обобщения [43]. Диетология, в свою очередь, напоминает нам, как быстро развивается витаминодефицит у пациентов в критическом состоянии — концентрация витамина С в плазме может опускаться до уровня «латентной цинги», — при этом, отсутствуют доказательства того, что супрафизиологическое восполнение [запасов витамина в организме] способствует улучшению течения болезни [41].
Действие Шестое — центры клинических испытаний: от Белфаста до Мельбурна
Современная арка витамина C прошла через CCR. Лекция Марика на конференции CCR17 (Critical Care Reviews Meeting 17) зажгла искру десяти лет исследований [6]. Ситуация изменилась уже на момент CCR20, когда в прямом эфире состоялась презентация РКИ VITAMINS для тысяч врачей по всему миру, что сопровождалось открытыми обсуждениями и немедленной реакцией редакции [8]. Тщательно разработанный дизайн LOVIT заставил переосмыслить устоявшиеся представления: была выдвинута гипотеза о том, что применение высоких доз витамина С в лечении сепсиса несет вред [12].
Действие Седьмое — круг замкнулся: высокая доза, затем мегадоза?
Даже когда клинические испытания при сепсисе охладили энтузиазм, некоторые исследователи задались вопросом, может ли витамин С действовать при иных биологических условиях или в дозах, достаточно высоких, способных изменить механизм его действия. В доклинических и ранних трансляционных исследованиях изучалось применение «мегадозы» аскорбата натрия для купирования вазоплегии — фармакологическом эффекте, который способствует проявлению тех самых прооксидантных свойств, о которых говорилось выше. Гипотеза столь же смелая, сколь и спорная: может ли контролируемый выброс внеклеточного H₂O₂ сигнализировать о восстановлении сосудов при шоке? Ответ может быть получен только в результате строгих РКИ, ориентированных на здоровье пациента, а не на выяснение теоретических аспектов кинетики [42].
Интерес не угасает. В ходе недавнего пилотного двойного слепого рандомизированного исследования было протестировано применение “мегадозы” аскорбата натрия при септическом шоке (60 г в течение 6 часов): итогом стала фиксация физиологических симптомов (больший кумулятивный диурез; более быстрое снижение [титра] вазопрессора), однако существенной разницы в 24-часовой первичной конечной точке не наблюдалось; исследование было зарегистрировано как проспективное [39, 44]. За пределами окна набора в отделение интенсивной терапии, для РКИ в области неотложной помощи (C-EASIE) было рандомизировано 292 пациента с сепсисом или септическим шоком в группы раннего внутривенного введения витамина С (1,5 г каждые 6 часов в течение 4 дней) или плацебо: никаких результатов зафиксировано не было; подобные работы подчеркивают строгость современных протоколов РКИ [45, 46]. Зарегистрированные новые РКИ иллюстрируют процесс текущих изысканий в данной области, например, исследование применения высоких доз витамина С при септическом шоке и многоцентровую программу мегадоз [47, 48]. В области ухода за пациентами, пережившими остановку сердца, в протоколах, аналогичных VITaCCA, например, программе VICEPAC, оценивается схема применения высоких доз [витамина С] при остановке сердца, сопровождаемой шоком, во внегоспитальных условиях [49]. Многоцентровое РКИ допустимости применения «мегадоз» аскорбата натрия при раннем септическом шоке также зарегистрировано в ANZCTR (MEGA SCORES), что отражает методические дальнейшие шаги в этой области [50].
В рамках крупного международного многоцентрового исследования (VICToRY) при ожогах оценивается эффективность внутривенного введения высоких доз витамина С (примерно 200 мг/кг/день в течение 96 часов) в сочетании со стойкой дисфункцией органов и смертью. Набор пациентов проводится в том числе в канадских центрах, а подробная информация доступна на страницах регистрации и спонсоров [51, 52].
Финал — синдром, развивающийся после остановки сердца: исследование VITaCCA
Ишемия-реперфузия после остановки сердца — это окислительно-восстановительный шторм, отличающийся от иммунных нарушений при сепсисе. Это различие взято за основу в исследовании VITaCCA — многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования, проведенного в Нидерландах, целью которого было изучение влияния введения высоких доз витамина С (на начальных этапах реанимационных мероприятий) на дисфункцию органов после остановки сердца. В исследовании с плацебо сравниваются две стратегии внутривенного введения: ≈ 3 г/сут (аналогичная пищевой добавке) и 10 г/сут («фармакологическая») в течение 96 часов. Запланировано участие 270 пациентов, конечные точки основаны на шкале SOFA, а также проводились подробные исследования безопасности и фармакокинетики/фармакодинамики [53, 54, 55].
Здесь присутствует определенная поэтическая симметрия. Витамин, повлиявший на бортовую медицину в эпоху Нового Времени, обрел новую жизнь в области интенсивной терапии. Проведены серьезные испытания его применения в условиях сепсиса, и выяснилось много интересного о дозировке, сроках применения и потенциальном вреде. Теперь, в другой патофизиологической обстановке, нам, возможно, станет известно еще больше. В рамках конференции CCR Down Under в Мельбурне (9–10 декабря 2025 года) состоится презентация результатов VITaCCA [56], завершая путь, начатый с выступления Марика на конференции CCR17 и прошедший через исследования VITAMINS и LOVIT.
Спасёт ли VITaCCA роман витамина С или напишет ему эпитафию? Физиологические механизмы — скорее в пользу витамина С, но условия проведения РКИ жесткие, а моментом истины в определенном смысле станет CCR. До встречи в Мельбурне, где многое станет ясно.
