Исследование SAMSON и эффект ноцебо: о непереносимости статинов
Краткий обзор
Цель
Статины являются незаменимыми препаратами в лечении сердечно-сосудистых заболеваний атеросклеротического генеза; однако они по-прежнему недостаточно широко используются, в значительной степени из-за опасений по поводу побочных эффектов. В статье описана роль эффекта ноцебо в восприятии непереносимости статинов и предложены рекомендации по лечению с использованием как статинов, так и других гиполипидемических препаратов.
Недавние результаты
В ходе недавнего исследования «Метод самооценки побочных эффектов статинов или ноцебо» (SAMSON) было показано, что 90 % неблагоприятных симптомов, связанных со статинами, возникали также и при приеме плацебо, что является убедительным свидетельством эффекта ноцебо. Важно отметить, что 50 % пациентов, участвовавших в исследовании, смогли успешно возобновить терапию статинами.
Резюме
Непереносимость статинов встречается часто, и в большинстве случаев ее легко купировать путем подбора сроков терапии и корректировки доз и/или режимов дозирования. Для тех, у кого сохраняется переносимость статинов, существуют многочисленные альтернативные гиполипидемические препараты, обладающие высокими профилями безопасности и эффективности.
Введение
Атеросклеротические сердечно-сосудистые заболевания (АССЗ) являются основной причиной заболеваемости и смертности во всем мире [1]. В последнее время бремя атеросклеротических заболеваний растет. В 2020 году ССЗ стали причиной около 19 миллионов смертей, что на 18,7 % больше, чем в 2010 году [2].
Статины, механизм действия которых заключается в ингибировании 3-гидрокси-3-метилглутарил-КоА (ГМГ-КоА)-редуктазы — фермента, определяющего скорость биосинтеза холестерина, — играют важную роль в лечении АССЗ. С момента их внедрения в клиническую практику в 1980-е годы в ходе многочисленных исследований была продемонстрирована безопасность и эффективность терапии статинами для первичной и вторичной профилактики АССЗ [3–8].
Несмотря на это, применение статиновой терапии среди пациентов остается на низком уровне. Из-за опасений по поводу возможных побочных эффектов, которые усиливаются дезинформацией, распространяемой в СМИ, частота несоблюдения режима лечения и прекращения терапии статинами высока [9].
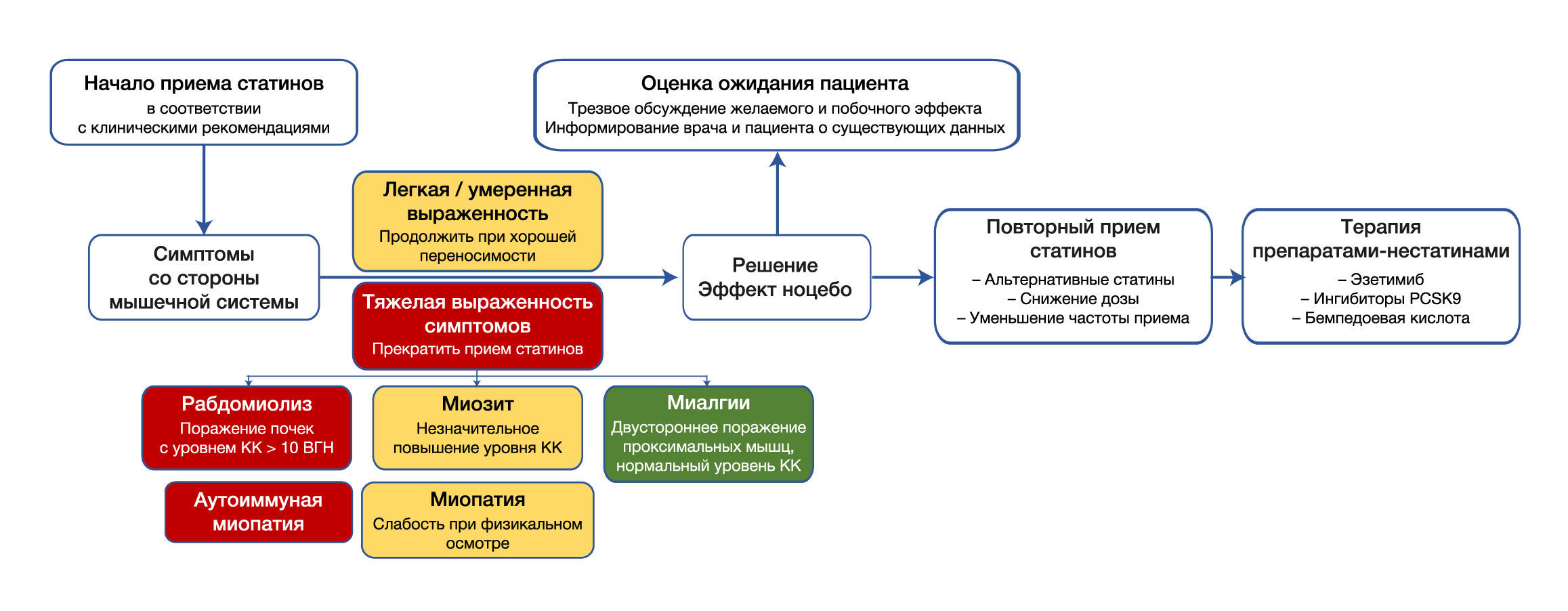
В данном обзоре обсуждаются стратегии лечения непереносимости статинов, и особое внимание авторы уделяют эффекту «ноцебо» — явлению, при котором ожидание отрицательного эффекта приводит к отрицательному результату (рис. 1).
Частота побочных эффектов, связанных со статинами
В целом, побочные эффекты лекарственных препаратов довольно распространены и способны привести к множеству негативных последствий, например, к стрессу у пациентов, несоблюдению режима лечения и прекращению приема лекарств, а также увеличению расходов на здравоохранение и использование медицинских услуг [10]. Оценки распространенности побочных эффектов, связанных со статинами, различаются между исследованиями, но, как правило, они выше в наблюдательных и когортных исследованиях (5–30 %) по сравнению с рандомизированными клиническими испытаниями (1–5 %).
Например, в рамках исследования «Предсказание мышечного риска в наблюдательных условиях» (PRIMO), обсервационного исследования, испытуемыми которого были более 7000 пациентов, получавших терапию статинами в высоких дозах, удалось показать, что 10,5% пациентов испытывали негативные симптомы со стороны мышечной системы (среднее время появления симптомов составило 1 месяц после начала приема статинов) [11]. Это было значительно выше, чем показатели 1–5 %, зарегистрированные в клинических испытаниях, проводимых в то время [12]. Аналогичным образом, в исследовании «Влияние статинов на функцию и активность скелетных мышц» (STOMP) 420 здоровых пациентов, ранее не принимавших статины, получали 80 мг аторвастатина по сравнению с плацебо в течение 6 месяцев [13]. Симптомы, соответствующие описанию миалгии, наблюдались у 9,4 % пациентов, принимавших аторвастатин, и у 4,6 % пациентов, принимавших плацебо, что позволяет предположить приблизительно 5%-ную частоту возникновения мышечных симптомов, связанных со статинами [14]. Согласно недавнему метаанализу, состоявшему из 176 исследований, где испытуемыми были более 4 миллионов человек, общая распространённость непереносимости статинов составляет 9,1 %. Аналогичная тенденция к снижению распространенности побочных эффектов, связанных со статинами, наблюдалась в рандомизированных контролируемых исследованиях (4,9% ) по сравнению с когортными исследованиями (17 %) [15].
Истинную частоту побочных эффектов, связанных со статинами, сложно определить из-за различий в определениях побочных эффектов в разных исследованиях, конкретных [для каждого исследования] критериев включения и исключения испытуемых в рандомизированных исследованиях, а также эффекта ноцебо — в частности, пациенты связывают все симптомы со стороны мышечной системы, возникающие во время исследования, с приемом статинов, исключая иные потенциальными причины. Однако к факторам риска развития побочных эффектов, связанных со статинами, относят:
- прием статинов в высоких дозах,
- пожилой возраст,
- женский пол,
- принадлежность к азиатским этносам,
- гипотиреоз,
- дефицит витамина D [16].
Симптомы поражения мышц, связанные со статинами
Из побочных эффектов, связанных со статинами, симптомы поражения мышц встречаются наиболее часто и широко освещены. Основной процент таких симптомов составляют миалгии, не связанные с повышением уровня креатинфосфокиназы (КФК). В типичную картину миалгий, провоцируемых статинами, входят двусторонние проксимальные мышечные поражения, которые начинаются через несколько недель или месяцев после начала приема статинов и исчезают после отмены. Миопатия, характеризующаяся объективной мышечной слабостью, и миозит с сопутствующим повышением уровня КФК наблюдаются реже [17].
Обнадеживает то, что серьезные побочные эффекты со стороны мышечной системы, связанные с приемом статинов, встречаются крайне редко. Рабдомиолиз, т.е. повышение уровня КФК более чем в десять раз выше верхней границы нормы с признаками поражения почек, встречается у < 0,1 % пациентов, принимающих статины [18]. Аутоиммунная миопатия, ассоциированная со статинами, встречается еще реже, с предполагаемой частотой 2–3 на 100 000. Она проявляется симметричной проксимальной мышечной слабостью наряду со значительным повышением уровня КК (более, чем в 10 раз превышена верхняя граница нормы; часто > 2000 МЕ/л), что сохраняется несмотря на прекращение терапии статинами. Подтверждением диагноза служит обнаружение аутоантител к ГМГ-КоА-редуктазе, а лечение заключается в терапии иммуносупрессорами [19].
Существует несколько предполагаемых механизмов развития мышечных симптомов, ассоциированных со статинами. Статины могут повышать восприимчивость скелетных мышц к миопатии посредством диссоциации FK506-связывающего белка от рианодинового рецептора 1 — канала высвобождения кальция из саркоплазматического ретикулума (СПР) — что приводит к спонтанному выходу кальция [из СПР]. Такая аномальная ситуация с выделением кальция впоследствии запускает проапоптотический сигналинг. Аномальное высвобождение кальция саркоплазматическим ретикулумом является частью миопатического механизма при таких заболеваниях скелетных мышц, как злокачественная гипертермия. Кроме того, терапия статинами увеличивает количество активных форм кислорода и азота, что также может влиять на активность рианодиновых рецепторов [20]. Известно, что статины снижают уровень коэнзима Q10, что, в свою очередь, способно влиять на функцию митохондрий [21].
Эффект ноцебо и отмена статинов
Хотя побочные эффекты лекарств часто обусловлены фармакологическим действием препарата, ожидания пациента также влияют на восприятие побочных эффектов. Эффект плацебо обусловлен позитивными ожиданиями, ведущими к субъективно-ощущаемому положительному результату; и наоборот, негативные ожидания могут привести к субъективно-ощущаемым неблагоприятным эффектам, что именуется эффектом ноцебо [22].
Дезинформация в СМИ сыграла важную роль в возникновении эффекта ноцебо, окружающего тему терапии статинами. Анализ новостных сообщений и интернет-запросов пользователей о статинах свидетельствует, что подавляющее большинство внимания уделяется риску, а не пользе от этих препаратов [9]. Это приводит к непропорционально высокому числу сообщений о предполагаемых побочных эффектах, связанных с терапией статинами.
Из-за распространенности предполагаемых побочных эффектов, связанных со статинами, частота самостоятельной отмены пациентами этих препаратов высока: по оценкам, 10 % пациентов прекращают терапию статинами после ее начала [23]. Продолжение гиполипидемической терапии остается критически важным для снижения риска АССЗ, поскольку общая продолжительность времени, в течение которого поддерживается сниженный уровень холестерина, так же важна, как и абсолютное снижение [концентрации] холестерина. Как сообщают Ньюман с соавт., ключевыми факторами отмены статинов являются страх развития побочных эффектов и дезинформация в СМИ или сведения, почерпнутые от друзей, членов семьи или из интернета [23]. Примечательно, что после периода интенсивного освещения в СМИ Великобритании побочных эффектов статинов, Мэтьюз с соавт. выявили увеличение числа пациентов, прекративших терапию статинами [24]. Было обнаружено, что такие высокие показатели самостоятельной отмены статинов приводят к неблагоприятным сердечно-сосудистым исходам [25, 26]. Кроме того, страх побочных эффектов является наиболее частой причиной, по которой люди отказываются начинать терапию статинами, несмотря на назначение врача [27].
Эффект ноцебо N-of-1 исследования
Эффект ноцебо был продемонстрирован в многочисленных рандомизированных клинических исследованиях и односубъектных исследованиях, в которых отдельные пациенты в ходе исследования переходили из экспериментальной группы в группу плацебо вслепую. Эти исследования продемонстрировали схожую частоту нежелательных явлений в группах статинов и плацебо [8].
Джой с соавт. воспользовались дизайном односубъектного исследования для оценки переносимости статинов в небольшом исследовании для подтверждения концепции. Восемь пациентов прошли курс лечения статинами и плацебо в случайном порядке. Каждый курс длился три недели с трехнедельным ликвидационным периодом. В качестве первичного исхода использовалась визуальная аналоговая шкала (ВАШ) с оценкой от 0 до 100, где 0 — отсутствие симптомов. У семи из восьми пациентов, участвовавших в исследовании, не наблюдалось значительного усиления миалгии (по шкале ВАШ) при лечении статинами по сравнению с плацебо, и в конечном итоге пять пациентов возобновили терапию статинами после рассмотрения открытых результатов со своим врачом [28]. Применение дизайна исследования с участием одного пациента для оценки миалгии, связанной с приемом статинов, послужило основой для последующих исследований.
SAMSON
Исследование SAMSON — это недавний реальный пример эффекта ноцебо, связанного с побочными эффектами статинов. В исследовании 60 пациентов, у которых ранее была замечена непереносимость статинов, получали или аторвастатин в дозе 20 мг, или плацебо, или не принимали никаких препаратов. Каждый курс лечения проводился в течение 1 месяца в случайной последовательности и в общей сложности в течение 12 месяцев; однако пациентам разрешалось прекращать прием таблеток досрочно, если наблюдались симптомы непереносимости.
Ежедневно пациенты с помощью приложения в смартфоне оценивали тяжесть симптомов по шкале от 0 до 100, где 0 соответствовал отсутствию симптомов. Первичным результатом был коэффициент ноцебо, который рассчитывался как разность интенсивности симптомов при приеме плацебо и интенсивности симптомов без лечения, поделенная на разность интенсивности симптомов при приеме статинов и без лечения. Результаты продемонстрировали коэффициент ноцебо 0,90, что соответствует 90 % симптомов, обусловленных статинами, также вызванных плацебо. Через 6 месяцев после завершения исследования половина пациентов возобновила терапию статинами [29].
Хотя усредненные показатели симптомов были значительно ниже в месяцы без приема таблеток (8,0) по сравнению со временем приема статинов (16,3) и плацебо (15,4), значимых различий между средними показателями симптомов в месяцы приема плацебо и статинов не наблюдалось. Также не наблюдалось различий в частоте прекращения приема препарата из-за непереносимости симптомов в месяцы приема статинов и плацебо (21,6 % и 17,2 % соответственно) [30]. В целом, эти результаты демонстрируют значимую роль негативных ожиданий пациентов в переносимости терапии статинами.
StatinWISE
Исследование побочных эффектов статинов на основе веб-технологий (StatinWISE) представляет собой серию исследований (с участием одного пациента), где сравнивалось лечение аторвастатином в дозе 20 мг с плацебо в шести рандомизированных двухмесячных периодах лечения [31]. Симптомы оценивались ежедневно по шкале (ВАШ) от 0 до 10, где 0 — отсутствие симптомов. Существенных различий между средними показателями мышечных симптомов в группах статинов и плацебо не наблюдалось.
Участники, завершившие шесть периодов лечения, получили индивидуальные результаты по завершении исследования. Большинство (88 %) пациентов сочли исследование полезным, а 66 % возобновили или изъявили желание возобновить прием статинов [31].
Исследования GAUSS
Безопасность и эффективность ингибитора пропротеинконвертазы субтилизин/кексин 9-го типа (PCSK9) эволокумаба у пациентов с непереносимостью статинов были продемонстрированы в исследовании GAUSS (Gal Achievement After Utilizing an Anti-PCSK9 Antibody in Statin-Intolerant Subjects — достижение целевого уровня холестерина у пациентов с непереносимостью статинов при применении антитела к PCSK9). Каждое из этих исследований продемонстрировало значительную эффективность ингибиторов PCSK9 в снижении уровня холестерина липопротеинов низкой плотности (ХС-ЛПНП) без чрезмерных побочных эффектов со стороны мышц по сравнению с плацебо, статином или эзетимибом.
В исследовании GAUSS-1 эволокумаб привел к снижению уровня ЛПНП на 41–63 % по сравнению с 15 % при применении эзетимиба, который в то время являлся предпочтительным гиполипидемическим средством для пациентов с непереносимостью статинов. В этом исследовании миалгия наблюдалась у 7,4 % пациентов, принимавших только эволокумаб, у 20,0 % пациентов, принимавших эволокумаб в сочетании с эзетимибом, и у 3,1 % пациентов, принимавших эзетимиб в сочетании с плацебо [32].
Результаты исследования GAUSS-2, в котором пациенты принимали препарат дважды в месяц, сравнивали с ежемесячным применением эволокумаба плюс плацебо (per os) и эзетимиба плюс плацебо (подкожно). Эволокумаб способствовал снижению уровня ХС-ЛПНП на 53–56 % от исходного значения и характеризовался меньшей частотой побочных эффектов, связанных с мышечной функцией, по сравнению с эзетимибом (12 % против 23 % соответственно) [33, 34].
Наконец, исследование GAUSS-3 было посвящено объективной оценке непереносимости статинов перед рандомизацией в группы эволокумаба или эзетимиба, в сравнении с данными о непереносимости статинов в анамнезе исследований GAUSS-1 и GAUSS-2. В первой фазе исследования пациенты получали 20 мг аторвастатина или плацебо. Те, у кого наблюдалось повышение уровня КК или побочные симптомы со стороны мышц при приеме аторвастатина, а не плацебо, впоследствии были рандомизированы во вторую фазу исследования, которая заключалась в лечении эволокумабом или эзетимибом в течение 24 недель [35].
В общей сложности у 42,6 % пациентов в группе аторвастатина наблюдались побочные эффекты, связанные с функцией мышц, по сравнению с 26,5 % в группе плацебо. Хотя частота побочных эффектов, связанных с мышечной функцией, была выше в группе приема статинов, больший процент пациентов с симптомами в группе плацебо вновь указывает на компонент эффекта ноцебо. Примечательно, что у более 80 % пациентов в этом исследовании ранее наблюдалась непереносимость трех или более статинов.
В итоге эволокумаб привёл к более выраженному снижению уровня ХС-ЛПНП, чем эзетимиб (52,8 % против 16,7 % соответственно). Побочные эффекты со стороны мышечной системы были схожими в обеих группах (20,7 % и 28,8 % в группах эволокумаба и эзетимиба соответственно); однако лишь у небольшого числа пациентов (0,7 % и 6,8 % соответственно) это привело к отмене исследуемого препарата [36].
ODYSSEY ALTERNATIVE
Аналогично GAUSS-3, в исследовании ODYSSEY ALTERNATIVE сравнивалась эффективность ингибитора PCSK9 алирокумаба и эзетимиба в контексте снижения уровня ХС-ЛПНП у пациентов с непереносимостью статинов. У испытуемых до начала исследования наблюдалась непереносимость двух или более статинов. Первоначально пациенты проходили четырехнедельный вводный период с плацебо (как перорально, так и подкожно). Пациенты, у которых не наблюдалось побочных эффектов со стороны мышц, были рандомизированы в группы, в которых проводилась 24-недельная терапия:
- алирокумабом плюс плацебо (перорально);
- эзетимибом плюс плацебо (подкожно);
- повторная провокационная терапия аторвастатином плюс плацебо (подкожно).
Применение алирокумаба приводило к более выраженному снижению уровня ХС-ЛПНП относительно исходного уровня (45,0 %) по сравнению с эзетимибом (14,6 %). Частота возникновения побочных эффектов со стороны мышц, приведших к отмене исследуемого препарата, была схожей у алирокумаба (15,9 %), аторвастатина (22,2 %) или эзетимиба (20,2 %).
После 24-недельного периода исследования у участников была возможность продолжить открытое лечение алирокумабом. В течение открытого периода только 2,1 % пациентов прекратили прием исследуемого препарата по причине нежелательных явлений со стороны мышц. Это вновь подчеркивает роль негативных ожиданий в контексте влияния на результаты лечения среди пациентов, поскольку частота прекращения приема исследуемого препарата была выше в период двойного слепого исследования, когда участники исследования были осведомлены о возможности рандомизации на терапию статинами [37].
Лечение непереносимости статинов
Лечение эффекта ноцебо
Механизмы, лежащие в основе эффекта ноцебо, изучены меньше, чем механизмы эффекта плацебо.
Ниже — перечень предполагаемых факторов, способствующих эффекту ноцебо:
- фрейминг (установление рамок) и вербальное внушение, как способ описания препарата;
- изучение опыта других людей или даже наблюдение за ними;
- классическое психологическое обусловливание, при котором нейтральные стимулы, ранее ассоциированные с неблагоприятным опытом, могут вызывать неблагоприятные последствия без фактического приема препарата.
Знание врачом этих концепций может предотвратить возникновение эффекта ноцебо.
В последующем необходимо выявить пациентов из группы повышенного риска, к примеру, пациентов с тревогой, депрессией или соматизированными расстройствами, провести оценку ожиданий пациента в отношении лечения, обсудить механизмы преодоления потенциальных побочных эффектов и перечислить желательные и нежелательные эффекты [10, 22, 38]. Поскольку чаще всего для поиска информации о лекарствах и болезнях пациенты используют интернет, крайне важно, чтобы медицинские работники предоставляли пациентам перечень научных ресурсов и с готовностью относились к тому, что пациенты уже могут быть дезинформированы. Данные о реальном использовании лекарств ясно показывают, что решения о назначении лекарств часто основаны на иррациональных предубеждениях [39]. Поэтому непрерывное обучение медицинских работников является ключевым компонентом улучшения приверженности лечению.
Режимы дозирования
Важно отметить, что у подавляющего большинства пациентов, которым повторно назначают статины после развития побочных эффектов, наблюдается переносимость данных препаратов [40]. Поэтому при возникновении симптомов непереносимости необходимо провести оценку обратимых причин, таких как увеличение физической активности, лекарственные взаимодействия, гипотиреоз и дефицит витамина D [41]. Если обратимая причина не выявлена, существуют различные стратегии для уменьшения побочных эффектов статинов. К ним относятся:
- временное прекращение терапии статинами с возобновлением приема того же статина после исчезновения симптомов;
- снижение дозы статина;
- переход на другой статин или
- уменьшение частоты приема статинов [42].
Часто даже изменение частоты приема не приводит к существенному изменению эффективности статинов. Например, аторвастатин и розувастатин имеют более длительный период полувыведения и, следовательно, их можно принимать реже. Например, Ruisinger с соавт. установили, что прием розувастатина в дозах от 2,5 до 20 мг всего один раз в неделю приводит к снижению уровня ХС-ЛПНП на 23 %, а хорошую переносимость проявили 74 % пациентов [43]. Важно отметить, что предоставление пациентам возможности выбора между этими вариантами может снизить эффект ноцебо [44].
Альтернативные препараты
Эзетимиб
Эзетимиб — ингибитор абсорбции холестерина в кишечнике, обычно является препаратом первой линии, который используется как добавление к терапии статинами для достижения целевых показателей снижения уровня ХС-ЛПНП [Arnett Circulation 2019]. Это обусловлено его доказанной переносимостью, а также эффективностью в снижении уровня ХС-ЛПНП примерно на 20 % [45]. Комбинации статина с эзетимибом оказывается достаточно для снижения уровня ХС-ЛПНП до уровня менее 70 мг/дл у большинства пациентов [17].
Ингибиторы PCSK9
В последнее время применение ингибиторов PCSK9 алирокумаба и эволокумаба продемонстрировало выраженное снижение уровня ХС-ЛПНП с низкой частотой побочных эффектов. PCSK9 секретируется гепатоцитами плазмы крови и связывается с рецептором ЛПНП, что приводит к лизосомальной деградации, снижению экспрессии рецепторов ЛПНП и уменьшению клиренса ХС-ЛПНП. У пациентов с семейной гиперхолестеринемией были выявлены мутации с усилением функции PCKS9, приводящие к повышению уровня ХС-ЛПНП и преждевременному развитию атеросклеротических сердечно-сосудистых заболеваний [46].
У пациентов с высоким риском развития АССЗ и уровнем ЛПНП более 70 мг/дл, несмотря на применение статинов, лечение эволокумабом приводило к снижению частоты серьезных неблагоприятных сердечно-сосудистых событий [47]. Прием алирокумаба с фоновой максимально переносимой дозой статина, плюс эзетимиб или без него, привел к снижению риска рецидивирующих ишемических событий у пациентов с острым коронарным синдромом [48]. Текущие рекомендации поддерживают применение ингибиторов PCSK9 в качестве дополнения к максимально переносимой гиполипидемической терапии, а именно статину плюс эзетимиб [17]. Использование терапии ингибиторами PCSK9 изначально было низким после одобрения FDA из-за высоких накладных расходов и частого отсутствия одобрения страховыми компаниями [49]. Со временем снижение годовой стоимости лечения и повышение осведомленности о требованиях к предварительному разрешению на ингибиторы PCSK9 обеспечили более широкий доступ к ингибиторам PCSK9 у пациентов с непереносимостью статинов [50].
Бемпедоевая кислота
Бемпедоевая кислота — это новый низкомолекулярный ингибитор АТФ-цитратлиазы (фермента, предшествующего ГМГ-КоА-редуктазе в пути биосинтеза холестерина). Препарат выпускается в форме пролекарства и активируется длинноцепочечной ацил-КоА-синтетазой 1, ферментом, обнаруженным в тканях печени [51]. Препарат продемонстрировал эффективность в плане снижения уровня ЛПНП у пациентов как с нормальной переносимостью, так и с непереносимостью статинов.
В ходе II фазы одного исследования у пациентов с непереносимостью статинов в течение 8 недель изучались результаты применения бемпедоевой кислоты в сравнении с плацебо. На протяжении всего исследования пациенты не принимали никаких других гиполипидемических средств. В группе, принимавшей бемпедоевую кислоту, снижение уровня ХС-ЛПНП было на 28,7 % выше, чем в группе плацебо. Примечательно, что три пациента (16 %) в группе плацебо прекратили прием исследуемого препарата из-за побочных эффектов со стороны мышц, в то время как в группе, принимавшей бемпедоевую кислоту, таких случаев не наблюдалось [52].
В III фазе исследования CLEAR-Serenity изучалась безопасность и эффективность бемпедоевой кислоты у пациентов с переносимостью статинов в анамнезе и с показаниями к гиполипидемической терапии для первичной или вторичной профилактики. Пациенты продолжали базовую гиполипидемическую терапию, которая заключалась в приеме статинов в очень низких дозах у части пациентов (9,9 % в группе плацебо, 7,7 % в группе бемпедоевой кислоты), при условии стабильности и переносимости. В этой группе применение бемпедоевой кислоты также привело к значительному снижению уровня ХС-ЛПНП по сравнению с плацебо, без значительного увеличения побочных эффектов со стороны мышц. Миалгия оказалась наиболее часто регистрируемым побочным эффектом со стороны мышц. Из-за нее прием исследуемого препарата пришлось отменить у 3,4 % пациентов, получавших бемпедоевую кислоту, по сравнению с 6,3 % пациентов, получавших плацебо [53].
В исследовании CLEAR-Harmony добавление бемпедоевой кислоты к максимально переносимой терапии статинами привело к значительному снижению уровня ХС-ЛПНП относительно с плацебо (снижение на 16,5 % от исходного уровня), без более высокой частоты нежелательных явлений по сравнению с плацебо у пациентов с установленным АССЗ и/или гетерозиготной семейной гиперлипидемией. Частота отмены препарата из-за побочных эффектов со стороны мышц была низкой в группе бемпедоевой кислоты и сопоставимой с частотой в группе плацебо (2,1 % и 1,9 %, соответственно). Примечательно, что достоверных различий частоты побочных эффектов со стороны мышц не было в зависимости от интенсивности фоновой статиновой терапии [54].
Баллантайн с соавт. продемонстрировали в III фазе двойного слепого рандомизированного контролируемого исследования следующее: добавление фиксированной комбинации бемпедоевой кислоты (180 мг) и эзетимиба (10 мг) к максимально переносимой терапии статинами приводит к снижению уровня ХС-ЛПНП на 38 % по сравнению с плацебо. Данное снижение уровня ХС-ЛПНП оказалось более выраженным, чем при применении только бемпедоевой кислоты (17,2 %) или только эзетимиба (23,2 %). Частота побочных симптомов со стороны мышц в группах была схожей. Эта фиксированная комбинация может быть особенно привлекательна для пациентов с непереносимостью статинов, поскольку степень снижения уровня ЛПНП приближается к таковой при умеренной или высокой интенсивности статинов [55].
В то время как удвоение дозы статинов приводит к снижению уровня ЛПНП примерно на 6 %, лечение бемпедоевой кислотой приводит к значительно более выраженному снижению уровня ЛПНП как в условиях монотерапии, так и в сочетании с другими гиполипидемическими препаратами и, что важно, не приводит к увеличению частоты побочных эффектов, связанных с функцией мышечной ткани, по сравнению с плацебо. Таким образом, бемпедоевая кислота — это новый вариант для пациентов с непереносимостью статинов, которым требуется снизить уровень ХС-ЛПНП в целях первичной или вторичной профилактики.
Инклисиран
Относительно недавно Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило инклисиран — ингибитор синтеза PCSK9 в печени, препарат на основе малой интерферирующей РНК (siRNA). Исследования ORION-10 и ORION-11 продемонстрировали, что добавление инклисирана к максимально переносимой гиполипидемической терапии привело к снижению уровня ХС-ЛПНП примерно на 50 % в сравнении с плацебо [56]. Хотя частота нежелательных реакций в месте введения была выше при применении инклисирана, чем в группе плацебо, достоверных различий в частоте миалгий между двумя группами не было [57]. Учитывая аспекты безопасности и переносимости, а также необходимость применения всего лишь один раз в 6 месяцев, инклисиран является перспективным препаратом для снижения уровня липидов.
Выводы
Побочные эффекты терапии статинами, в частности симптомы со стороны мышечной ткани, представляют собой часто встречающуюся клиническую проблему и в значительной степени подвержены эффекту ноцебо. Пациенты, сталкивающиеся с побочными эффектами, связанными со статинами, чаще прекращают терапию, что, в свою очередь, приводит к неблагоприятным сердечно-сосудистым исходам. В связи с этим врачам необходимо применять методы снижения эффекта ноцебо у пациентов. Краеугольным камнем является формирование у пациентов адекватных ожиданий с учетом того, что многие пациенты хорошо переносят терапию статинами при возобновлении приема этих препаратов. В перечень способов улучшения переносимости включают снижение доз, уменьшение частоты приема и клинические испытания альтернативных статинов. Для тех, у кого сохраняется непереносимость, существует множество альтернативных гиполипидемических препаратов, таких как бемпедоевая кислота и различные варианты ингибиторов PCSK9, которые могут использоваться самостоятельно или в сочетании со статинами и у которых хорошо изучены профили безопасности и эффективности в контексте лечения АССЗ.
