Почему нейроны живут долго? Механизм поддержания целостности генома нейронов

Геномная ДНК нейронов головного мозга нестабильна, и мутации, вызванные погрешностями репарации, могут привести к нарушению нейрогенеза и развитию нейродегенеративных заболеваний. Повреждение генома нейронов может быть вызвано как экзогенными, так и эндогенными факторами. Быстрая пролиферация нейрональных стволовых клеток во время эмбрионального развития мозга может привести к возникновению ошибок при удвоении генома. Электрическое возбуждение и резкие изменения экспрессии генов в функциональных нейронах создают риск повреждения геномной ДНК. Функцию нейронов поддерживает точная репарация повреждений ДНК, вызванных событиями, нарушающими стабильность геномной ДНК. Геномная целостность представляет собой сохранение последовательности и структуры ДНК. Молекулярные механизмы, поддерживающие геномную целостность, критически важны для здоровой работы нейронов. В настоящем обзоре авторы описывают недавний прогресс в понимании целостности генома функциональных нейронов, учитывая нарушения, наблюдаемые при неврологических заболеваниях.
1 Введение
Целостность геномной ДНК, включая последовательность нуклеотидов и структуру хроматина, необходима для выживания клеток и их нормальной физиологической функции. Кроме того, важную роль в поддержании целостности генома играют биохимические модификации, такие как метилирование ДНК, ассоциированные с гистонами эпигеномные модификации и другие трехмерные структуры ДНК. Для поддержания физиологических функций различных органов и здоровья человека особенно важно сохранение целостности генома в стволовых клетках, дающих начало дифференцированным клеткам, которые формируют каждый орган.
Геномная нестабильность может возникать даже в нормальных физиологических условиях. Повреждение ДНК, вызванное мутациями, влияет на физиологические функции клеток и приводит к системному ухудшению здоровья (Aguilera and García-Muse, 2013). Например, целостность генома нарушается в клетках злокачественных опухолей, что делает невозможным поддержание нормальной функции клеток, а также приводит к неконтролируемой пролиферации и метастазированию. Таким образом, механизмы, поддерживающие целостность генома, такие как регуляция хроматина и системы репарации ДНК, имеют решающее значение для поддержания нормальной клеточной функции. Решающее значение для профилактики и лечения заболеваний имеет более глубокое понимание этих механизмов, а также стратегий устранения геномных повреждений (Scheijen and Wilson, 2022). (В зависимости от определения нормы, мутагенез в раковых клетках усиливает способность их выполнять нормальные функции, здесь палка о двух концах, а также раковые клетки во многих случаях сложно назвать нормальными физиологическими условиями, и, следовательно, они не могут являться примером того, насколько важно для нормальных клеток поддержание целостности генома, и, если мы уже говорим о раке, то нам известно, что соматические мутации, увеличивающие приспособленность пролиферирующих клеток, являются фактором устойчивости к раку. — прим. ред.)
Было высказано предположение, что в зрелых нейронах мозга целостность генома не сохраняется (Zolzaya et al., 2024). От 13 до 41 % нейронов коры головного мозга человека демонстрируют вариации числа копий (CNV) генов (McConnell et al., 2013), а недавние исследования с использованием секвенирования нового поколения показали, что в геноме нейронов встречается множество более мелких вариаций последовательностей ДНК (Lodato et al., 2018; Luquette et al., 2022). Учитывая, что нейроны головного мозга имеют чрезвычайно долгую продолжительность жизни, а образование новых нейронов из нейрональных стволовых клеток ограничено, механизм, препятствующий нарушению стабильности генома и сохраняющий нормальную функцию нейронов, играет ключевую роль для здоровой работы мозга. (Если у нас у 41% нейронов изменения в количестве копий генов, то говорить о важности геномной стабильности в функционировании нейронов попросту бессмысленно. К этой цифре тоже есть вопросы - недавние исследования очень сильно подвергают сомнению ранние данные о соматическом мутагенезе в мозге, так, например, пристальное изучение ранее популярной гипотезы об активности Alu повторов в нервной ткани продемонстрировало практически полную артефактность эффекта. Авторов не смутило отсутствие воспроизведения результата с 2013 года. — прим. ред.)
2 Нестабильность генома нейронов
Для эффективной передачи информации в нервной системе нейроны должны поддерживать высокую метаболическую активность. Для производства энергии, необходимой для своей деятельности, мозг потребляет около 25 % глюкозы организма (Steiner, 2019; Trigo et al., 2022). Зрелые нейроны в своих митохондриях производят 4,7 миллиарда молекул аденозинтрифосфата (АТФ) в секунду. В ходе этого процесса 1–3 % кислорода преобразуется в активные формы кислорода (АФК), которые могут нарушать стабильность геномной ДНК (Salehi et al., 2018). В результате нейроны сталкиваются с более высоким риском нестабильности генома, чем другие соматические клетки (Zhu et al., 2012; Magistretti and Allaman, 2015). Прежде всего, повреждение геномной ДНК может происходить в рамках нормальных физиологических функций мозга. Например, количество двуцепочечных разрывов (ДЦР) увеличивается в энторинальной коре, теменной коре и зубчатой извилине при исследовании новой среды (Suberbielle et al., 2013). Кроме того, количество ДЦР возрастает в первичной зрительной коре при освещении глаз в течение 15 минут (Suberbielle et al., 2013) и в гиппокампе во время формирования памяти у мышей (Castro-Pérez et al., 2016).
Помимо физиологической активности, геном нейронов чрезвычайно восприимчив к повреждениям, вызванным токсичным действием наркотиков (Sanchez-Aceves et al., 2024; Torre et al., 2021; Calls et al., 2021). Было показано, что употребление алкоголя приводит к накоплению в нейронах ДЦР (Rulten et al., 2008). Неоднократное введение кокаина мышам вызывает гиперацетилирование гистонов в 1696 локусах прилежащего ядра (Renthal et al., 2009), что приводит к повреждению ДНК во многих областях мозга (de Souza et al., 2014). Метамфетамин, непрямой адреномиметик, также вызывает повреждение геномной ДНК нейронов (Johnson et al., 2015; Tokunaga et al., 2008).
Активность нейронов индуцирует экспрессию ранних генов (IEG — immediate early genes), которые играют важную роль в нейрональной пластичности (Yap and Greenberg, 2018). Нарушение регуляции IEG приводит к различным неврологическим расстройствам (Ebert and Greenberg, 2013). Быстрая регуляция IEG опосредована физическим контактом между энхансером и промотором посредством одноцепочечных разрывов (ОЦР) или ДЦР в геномной ДНК (Madabhushi et al., 2015; Wu et al., 2021; DelintRamirez et al., 2022). Тем не менее неоднократные ОЦР и ДЦР, сопровождающиеся изменениями трехмерной структуры генома, могут вызывать физиологическое нарушение функции нейронов (Dileep et al., 2023). (Энхансер-промоторные контакты совершенно не требует двуцепочечных разрывов. ДНК обладает гибкостью. Это молекулы в растворе - они могут взаимодействововать в трёх измерениях. Само заявление, что именно путём разрезания и перетаскивания встречаются промотор и энхансер не находит потверждения в статьях, на которых ссылаются авторы — прим. ред.)
Эпигеномные модификации нейронов необходимы для функций памяти и обучения в головном мозге (Zovkic et al., 2013). В ходе развития мозга происходит метилирование ДНК, модифицирующее цитозины в CpG-островках. За метилирование вновь синтезированных цепей ДНК после репликации отвечает ДНК-метилтрансфераза DNMT1 (Li et al., 1992), в то время как DNMT3A регулирует экспрессию генов в ответ на те или иные клеточные условия (Wei et al., 2021; Li et al., 2022). DNMT3B, с другой стороны, участвует в метилировании генов, специфичных для Х-хромосомы (Yagi et al., 2020). Белки, связывающиеся с метилированной ДНК, могут вызывать структурные изменения хроматина, подавляя транскрипцию регулируемых ими генов. Поскольку при различных злокачественных новообразованиях паттерны метилирования ДНК нарушаются, мутации DNMT могут дестабилизировать геном (Valencia and Kadoch, 2019). Например, контекстуальная выработка условного рефлекса, связанного с переживанием чувства страха (КВРС), увеличивает экспрессию DNMT в нейронах гиппокампа, а ингибирование DNMT снижает условную память и подавляет долговременную потенциацию (ДВП) в боковой ветви Шеффера (Levenson et al., 2006). (Путают причину и следствие - нарушение функции метилтрансферазы в раковых клетках не обязательно является причиной трансформации здоровой клетки, а может быть связано с буквально чем угодно. Гиппокамп также не является формой рака, и поэтому не может быть примером нарушения функции метилтрансферазы в раке, а долговременная потенциация не является характерным примером нейропластичности. — прим. ред.) Таким образом, регуляция метилирования ДНК играет важную роль в нейрональной пластичности. Кроме того, наблюдаются различия в уровнях метилирования ДНК у нейронов с разными проекционными зонами в центральной нервной системе (Zhang et al., 2021; Zhou et al., 2023).
Регуляторный процесс эпигеномной модификации включает репарацию ДНК с заменой оснований ферментами семейства TET (Ten-Eleven Translocation): TET1, TET2 и TET3. Ферменты TET важны для активации деметилирования ДНК, включающего окисление 5-метилцитозина до 5-гидроксиметилцитозина (Zhang et al., 2023). Было показано, что у мышей с нокаутом TET1 нарушены пространственное обучение и кратковременная память (Zhang et al., 2013); это позволяет предположить, что для нормальной работы нейронов необходимо поддержание целостности генома посредством регуляции эпигеномных модификаций. (Влияние нокаута TET1 одновременно на деметилирование и на память не является доказательством влияния метилирования на память, максима "один белок - одна функция" не кажется устойчивой к современным знаниям. — прим. ред.)
В большинстве органов клетки с нарушениями функции удаляются посредством апоптоза или фагоцитоза, а утраченные клетки замещаются благодаря регенеративным механизмам. Однако в головном мозге постнатальный нейрогенез ограничен лишь несколькими областями, такими как зубчатая извилина гиппокампа. Регенерирующие нейроны могут фагоцитироваться микроглией (Butler et al., 2021), однако механизм удаления нейронов в ответ на мутации в их геноме остается неясным. Геномные мутации во многих типах клеток часто приводят к появлению у этих клеток аберрантных характеристик. Такие клетки, как правило, либо подвергаются апоптозу с участием p53, либо элиминируются иммунной системой (Attardi, 2005; Szybinska and Lesniak, 2017). Однако мутантные клетки, преодолевшие эти защитные системы, могут начать пролиферировать, что в конечном итоге приводит к злокачественному росту. Напротив, нейроны редко приобретают пролиферативный потенциал. Таким образом, вполне вероятно, что аномальные нейроны продолжат находиться в мозге, внося вклад в нейронную активность, на протяжении всей своей жизни в организме человека.
Геномная нестабильность также возрастает в нейронах с возрастом. Например, сравнительное геномное секвенирование ДНК нейронов префронтальной коры и гиппокампа людей в возрасте от четырех месяцев до 82 лет выявило зависимую от возраста мутацию (Lodato et al., 2018). В нейронах головного мозга с возрастной нейродегенерацией обнаруживается больше мутаций, чем в нейронах здорового мозга (Li et al., 2023). Накопление повреждений геномной ДНК в нейронах приводит к различным нейродегенеративным заболеваниям (Rass et al., 2007). Например, в нейронах пациентов с болезнью Альцгеймера на ранних стадиях наблюдается повышенное накопление двуцепочечных разрывов (ДЦР), что было отмечено в посмертных исследованиях мозга (Suberbielle et al., 2013; Wu et al., 2021; Madabhushi et al., 2015; Reid et al., 2021). Многочисленные исследования дают основания полагать, что возрастная потеря геномной целостности, предположительно, способствует патогенезу болезни Альцгеймера (Weissman et al., 2009; Kruman et al., 2004; Iourov et al., 2009; Herrup et al., 2013).
Мутации в молекулах основного компонента ответа на повреждение ДНК (DDR — DNA damage response) связаны с синдромами хромосомной нестабильности у человека (McKinnon, 2017; Shiloh, 2003). Например, атаксия-телеангиэктазия вызывается мутациями в гене ATM, продукт которого задействован в ответе клетки на появление ДЦР (Shiloh and Rotman, 1996). Мутации в гене MRE11, участвующем в обнаружении ОЦР, также встречаются при синдроме, сходном с атаксией-телеангиэктазией (Stewart et al., 1999). Сходным образом, мутации в гене XRCC1, участвующие в восстановлении ОЦР, вызывают паралич глазодвигательного нерва, аксональную нейропатию и прогрессирующую мозжечковую атаксию (Hoch et al., 2017; O’Connor et al., 2018).
3 Механизмы защиты целостности генома нейронов
Как описано выше, функциональные нейроны часто повреждаются в результате клеточного метаболизма, передачи нервного импульса и регуляции экспрессии генов, которые отвечают за физиологические функции здорового мозга. Обеспечение долгосрочного сохранения целостности генома и функциональности нейронов достигается за счет специфических механизмов (Lyu et al., 2022). Недавние данные, полученные в результате изучения заболеваний и экспериментальных исследований, показали, что на целостность генома нейронов влияют такие структуры ДНК, как R-петли, G-квадруплексы и «длинные гены», и эти структуры строго регулируются ферментами, в частности, топоизомеразами и хеликазами (рисунок 1).
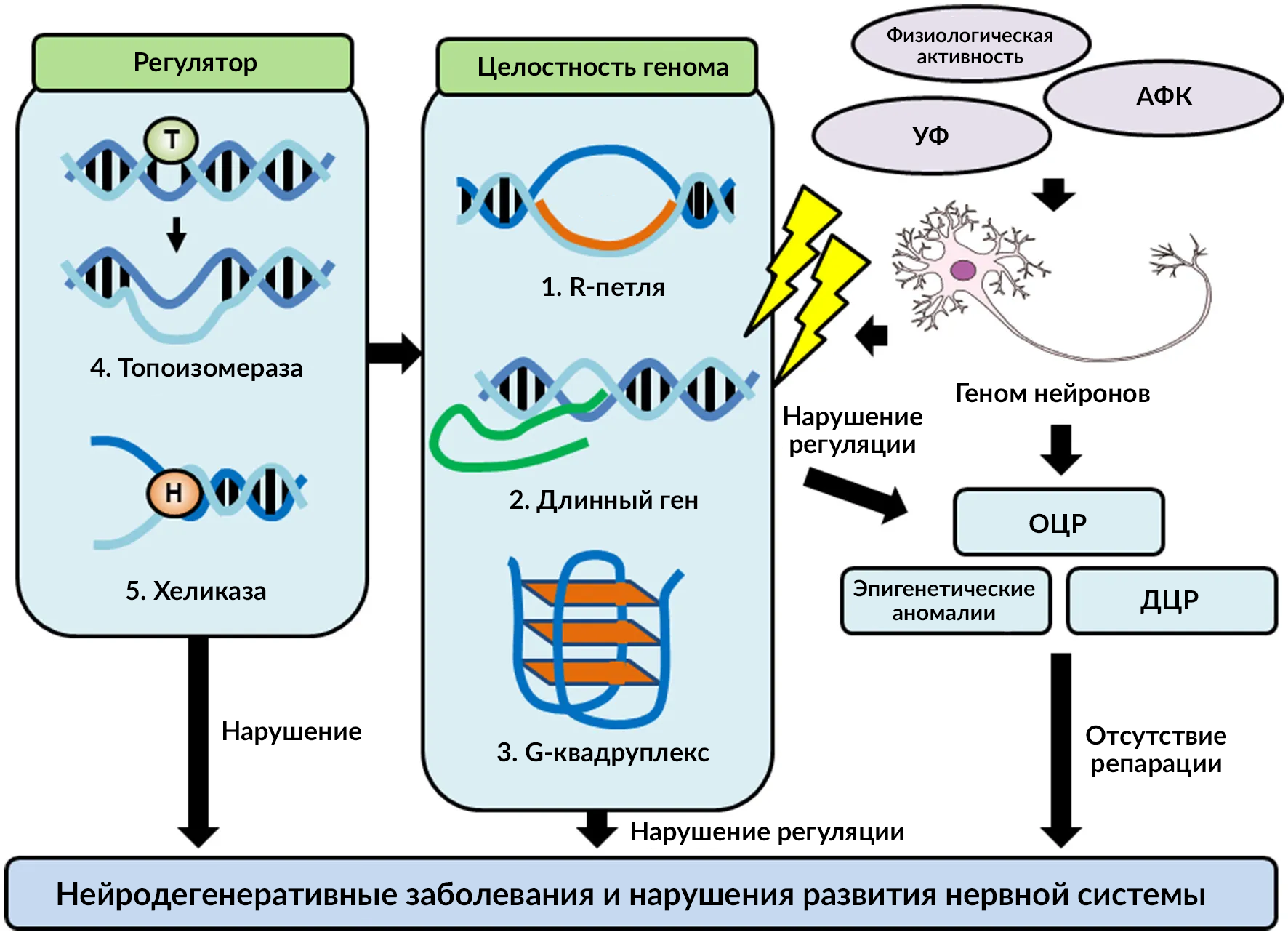
3.1 R-петля
В ходе экспрессии гена между матричной геномной ДНК и синтезируемым РНК-транскриптом образуется гибрид ДНК–РНК, в результате чего нематричная ДНК остается одноцепочечной. Такая структура называется R-петлей. Если R-петля не удаляется надлежащим образом сенатаксином или РНКазой H, это приводит к появлению аномалий в репликативных вилках и накоплению повреждений ДНК. Кроме того, R-петли влияют на различные биологические процессы, включая транскрипцию, трансляцию и механизмы репарации ДНК. Нарушение регуляции R-петель связано с развитием ряда неврологических заболеваний (Groh and Gromak, 2014; Skourti-Stathaki et al., 2011; Sollier and Cimprich, 2015; Loomis et al., 2014). Аномальное накопление R-петель способствует появлению таких заболеваний, как атаксия-телеангиэктазия (Groh and Gromak, 2014; García-Muse and Aguilera, 2019), боковой амиотрофический склероз (БАС/ALS; Salvi and Mekhail, 2015), атаксия-окуломоторная апраксия (Fogel et al., 2014; Becherel et al., 2015) и спинальная мышечная атрофия (Kannan et al., 2018; Hensel et al., 2020). Недавние исследования показали, что R-петля участвует в регуляции экспрессии NPAS4 в ответ на хронический психосоциальный стресс или употребление кокаина (Akiki et al., 2024). Таким образом, R-петля также участвует в немедленной реакции нейронной активности; другие физиологические функции R-петли еще предстоит выяснить.
Одноцепочечная ДНК в R-петле уязвима для ОЦР вследствие ее восприимчивости к нуклеазам (Allison and Wang, 2019). Кроме того, R-петли формируют области отрицательно и положительно сверхспирализованных структур ДНК вблизи точек начала транскрипции, создавая барьеры для элонгации (Zardoni et al., 2021), участвуя в эпигеномной регуляции (Ginno et al., 2012) и влияя на пути репарации ДНК (Keskin et al., 2014). Чтобы преодолеть этот барьер, клетки временно расщепляют и вновь соединяют цепи ДНК с помощью топоизомераз, снимая торсионное напряжение (Saunders et al., 2006; Le et al., 2019).
В делящихся дрожжах (Ohle et al., 2016) и иммортализованных клеточных линиях человека (клетки RPE-hTERT; Yasuhara et al., 2018) RAD52 распознает R-петлю как ориентир для репарации, в то время как XPG-хеликаза удаляет ее, чтобы активировать репарацию путем гомологичной рекомбинации (РГР). Однако у нейронов отсутствуют эффективные механизмы РГР для репарации ДНК. Например, при спорадическом БАС репарация ДЦР снижена из-за аномальной субклеточной локализации TDP-43 в мотонейронах. TDP-43 быстро накапливается в местах расположения ДЦР в нейронах и способствует сборке факторов, которые участвуют в репарации ДНК, — в частности, в негомологичном соединении концов (NHEJ — nonhomologous end-joining; Orii et al., 2006; Mitra et al., 2019). Это наблюдение дает основание предполагать, что в нейронах молекулярный аппарат является одним из механизмов репарации ДНК в метаболизме R-петли.
3.2 G-квадруплекс
G-квадруплекс (G4) — это структура высшего порядка в молекулах нуклеиновых кислот, образующаяся в результате формирования хугстеновских водородных связей между остатками гуанина (Monsen et al., 2022). Такие структуры обладают высокой стабильностью и играют важную роль в регуляции транскрипции, репликации, определении сайта ДЦР, поддержании стабильности генома и метаболизме РНК (Hänsel-Hertsch et al., 2017; Fay et al., 2017). В частности, в нейронах функция G4 состоит в регуляции экспрессии продуктов соответствующих генов. Так, например, работает G4 в промоторе тирозингидроксилазы — ключевого скорость-лимитирующего фермента биосинтеза катехоламиновых нейромедиаторов (Banerjee et al., 2014). Фактически избирательное разрушение таких G4 путем мутации промоторных последовательностей ДНК влияет на транскрипцию тирозингидроксилазы (Banerjee et al., 2014). Иммуногистохимический анализ мозга взрослых мышей показывает, что G4 широко распространен в нейронах всех его отделов, включая обонятельную луковицу, пирамидные нейроны гиппокампа, зернистые клетки зубчатой извилины и нейроны Пуркинье мозжечка (Asamitsu et al., 2020; Comptdaer et al., 2024). Интересно, что распределение G4 в ядре нейронов весьма динамично. Иммуногистохимическая окраска G4 показала меньшее количество G4 в глиальных клетках, чем в нейронах, что указывает на особенно высокую активность формирования G4 именно в нейронах (Asamitsu et al., 2020).
Структурный анализ продемонстрировал, что хеликаза DHX36, принадлежащая к семейству DExD/H box, разрешает структуру G4 (Chen et al., 2018). Полногеномное выявление G4 с помощью секвенирования G4-ДНК показывает, что DHX36 устраняет G4 и восстанавливает экспрессию генов, подавляемую при запоминании страха у мышей, подвергавшихся воздействию электрического тока в сочетании со звуковыми стимулами, с последующим восстановлением памяти о страхе, вызванном воздействием только звуковых стимулов (Marshall et al., 2024). Тем не менее в нейрональных клетках-предшественниках стабилизация G4 способствует апоптозу, вызванному повреждением ДНК (Watson et al., 2013). Сходным образом, в нейронах крыс стабилизация G4 подавляет экспрессию гена Brca1, необходимого для репарации ДНК, и вызывает накопление ДЦР (Moruno-Manchon et al., 2017). Мутации в гене ATRX стабилизируют G4 и способствуют накоплению повреждений ДНК (Wang et al., 2019). G4 можно обнаружить с помощью анализа задержки электрофоретического сдвига в геле. Хеликаза ATRX связывается с геномной ДНК и, как предполагается, играет роль в разрешении G4 по всему геному и ослаблении их неблагоприятных эффектов (Law et al., 2010).
3.3 «Длинные гены»
Дефектные формы MECP2 — белка, подавляющего экспрессию генов путем связывания с метилированной ДНК, — приводят к нарушению функции синапсов и вызывают синдром Ретта. Исследования мозга пациентов с синдромом Ретта и работы на мышиных моделях показали, что дефицит MECP2 увеличивает экспрессию «длинных генов», охватывающих более 100 тыс. пар нуклеотидов по всему геному и продукты которых связаны с синапсами (Sugino et al., 2014; Gabel et al., 2015). Примечательно, что в нейронах по сравнению с другими типами клеток обнаруживается значительно более высокий уровень экспрессии «длинных генов» (Gabel et al., 2015). Экспрессия «длинных генов» велика в лобной доле и миндалевидном теле, где она связана с нарушениями развития нервной системы, такими как аутизм (Gabel et al., 2015). Кроме того, среди всех клеток, образующих головной мозг, экспрессия еще более «длинных» генов специфична именно для нейронов (Zylka et al., 2015).
«Длинные гены» также участвуют в развитии других неврологических заболеваний. Локусы TDP-43 и FUS/TLS отвечают за развитие за бокового амиотрофического склероза; с них транскрибируются РНК-продукты длиной более 100 тыс. пар нуклеотидов (LagierTourenne et al., 2012; Polymenidou et al., 2011). Сходным образом, CNTNAP2, другой «длинный ген», участвует в развитии аутизма (Peñagarikano and Geschwind, 2012). Терапия с применением ингибитора топоизомеразы топотекана устраняет гиперэкспрессию «длинных генов» в моделях синдрома Ретта (Mabb et al., 2014; King et al., 2013).
В нейронах дрозофилы старение приводит к накоплению R-петель в «длинном гене» и этот топологический стресс снимается ферментом Top3B (Jauregui-Lozano et al., 2022). Для нейронов характерно, что «длинные гены» формируют особенно сложные переплетения ДНК и РНК, участвующие в регуляции генома. Для поддержания геномной целостности нейронов топоизомераза и различные хеликазные комплексы работают совместно, регулируя ОЦР и ДЦР в составе «длинных генов» (Zagnoli-Vieira and Caldecott, 2020).
3.4 Топоизомераза
Топоизомераза (Top) играет важную роль в стабилизации генома и снятии топологического напряжения цепях ДНК. Значительное количество исследований подчеркивает роль Top во время репликации. Она устраняет суперспиральную структуру, предотвращая появление разрывов в ДНК. Ингибиторы Top широко изучаются в качестве противоопухолевых агентов, поскольку они вызывают разрывы ДНК, летальные для пролиферирующих клеток (Pommier et al., 2022). Даже в непролиферативных нейронах Top важна для поддержания целостности генома, участвуя в восстановлении структур R-петли и G4, образующихся в процессе экспрессии генов. Нарушение регуляции различных ферментов Top связано с нейродегенеративными заболеваниями и нарушениями развития нервной системы, такими как аутизм, интеллектуальные расстройства, шизофрения и деменция (Katyal et al., 2014; Neale et al., 2012; Stoll et al., 2013; Tiwari and Wilson, 2019; Fragola et al., 2020; Milano et al., 2024; Crewe and Madabhushi, 2021). Например, мутации Top3B связаны с аутизмом (Stoll et al., 2013; Iossifov et al., 2012), психическими расстройствами (Ahmad et al., 2017a; Stoll et al., 2013), шизофренией (Xu et al., 2012) и когнитивной дисфункцией (Kaufman et al., 2016).
Топоизомераза 2β (Top2B) также играет уникальную роль в нейрогенезе. Хотя делеция Top2B не влияет на образование нейронов, она нарушает рост аксонов мотонейронов вентральных рогов спинного мозга (Yang et al., 2000). Как правило, в эмбриональных стволовых клетках с дефицитом Top2B не выявляются дефекты пролиферации или нейрональной дифференцировки (Tiwari et al., 2012). В зернистых нейронах мозжечка обработка ингибитором Top2B усиливает экспрессию 18% детектируемых транскриптов (Tsutsui et al., 2001). В стимулированных нейронах Top2B регулирует экспрессию генов, индуцируя ДЦР в IEG (Tsutsui et al., 2001). Следовательно, регуляция структуры геномной ДНК с помощью Top необходима для дифференцировки и функции нейронов.
Топоизомераза 1 (Top1) участвует в процессе транскрипции, снимая супервитки в молекуле ДНК, что способствует образованию R-петли (Drolet et al., 1995; El Hage et al., 2010). Однако дефицит Top1 также усиливает топологический стресс и способствует образованию R-петли, что позволяет предположить, что фермент Top участвует как в формировании, так и в разрешении R-петли (Promonet et al., 2020). Top3B, которая, как и Top1, относится к Top I типа, уникальна тем, что может работать как с ДНК, так и с РНК (Ahmad et al., 2017a,b; Saha et al., 2020). Известно, что функциональное ингибирование Top3B повреждает R-петлю, что приводит к снижению функции нейронов, тогда как гиперэкспрессия Top3B приводит к ее повышению (Skourti-Stathaki and Proudfoot, 2014). Мутантная Top3B с пониженной ферментативной активностью вызывает накопление в геноме R-петель (Huang et al., 2018). После связывания с R-петлей Top3B взаимодействует с DDX5, устраняя эту структуру (Saha et al., 2022a).
Топоизомеразы также взаимодействуют с ДНК посредством расщепления комплексов. Например, Top1 ковалентно связывается с 3'-концом при расплетании ДНК, и такой промежуточный продукт реакции (комплекс с ДНК) называется комплексом расщепления Top1 (комплекс расщепления топоизомеразы 1; Top1cc); комплекс Top2 с ДНК называется Top2cc (Wojtaszek and Williams, 2024). Если эти комплексы не разрешаются в процессе репарации ДНК, они могут вызывать в ней дополнительные повреждения. Top1cc удаляется из ДНК благодаря ферментативной активности тирозил-ДНК-фосфодиэстеразы 1 (TDP1), а мутации в TDP1 вызывают спиноцеребеллярную дегенерацию (El-Khamisy et al., 2005; Takashima et al., 2002). Сходным образом, это же заболевание может вызываться мутациями в TDP2, устраняющей Top2cc (Gómez-Herreros et al., 2014).
3.5 Хеликаза
Хеликаза представляет собой фермент, который разрывает водородные связи между основаниями цепей ДНК и РНК с затратой АТФ и диссоциирует цепи нуклеиновых кислот. В нейронах специфические хеликазы, такие как DHX36 и ATRX, отвечают за структуру G4 в геноме, в то время как DDX5 участвует в разрешении R-петли (Saha et al., 2022a). Примечательно, что снижение экспрессии DDX21 в первично культивируемых кортикальных нейронах приводит к накоплению G4 и повреждений в геномной ДНК (Lyu et al., 2022). DDX21 также играет роль в устранении R-петель (Song et al., 2017). Поскольку хеликазы могут расплетать как гибриды ДНК–ДНК, так и ДНК–РНК, они являются важными факторами поддержания целостности генома. Однако функциональная специфичность примерно 100 хеликаз в геноме человека до сих пор в значительной степени неизвестна. Многие хеликазы работают совместно с Top, что позволяет предположить, что эти комплексы формируются для сохранения целостности генома (Tsukada et al., 2024; Tan et al., 2023; Saha et al., 2022b; Gupta et al., 2022; Yang et al., 2020). Уникальные и/или специфические функции каждой хеликазы еще предстоит выяснить.
4 Заключение
Здоровому мозгу требуется поддерживать целостность генома, необходимую для функционирования нейронов. Однако нарушение стабильности генома представляет собой постоянную проблему, возникающую из-за ежедневного стресса, физиологической активности нейронов и накопления повреждений ДНК (Zolzaya et al., 2024). Мутации также могут возникать в геноме нейронов в процессе нормального роста и старения человека. Другими словами, восстановление геномной ДНК нейронов часто происходит не полностью, что приводит к неизбежным повреждениям генома и возможным последствиям для функции нейронов. Это постоянное напряжение, связанное с поддержанием жизнеспособности долгоживущих нейронов в ходе роста и старения организма, повышает риск развития нейродегенеративных и психических заболеваний, при которых повторяющиеся повреждения ДНК и структурные изменения генома нарушают работу нервной системы.
Недавние исследования дают основания полагать, что защитным механизмом для специфической для нейронов геномной целостности может быть действие обширной молекулярной сети топоизомераз, хеликаз и факторов, участвующих в репарации ДНК в ответ на изменения структуры геномной ДНК нейронов, включая R-петли, G4 и регуляцию «длинных генов». Технологические инновации позволили анализировать функции этих молекул в целом геноме, а достижения в методах масс-спектрометрии дали возможность всесторонне идентифицировать более крупные молекулярные сети. Анализируя молекулы, необходимые для сохранения геномной целостности, можно выяснить, как молекулярные сети отвечают за функционирование нейронов по всему геному, тем самым раскрывая динамику генома нейронов и связывая нарушения в этой сети с различными неврологическими заболеваниями.
