Фармакология антисмысловых препаратов
Франк Беннетт, Бренда Ф. Бейкер, Нгуен Фам, Эрик Суэйзи и Ричард С. Гири
Ключевые слова: антисмысловые олигонуклеотиды, этеплирсен, мипомерсен, нусинерсен, олигонуклеотид, патисиран, РНК, интерференция РНК, сплайсинг РНК, РНКаза H
Аннотация
Результаты последних исследований показали, насколько значительны и разнообразны роли РНК в поддержании функций клетки, а также определили вклад РНК в развитие патологий, что способствовало расширению спектра потенциальных терапевтических мишеней. Наиболее прямое и избирательное воздействие на РНК-мишень оказывают антисмысловые нуклеотиды, на основе которых сформировалась технология разработки лекарств. Антисмысловые нуклеотиды могут влиять на РНК клеток несколькими путями: разрушая РНК-мишень или же изменяя её функции. Обладая различными механизмами воздействия, антисмысловые препараты демонстрируют возможность терапии широкого ряда заболеваний. Данный обзор освещает некоторые преимущества внедрения антисмысловых препаратов в клиническую практику.
Примечание редакции: для вашего удобства мы перевели таблицу в PDF. Нажимайте на «Таблица 1» для того, чтобы открыть PDF в новом окне.
ВВЕДЕНИЕ
Создание антисмысловых препаратов позволяет разрабатывать лекарства на основе малых молекул и белков, обладающие дополнительным механизмом действия – направленностью действия не на белки, а на РНК. Такие терапевтические стратегии позволяют расширить число и спектр мишеней для разработки новых методов лечения. Возможно создание антисмысловых препаратов, связывающихся с такими труднодоступными мишенями, как РНК, кодирующие каркасные белки, или транскрипционные факторы, некодирующие РНК и РНК, токсичные для клеток. Кроме того, такие технологии эффективны и выгодны для медицинской геномики и генетики, поскольку они позволяют создать препараты для лечения как моногенных, так и полигенных заболеваний. Использование (назначение) мипомерсена (mipomersen) в качестве терапевтического средства при семейной гиперхолестеринемии подтвердило эффективность антисмысловых препаратов для лечения системных заболеваний [1]. Кроме того, многочисленные клинические испытания показали возможность безопасного применения антисмысловых препаратов для лечения пациентов с использованием различных методов. На сегодняшний день антисмысловые препараты в клинической практике могут оказывать как системные, так и местные эффекты на различные ткани (Таблица 1). Достижения в области химии олигонуклеотидов позволят в дальнейшем усовершенствовать антисмысловые препараты, повысив их активность, безопасность и уровень распределения в тканях. Технологиям антисмысловых препаратов посвящены некоторые свежие обзоры [см. 2–5]. Данный обзор рассматривает достижения, благодаря которым антисмысловые препараты успешно проходят клинические испытания и применяются непосредственно для лечения пациентов.
МЕХАНИЗМЫ ДЕЙСТВИЯ АНТИСМЫСЛОВЫХ ПРЕПАРАТОВ
В данном обзоре авторы дают следующее определение антисмысловых олигонуклеотидов (АСО): это олигонуклеотиды, связывающиеся с РНК по принципу комплементарности и, таким образом, изменяющие функцию РНК-мишени. Такое определение объединяет множество типов олигонуклеотидов и различные механизмы их воздействия на РНК после связывания (детально рассмотрены в источниках 3 и 6). Вкратце, механизмы действия АСО можно разделить на две группы: 1) связывание с РНК и нарушение их функции, без содействия её разрушению, например, остановка трансляции или изменение процессинга РНК и 2) ускорение разрушения РНК при помощи эндогенных ферментов, таких как РНКаза H или Argonaute-2 [данный механизм носит название РНК-интерференция (RNAi)] (Рисунок 1). В недавних исследованиях было показано, что АСО также способны усиливать продукцию белков либо путём антагонизма с микроРНК, в норме подавляющими продукцию белка, либо путём маскировки открытой рамки считывания на 5′-концевом участке [7–9].
ТЕРАПЕВТИЧЕСКАЯ ХИМИЯ АНТИСМЫСЛОВЫХ ОЛИГОНУКЛЕОТИДОВ
В биологических системах немодифицированные ДНК и РНК по своей природе нестабильны, так как подвергаются воздействию повсеместно экспрессирующихся нуклеаз. Для применения олигонуклеотидов в качестве антисмысловых препаратов, необходимо их модифицировать таким образом, чтобы сохранить или улучшить их способность комплементарно связываться с РНК, повысить устойчивость к расщеплению нуклеазами, обеспечить распределение в тканях и доставить в тот же клеточный компартмент, где находятся РНК-мишени. Для этих целей используется несколько различных химических методов.
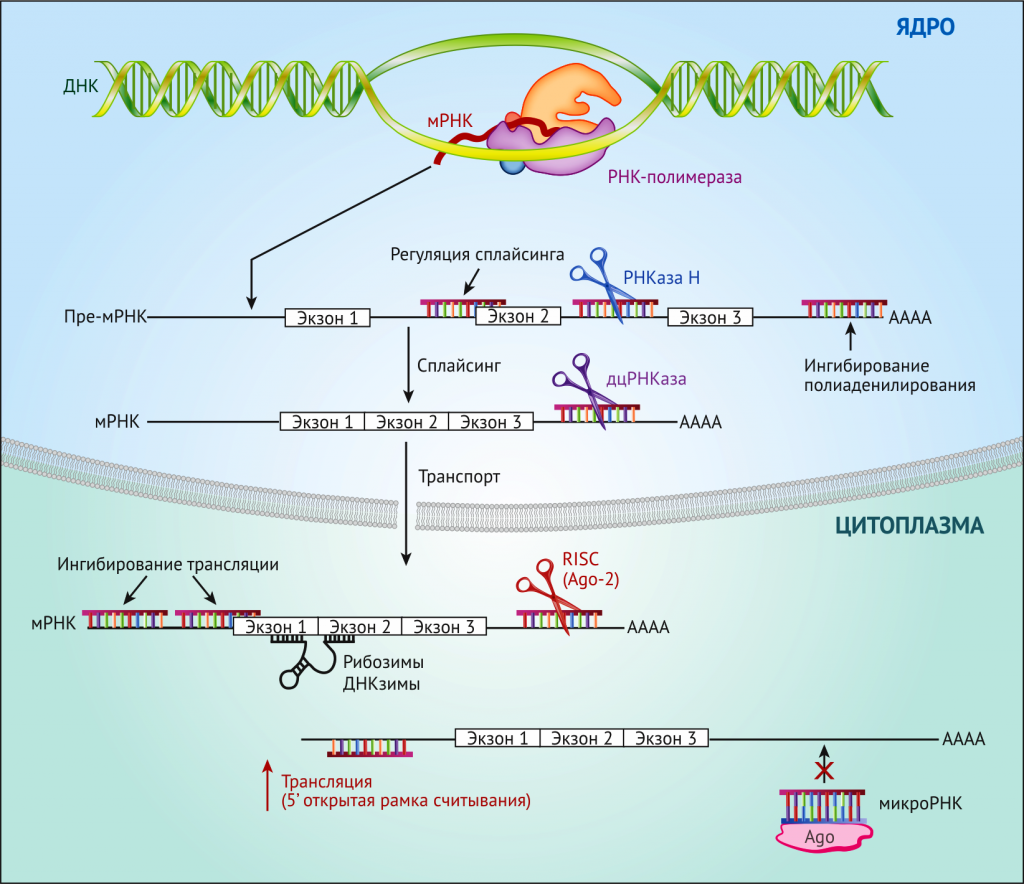
Сокращения: Ago-2 – Argonaute-2; дцРНКаза – нуклеаза двуцепочечных РНК; RISC – РНК-индуцированный комплекс сайленсинга; киРНК – короткие интерферирующие РНК.
Источник: Annual Reviews
Модификация цепи
Так как нуклеазы расщепляют фосфодиэфирную связь, очевидно, что первоочередной мишенью химической модификации олигонуклеотидов оказывается непосредственно их сахарофосфатный остов. Чаще всего для получения антисмысловых препаратов проводят фосфоротиоатную (PS) модификацию сахарофосфатного остова (Рис. 2), при которой один из атомов кислорода в фосфатной группе (не вовлечённый непосредственно в межнуклеотидную связь) заменяется на атом серы. PS-связь значительно повышает устойчивость к расщеплению нуклеазами [10], поэтому при системном введении PS-нуклеотиды обладают достаточной стабильностью в плазме, тканях и клетках, что позволяет им достигнуть РНК-мишеней. PS-олигодезоксинуклеотиды (ОДН), часто называемые «АСО первого поколения», способны стимулировать расщепление РНК-мишени РНКазой H, что является крайне важной составляющей механизма действия многих антисмысловых препаратов.
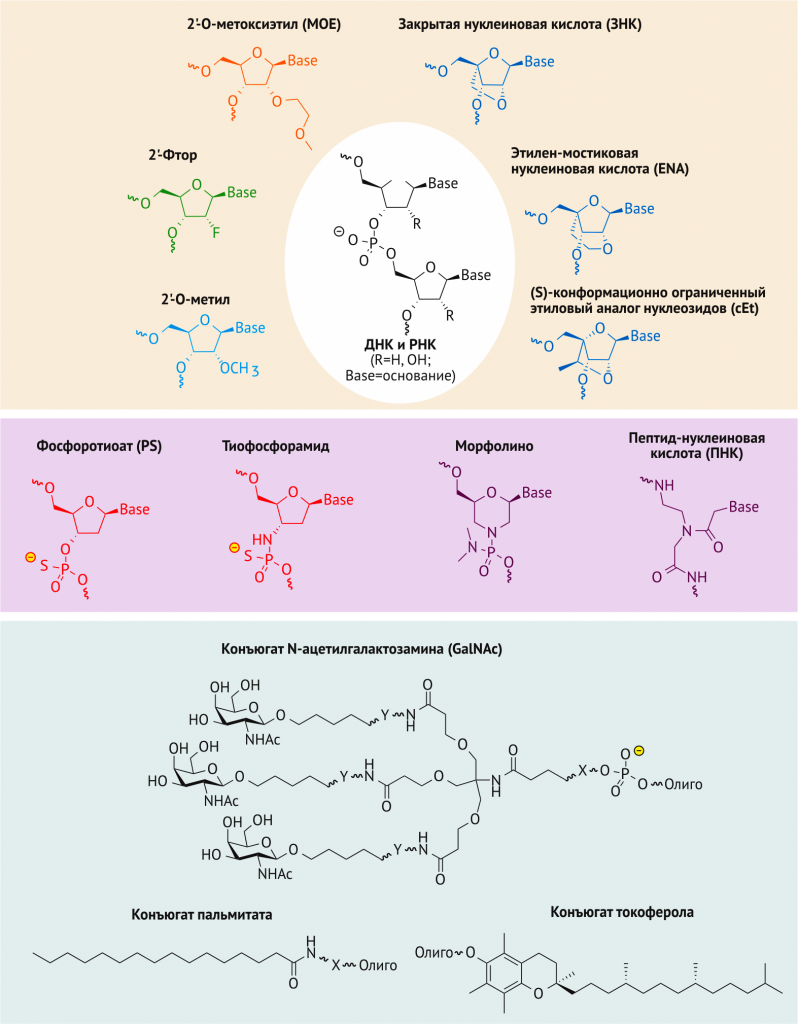
Другой пример ОДН с модифицированной цепью – это N3’→P5′ тиофосфорамидатные ОДН (Рисунок 2), у которых кислород в 3′-положении дезоксирибозы заменён на аминогруппу. У тиофосфорамидатов и фосфорамидатов проявляется высокая аффинность (сродство) к комплементарной РНК и высокая устойчивость к нуклеазам [11], однако в их действии не участвует РНКаза H.
Помимо модификаций фосфодиэфирной связи олигонуклеотидной цепи, разрабатываются вещества с заменой сахарофосфатного остова на изостер (прим. пер.: другую группу атомов, сохраняющую биологическую активность исходного соединения). Одна из таких замен привела к созданию фосфородиамидатных олигонуклеотидов с морфолиновой группой (Рис. 2). Благодаря фосфородиамидатным связям морфолиновые олигонуклеотиды биохимически нейтральны. Молекулы с подобными заменами по свойствам близки к ДНК и устойчивы к действию нуклеаз. В механизме их действия не участвует РНКаза H – он преимущественно заключается в остановке трансляции или других способах пространственной блокировки синтеза белков.
Модификация гетероциклов
Модификация гетероциклов (оснований) направлена преимущественно на повышение сродства и усиление связывания с комплементарными нуклеиновыми кислотами [12]. Замена водорода в положении C5 дезоксицитидина на метильную группу повышает температуру плавления дуплекса ДНК-РНК примерно на 0,5°C на одну замену (13) благодаря усилению стэкинга (прим. пер.: гидрофобное взаимодействие, обеспечивающее поддержание вторичной структуры двухцепочечной молекулы ДНК) в 5′-области основания. Такая модификация поддерживает механизм действия РНКазы H и применяется в некоторых антисмысловых препаратах для ослабления их иммуностимулирующего потенциала (14). Дальнейшее усиление стэкинга с дополнительными ароматическими или π-обогащёнными поверхностями путём замены водорода в положении C5 на пропинил-группу повысило стабильность дуплекса, однако увеличило его токсичность (15, 16).
Модификации сахаров
На данный момент, для улучшения терапевтических свойств олигонуклеотидов наиболее эффективны модификации остатков сахаров в 2′-положении. Олигонуклеотиды, содержащие сахар, модифицированный в 2′-положении, часто называют “АСО второго поколения”. Группировка таких сахаров в РНК-подобную структуру повышает их связывающую способность. К сожалению, практически все соединения с модификацией в 2′-положении значительно ослабляют или полностью подавляют способность РНКазы H расщеплять цепь РНК противоположного участка модификации. Подобное ограничение было минимизировано благодаря использованию химерной стратегии (гапмеров), отграничивающей 2′-модифицированными остатками центральный участок олигонуклеотида [17]. Также существуют ограничения в применении 2′-модифицированных нуклеозидов для получения дуплексов коротких интерферирующих РНК (киРНК), вовлечённых в механизм РНК-интерференции. Значительно больше возможностей открывается для использования данной модификации в олигонуклеотидных препаратах, которые не задействуют фермент-опосредованные механизмы терминации синтеза белка, например, нарушение сплайсинга мРНК.
Повышение сродства наблюдается и при энергетически обусловленной 2ˊ-модификации путём внедрения электронегативного заместителя в 2′-позицию. Так 2′-фтор-модификация (Рис. 2) повышает степень сродства (и температуру плавления на ∼2°C на одну замену относительно ДНК) с РНК-мишенью [13]. 2′-O-алкильные группы слабее повышают связывающую способность, чем 2′-фтор-нуклеозиды, однако обеспечивают значительную устойчивость к нуклеазам. В клинических испытаниях значительные успехи проявили АСО с гапмерной структурой, включающей 2′-O-метил-нуклеозиды [18], а также однородно модифицированные 2′-O-метил-нуклеотиды, модулирующие сплайсинг РНК [19]. Кроме того, многообещающим является применение 2′-O-метил-нуклеозидов (Рис.2) в олигонуклеотидах киРНК.
Минимальное количество 2′-O-метил-нуклеозидов в исследованиях механизма их действия in vivo оказалось достаточным для стабилизации киРНК [20, 21], при этом оно вызывало минимум побочных эффектов благодаря ограничению способности нуклеозидов выступать в роли агонистов микроРНК [22]. Комбинация 2′-O-метил- и 2′-фтор-модификаций позволяет полностью убрать структуру РНК из киРНК, что повышает стабильность дуплексов и их способность запускать РНК-интерферецию [23]. Сходные структуры киРНК с обширными 2′-фтор и 2′-O-метил-модификациями проходят клинические испытания [24].
На сегодняшний день среди 2′-модификаций наибольшую результативность показывает 2′-O-метоксиэтил (2′MOE; Рис. 2) модификация [3]. 2′MOE повышает температуру плавления нуклеиновой кислоты (2°C на одну замену) и значительно повышает устойчивость к нуклеазам [13]. Также такая замена уменьшает неспецифическое связывание с белками, что может снизить токсичность [25]. Кроме того, 2ˊMOE-олигонуклеотиды могут быть использованы для поддержания разнообразия антисмысловых механизмов [7, 26–30]. 2′MOE-модифицированные олигонуклеотиды являются наиболее эффективными (как in vitro, так и в клинических испытаниях) представителями АСО второго поколения, и многие из 2ˊMOE-модифицированных антисмысловых препаратов успешно применяются в клинике (Таблица 1).
Как и при попытках улучшения традиционных низкомолекулярных лекарств, успешное ограничение конформационной подвижности лигандов ведёт к значительному повышению связывающей способности. Сильнее всего связывающую способность олигонуклеотидов повышает такая модификация их остатков сахаров как бициклическая система, в которой 4′-углерод связывается с 2′-гидроксильной группой. Такая система получила название 2′,4′- мостиковой нуклеиновой кислоты (Obika с соавт., см. 31) или закрытой нуклеиновой кислоты (ЗНК) (Wengel, см. 32) (Рис. 2). ЗНК обладают значительными способностями к гибридизации и высокоустойчивы к действиям нуклеаз. Однородно модифицированные ЗНК-нуклеотиды не способствуют механизму действия РНКазы H [33], поэтому для его обеспечения предлагается стратегия одновременного применения гамперов и ЗНК-модифицированных нуклеотидов. Разрабатываются многочисленные структурные аналоги ЗНК [34], обладающие некоторыми улучшенными возможностями [35, 36]. Хотя ЗНК-содержащие гапмерные олигонуклеотиды обладают более широким спектром действия, чем 2′-модифицированные структуры, они проявляют большую токсичность [37, 38]. Попытки уменьшить токсичность этих веществ привели к синтезу и оценке in vivo нескольких аналогов ЗНК, в том числе нуклеотидов с заменой мостикового гетероатома [39], стереоизомеров [40], алкильной заменой [41] и заменой бицикличного кольца на более устойчивые гекситол-производные системы [42, 43]. Многообещающими препаратами являются модифицированные олигонуклеотиды с заменой на (S)-конформационно ограниченный этил (cEt) [44, 45], показавшие успешность в клинических испытаниях по нескольким показаниям. Подобные исследования указывают на перспективность этого класса молекул для повышения эффективности действия антисмысловых нуклеотидов в ближайшем будущем.
Стратегии конъюгации
Предполагается, что конъюгация олигонуклеотидов с лигандами, способными связываться с различными акцепторными сайтами поверхности клетки, изменяет фармакокинетические свойства олигонуклеотидов. Исследователи стремятся улучшить внедрение олигонуклеотидных препаратов в ткани и клетки, конъюгируя молекулы препаратов с различными лигандами. Наиболее изученным классом конъюгатов являются конъюгаты олигонуклеотидов с холестерином; они усиливают воздействие на печень, одновременно уменьшая влияние на почки [20, 46, 47]. Холестерол-конъюгированные олигонуклеотиды применяются для создания антисмысловых препаратов с различным механизмом действия, включающим действие РНКазы H, киРНК и антагонистов микроРНК. Другие липидные группы, например, жирные кислоты и токоферол, как и холестерин, обладают потенциальной способностью к перераспределению олигонуклеотидов в организме животных и усилению их воздействия на мишени, в частности, экспрессирующиеся в печени [46, 48–50].
Основным достижением таргетной доставки олигонуклеотидов в гепатоциты стало применение конъюгатов мультивалентного N-ацетилгалактозамина (GalNAc). Показано, что трёхвалентные конъюгаты GalNAc с киРНК [24] и одноцепочечные традиционные АСО [51] повышают активность и эффективность молекул-мишеней в печени животных. При дальнейших исследованиях препаратов в доклинических (на приматах) и клинических испытаниях было установлено, что GalNAc-конъюгированные киРНК [24], ингибиторы микроРНК и АСО, способствующие действию РНКазы H, способны ингибировать многие клинически важные гены-мишени. Показано, что оптимизированный GalNAc-конъюгированный АСО второго поколения 2′-MOE, нацеленный на мРНК аполипопротеина (a) в 30 раз более эффективен, чем немодифицированный олигонуклеотид той же последовательности [52]. Ожидается, что такое преимущество позволит повысить терапевтический индекс препарата, уменьшить его стоимость и обеспечить пациентам удобную схему лечения, например, исключив необходимость применения препаратов для печени на протяжении месяца и более. Пока не установлено, окажется ли конъюгат-опосредованная доставка олигонуклеотидов к другим тканям настолько же эффективной, как и доставка к печени, однако её возможность остаётся интересной и перспективной областью изучения конъюгированных олигонуклеотидов в будущем.
ФАРМАКОКИНЕТИКА ОЛИГОНУКЛЕОТИДОВ
Фармакокинетические свойства олигонуклеотидов обусловлены преимущественно химическими свойствами их цепи и, таким образом, практически не различаются для различных последовательностей в пределах одного химического класса веществ [53, 54]. Биодоступность препарата в тканях обеспечивается его связыванием с белками плазмы, ограничивающим клубочковую фильтрацию и, в конечном счете, выведением олигонуклеотидов с мочой. Как обсуждалось выше, по сравнению с немодифицированными АСО, у PS-модифицированных олигонуклеотидов наблюдается повышенная стабильность в плазме, более прочная связь с белками и, как следствие, лучшая биодоступность в тканях. PS-модифицированные олигонуклеотиды обладают широким системным биораспределением и наибольшие их концентрации наблюдаются в печени и почках, костном мозге, адипоцитах и лимфоузлах (Рисунок 3). Такие АСО поступают в клетки преимущественно путём эндоцитоза [53, 55]. Как размер, так и заряд молекулы АСО препятствует их прохождению через гематоэнцефалический барьер, однако при интратекальном введении в спинномозговую жидкость (СМЖ) модифицированные одноцепочечные олигонуклеотиды широко распределяются по тканям центральной нервной системы (ЦНС) [28, 56]. При системном или местном введении олигонуклеотидов большинство из них поступает в клетки в течение нескольких часов, чему способствует быстрый эндоцитоз.
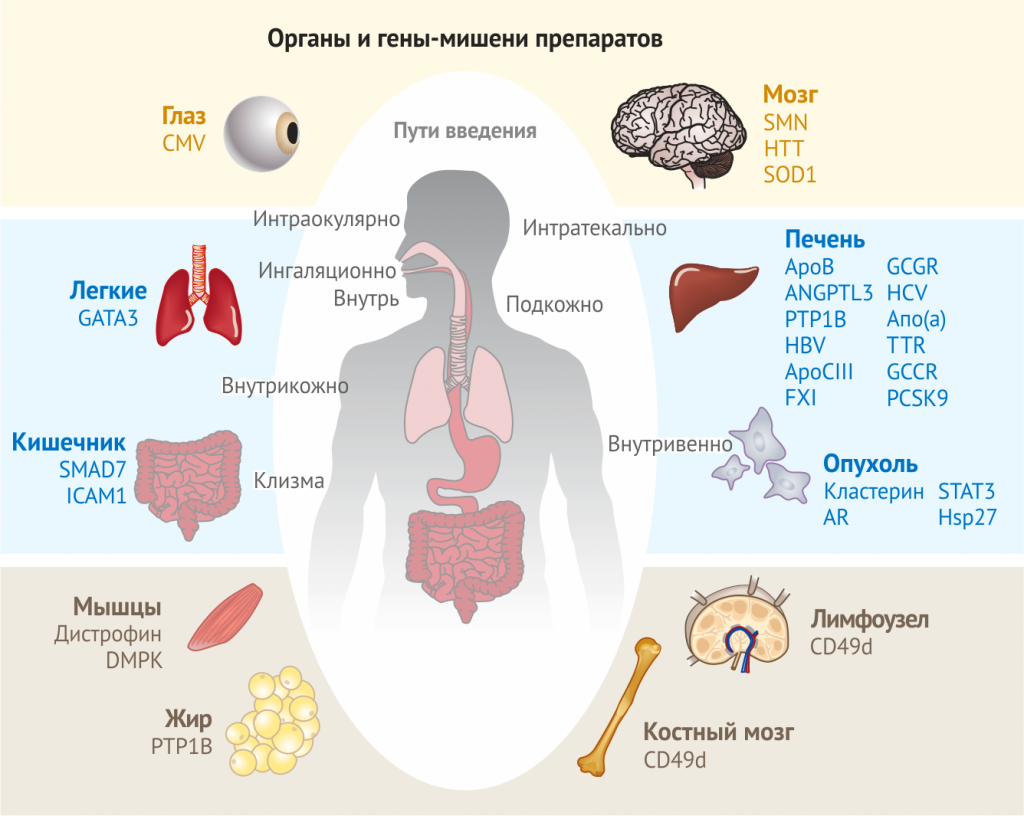
Источник: Annual Reviews
При подкожном введении (пк), АСО быстро поступают от места инъекции в кровоток, а пиковая концентрация в плазме для АСО второго поколения достигается через 3-4 часа [26, 54]. При внутривенном (в/в) или пк введении после достижения пиковой концентрации в плазме концентрация препарата быстро снижается по мультиэкспоненте, т.е. первоначальная фаза быстрого распределения препарата в тканях, занимающая от нескольких минут до часов, сменяется более медленной фазой окончательного выведения препарата из тканей (период полувыведения до нескольких недель). При системном распределении препараты преимущественно поступают в ткани печени, почек, костного мозга, адипоциты (за исключением липидных капель) и лимфатические узлы [54, 57, 58]. При пероральном, интравитреальном и ингаляционном введении, системная абсорбция АСО крайне низка и составляет менее 1% введённой дозы [59–61]. Увеличение системной абсорбции при пероральном введении препарата было достигнуто путём употребления АСО совместно с усилителями проницаемости, которые обратимо изменяют парацеллюлярный транспорт в тонком кишечнике [62].
Окончательному клиренсу и выведению PS-модифицированных ОДН первого поколения способствует их расщепление эндо- и экзонуклеазами на низкомолекулярные фрагменты, которые теряют способность связывать белки плазмы, а потому фильтруются и окончательно выводятся с мочой [53, 54]. АСО второго поколения с различными модификациями сахаров устойчивы к действию нуклеаз и, таким образом, метаболизируются медленно, с периодами полувыведения порядка около 2-4 недель, что позволяет применять их один раз в неделю или ещё реже.
Олигонуклеотиды, не имеющие заряда или слабее связанные с белками плазмы, такие как пептид-нуклеиновые кислоты, морфолино и немодифицированные киРНК в свободной форме, обладают большей величиной клиренса и быстрее выводятся из крови [63-65]. Эти соединения и их метаболиты легко фильтруются и выводятся из организма, что отражается в низком или практически отсутствующем поглощении их тканями. Таким образом, для повсеместной и успешной системной доставки препарата в ткани и клетки требуется обеспечить его оптимальное и сбалансированное связывание с белками плазмы.
ТОКСИКОЛОГИЯ АНТИСМЫСЛОВЫХ ОЛИГОНУКЛЕОТИДОВ
Как любые препараты, АСО имеют дозозависимую токсичность. Лучше всего охарактеризованы такие классы антисмысловых препаратов как PS-модифицированные ОДН первого поколения и 2′-MOE-модифицированные АСО [66, 67], так как многие препараты этих групп прошли клинические испытания (Таблица 1). Исследователи лишь начинают изучать токсикологические свойства других типов АСО [38, 63, 68-70].
Потенциальную токсичность АСО можно разделить на гибридизационно-зависимую и гибридизационно-независимую. Гибридизационно-зависимая токсичность объясняется усиленным фармакологическим эффектом и гибридизацией с РНК, не являющимися мишенями АСО. Токсичность такого типа аналогична наблюдаемой у других препаратов и её можно избежать или свести к минимуму путём надлежащего выбора РНК-мишени и тщательного изучения фармакологических и токсикологических свойств антисмысловых ингибиторов на этапе доклинических моделей. Гибридизационно-зависимую токсичность, связанную с воздействием на постороннюю мишень, можно уменьшить, применив тщательный биоинформационный анализ для выявления мишени с идеальным структурным соответствием или малым числом несовпадающих оснований. Для более коротких олигонуклеотидов с высокоаффинными модификациями более высока вероятность взаимодействия с посторонними мишенями и расщепления их, в случае активации РНКазы Н [69]. Олигонуклеотиды, действующие путём РНК-интерференции, могут выступать в роли микроРНК, которым для распознавания мишени достаточно совпадения 6-8 нуклеотидов (в т.н. «seed-регионе»), что может приводить к сотням или даже тысячам возможных побочных взаимодействий [71-73]. Возможные эффекты недостаточного распознавания в seed-регионе можно ослабить путём химических модификаций [22]. Если учесть все меры предосторожности, вероятность обнаружения селективного антисмыслового препарата значительно повышается.
Вторым источником потенциальной токсичности может выступать взаимодействие олигонуклеотидов с белками. Эти эффекты могут как зависеть от последовательности олигонуклеотида (например, взаимодействие с Toll-like рецепторами, см. 14), так и не показывать никакой взаимосвязи с последовательностью. В последнем случае токсичность, как правило, зависит от химических свойств олигонуклеотидов и белков, с которыми взаимодействует этот химический класс веществ.
Примеры побочных эффектов, которые в значительной степени независимы от последовательности, включают воздействие на свёртывание крови [74] и активацию комплемента [70, 75], в то время как активация иммунных клеток может оказаться как зависимой, так и независимой от последовательности [76, 77]. Понимание механизмов токсичности дает возможность проводить скрининг антисмысловых препаратов для выявления тех, которые обладают наилучшей переносимостью. Показано, что 2′-MOE-модифицированные антисмысловые препараты в целом имеют хорошую переносимость и переносятся лучше, чем PS-модифицированные ОДН [25, 66, 78, 79]. В модели на грызунах олигонуклеотиды, содержащие бициклические модификации сахаров, такие как ЗНК, могут проявлять гепатотоксичность, частично обусловленную повышенной склонностью к гибридизации с посторонними мишенями [38, 69]. Считается, что АСО с некоторыми специфическими бициклическими модификациями сахаров, такими как cEt, переносятся лучше, чем ЗНК [43]. Для других химических классов олигонуклеотидов профиль безопасности в литературе охарактеризован слабо, поскольку эти препараты находятся на ранних этапах клинических испытаний.
ФАРМАКОЛОГИЯ АНТИСМЫСЛОВЫХ ОЛИГОНУКЛЕОТИДОВ
За последние 25 лет множество антисмысловых олигонуклеотидов прошло клинические испытания как препараты терапии широкого спектра заболеваний [2, 80–82]. Для лечения цитомегаловирусного ретинита, который, помимо прочего, является распространённой оппортунистической инфекцией у больных ВИЧ-инфицированных пациентов, одобрен фомивирсен (fomivirsen) – антисмысловой препарат первого поколения, мишенью которого является цитомегаловирус [83]. Как было сказано выше, 2′-MOE-модифицированные антисмысловые препараты второго поколения проявляют более высокую эффективность, лучшую переносимость и большую продолжительность действия по сравнению с PS-модифицированными ОДН первого поколения. Многие препараты второго поколения в настоящее время находятся на стадии разработки (Таблица 1) и, как некоторые разрабатываемые препараты на основе киРНК, демонстрируют обнадёживающую эффективность в клинических испытаниях (Рис. 3). Всестороннее рассмотрение разрабатываемых антисмысловых препаратов выходит за пределы данного обзора. Здесь рассматриваются некоторые примеры использования антисмысловых препаратов в различных терапевтических областях.
Сердечно-сосудистые заболевания
Мипомерсен (mipomersen) – первый препарат на основе АСО второго поколения, одобренный Управлением по контролю за продуктами и лекарствами США (FDA) в качестве вспомогательной терапии при гомозиготной семейной гиперхолестеринемии (гоСГ). Он уменьшает содержание мРНК аполипопротеина В (apoB), тем самым снижая в плазме уровень apoB-содержащих частиц (например, холестерина липопротеинов низкой плотности (ХС-ЛПНП)]. Фармакологические свойства мипомерсена, установленные в доклинических и клинических испытаниях, были рассмотрены ранее [26, 84]. Недавний ретроспективный анализ рандомизированного контролируемого исследования III фазы показал, что мипомерсен эффективно снижает уровни apoB и ХС-ЛПНП у подростков (от 12 до 18 лет) больных гоСГ при максимально допустимой дозе статинов [85]. Аналогичное уменьшение уровня измеренных атерогенных липопротеинов наблюдалось для когорты пациентов-подростков по сравнению со взрослыми пациентами. Также было доказано, что мипомерсен снижает уровень всех apoB-содержащих атерогенных липопротеинов, включая липопротеин (а) [ЛП(a)], независимый генетический фактор риска сердечно-сосудистых заболеваний. При анализе объединенных данных из четырех исследований III фазы [86] было обнаружено, что мипомерсен значительно снижает уровень ЛП(a) у пациентов с широким спектром липидных нарушений. Наконец, терапия мипомерсеном в дозе до 400 мг в течение 4 недель абсолютно не влияла на реполяризацию в проводящей системе сердца [87]. Эти результаты позволяют утверждать, что мипомерсен, и, возможно, другие 2′-MOE-модифицированные АСО (благодаря сходным физико-химических свойствам и фармакокинетике) не влияют на интервал QT.
Аполипопротеин C III (apoCIII) играет важнейшую роль в метаболизме богатых триглицеридом липопротеинов, и снижение его экспрессии связано с более низким риском развития сердечно-сосудистых заболеваний [88, 89]. Фаза I рандомизированного двойного слепого плацебо-контролируемого клинического испытания воланесорсена (volanesorsen), антисмыслового препарата второго поколения, разработанного для снижения уровня мРНК apoCIII, продемонстрировала устойчивое дозозависимое и длительное снижение уровня apoCIII и триглицеридов в плазме здоровых добровольцев [88]. В фазе II последующего исследования, проведённого с участием трёх пациентов с синдромом семейной хиломикронемии (ССХ) и без плацебо-контроля [90], было выявлено резкое снижение содержания белка apoCIII (с 71% до 90%) и триглицеридов в плазме крови (с 56% до 86%).
Кроме того, в фазе II рандомизированного плацебо-контролируемого исследования с участием больных гипертриглицеридемией была подтверждена дозозависимость эффекта воланесорсена как при монотерапии, так и в качестве дополнительного препарата [91]. Уровень ХС-ЛПВП плазмы повышался, а уровень ХС-ЛПОНП дозозависимо снижался. Воланесорсен в настоящее время изучается в III фазе плацебо-контролируемых клинических испытаний лечения ССХ и семейной парциальной липодистрофии.
Имеющиеся данные свидетельствуют о том, что тяжёлая недостаточность фактора XI обеспечивает защиту от тромбоза глубоких вен и, следовательно, от поражений сердечно-сосудистой системы и сопутствующей смертности. Было показано, что у пациентов, перенесших полную артропластику коленного сустава, снижение уровня фактора XI с помощью IONIS-FXIRx является эффективным методом профилактики венозной тромбоэмболии (ВТЭ) и, по-видимому, безопасно в отношении риска кровотечений. В исследовании без плацебо-контроля с параллельными группами было показано, что пациенты, принимающие препарат, имеют более низкий риск ВТЭ и клинически значимого кровотечения по сравнению с пациентами, принимающими эноксапарин [92]. IONIS-FXIRx дозозависимо снижает уровень фактора XI без снижения уровня других компонентов внутреннего пути, что подчеркивает специфичность препарата и его значительную перспективность по сравнению с обычными антитромботическими средствами. В настоящее время продолжается фаза II исследования IONIS-FXIRx / BAY 2306001 с целью изучения влияния препарата на пациентов с терминальной стадией почечной недостаточности, находящихся на гемодиализе.
Воспаление и аутоиммунные заболевания
В настоящее время продолжается оценка эффективности АСО как препаратов для терапии нескольких воспалительных заболеваний, при этом наибольшую успешность продемонстрировали препараты, предлагаемые для лечения воспалительных заболеваний кишечника. SMAD7 представляет собой внутриклеточный ингибитор, препятствующий рецептор-зависимому фосфорилированию других белков SMAD, являющихся положительными эффекторами передачи сигнала трансформирующего фактора роста β1. Нацеленный на мРНК SMAD7, PS-модифицированный ОДН первого поколения монгерсен (mongersen), принимается перорально в форме таблеток, покрытых рН-чувствительной оболочкой [93]. В первом клиническом испытании монгерсена приняли участие 15 пациентов с активной стероид-резистентной и / или стероид-зависимой болезнью Крона [93], после чего проводилось рандомизированное плацебо-контролируемое исследование II фазы с подбором оптимальной дозировки для пациентов с активной формой болезни средней и тяжёлой степени [94]. Изучался эффект препарата в той же суточной дозе, но в более широком диапазоне доз и при более длительном 14-дневном курсе лечения. Препарат показал хорошую переносимость, причем 119 из 124 (96%) пациентов, получавших монгерсен перорально, успешно завершили 2-недельный период лечения. В частности, значительная доля пациентов из двух групп с повышенной дозировкой препарата (40 и 160 мг монгерсена в сутки) достигла клинической ремиссии. Благодаря этим обнадеживающим результатам II фазы, моргенсен перешёл в более долгосрочную фазу III исследования. Также этот препарат изучается в фазе III плацебо-контролируемого исследования с участием больных умеренным и тяжёлым язвенным колитом.
Исследование эффектов аликафорсена (alicaforsen), PS-модифицированного АСО первого поколения, действующего на молекулу межклеточной адгезии 1 (CD54), проводилось при его системном введении пациентам с болезнью Крона [95] и при введении с помощью клизмы больным легким и умеренным левосторонним язвенным колитом в активной форме (или активным резервуарным илеитом) [96-98]. На основании обнадеживающих результатов контролируемых исследований и исследований без плацебо-контроля в настоящее время разрабатывается препарат для лечения упорного хронического резервуарного илеита [96, 99].
Онкология
Поскольку рак остаётся одной из главных проблем современной медицины, основным направлением технологии антисмысловых препаратов становится разработка противоопухолевых средств. В некоторых ранних исследованиях антисмысловых препаратов изучалось их возможное применение в качестве терапии при различных типах рака [100]. Несмотря на довольно длительное применение этих препаратов в клинике, определение их противоопухолевого эффекта в клинических исследованиях остаётся затруднительным. Усовершенствование антисмысловых препаратов улучшило их эффективность и переносимость, что, следует надеяться, повысит успешность клинического лечения. В настоящее время один антисмысловой препарат против различных злокачественных образований находится в III фазе клинических исследований, а ещё несколько – на более ранних стадиях разработки (Таблица 1). Кастирсен (custirsen), химерный 2′-MOE-модифицированный антисмысловой препарат, показал многообещающие результаты в нескольких исследованиях фазы II, и в настоящее время изучается в фазе III клинического испытания при раке предстательной железы и раке лёгкого [101].
В настоящее время также изучаются два препарата с cEt-модификациями сахаров, показавшие значительную эффективность в клинических испытаниях. AZD9150 — это АСО, мишенью которого является преобразователь сигналов и активатор транскрипции 3 (signal transducer and activator of transcription 3, STAT3), который активируется при различных типах рака [102]. В фазе I исследования без плацебо-контроля препарат проявил обнадёживающую активность при монотерапии при нескольких типах рака, при этом наибольшая эффективность была отмечена при диффузной крупноклеточной В-клеточной лимфоме [102]. Второй cEt-модифицированный олигонуклеотид, мишенью которого является рецептор андрогенов, проходит клиническое исследование без плацебо-контроля как препарат для терапии рака предстательной железы (103). Клинические исследования некоторых других антисмысловых препаратов, в том числе аналогов микроРНК и киРНК, находятся на ранних стадиях (Таблица 1).
Неврология
Антисмысловые препараты рассматриваются как лекарства против многих неврологических заболеваний, а их поступление возможно обеспечить как системно, так и в СМЖ, окружающую ткани мозга (Таблица 1). Сквозь неповрежденный гематоэнцефалический барьер АСО в достаточном количестве не проходят, поэтому для терапии заболеваний головного или спинного мозга препараты требуется вводить непосредственно в СМЖ или паренхиму. После инъекции непосредственно в СМЖ, PS-модифицированные АСО второго поколения распространяются по всем тканям спинного и головного мозга [28, 56]. В отличие от одноцепочечных олигонуклеотидов, у двуцепочечных киРНК наблюдается более ограниченное распределение и сниженная активность в ЦНС. Большинство препаратов киРНК вводят непосредственно в паренхиму головного мозга, где они осуществляют локальное подавление гена-мишени [104, 105]. Таким образом, для терапии неврологических заболеваний разрабатываются антисмысловые препараты с различным механизмом действия и структурой олигонуклеотидов, при этом одноцепочечная структура АСО способствует их поступлению практически во все структуры ЦНС, а киРНК применяются для местной терапии.
Мышечная дистрофия Дюшенна (МДД) представляет собой прогрессирующее нервно-мышечное заболевание, приводящее к глубокой инвалидности и, в конечном счете, летальному исходу. МДД возникает в результате повреждения гена дистрофина точечными мутациями, инсерциями или хромосомными перестройками, что приводит к продукции укороченного малофункционального белка или отсутствию транскрипта в случае нонсенс-мутации [106]. В нескольких лабораториях применялись АСО, способствующие пропуску специфических экзонов дистрофина, и, как следствие, альтернативному сплайсингу и наработке продукта дистрофина с расширенной открытой рамкой считывания, результатом чего стало частичное восстановление функции белка [107, 108]. Поскольку в основе МДД могут лежать несколько геномных нарушений, для лечения всех форм заболевания невозможно применять какой-либо один олигонуклеотид. Наилучшие результаты в клинических испытаниях показали АСО, предназначенные для стимуляции пропуска экзона 51. Для двух таких препаратов рассматривается вопрос выпуска в обращение (Таблица 1).
Дрисаперсен (drisapersen) представляет собой однородный 2′-O-метил-PS-модифицированный олигонуклеотид, разработанный для связывания с последовательностью в пределах экзона 51 и способствующий пропуску экзона при трансляции [108], тогда как этеплирсен (eteplirsen) является однородно модифицированным морфолиновым препаратом, созданным для связывания с участком в экзоне 51 пре-мРНК дистрофина, аналогичным сайту связывания дрисаперсена [109]. Дрисаперсен вводят в виде инъекции подкожно, а этеплирсен – внутривенно в виде инфузии [19, 110, 111]. Несмотря на обнадеживающие клинические эффекты в ранних плацебо-контролируемых исследованиях фазы II [19, 110], дрисаперсен не превзошёл плацебо в более крупных плацебо-контролируемых исследованиях III фазы в отношении главного ожидаемого результата — возможности осуществления пациентом шести минут ходьбы. Первоначальная оценка этеплирсена проводилась в исследовании без плацебо-контроля, в котором препарат вводился пациентам внутривенно в течение недели в шести различных дозах. В целом, препарат переносился хорошо, а биопсия мышц показала, что введение наибольших доз приводило к вариабельному усилению экспрессии дистрофина [112]. Было проведено небольшое контролируемое исследование, в котором пациенты рандомно разделялись на группы, получавшие две дозы препарата либо плацебо в неделю в течение 24 недель (n=4 в группе), а на 25-й неделе, пациенты, принимавшие плацебо, были переведены на приём либо 30 мг/кг (n=2), либо 50 мг/кг (n=2) этеплирсена [111]. На 24-й неделе не наблюдалось существенных различий в дистанции, пройденной за шесть минут, между группами, принимавшими плацебо и препарат. На 48-й неделе пациенты, получавшие 50 мг/кг этеплирсена, были способны пройти за шесть минут такую же или большую дистанцию по сравнению с пациентами, получавшими плацебо и переведёнными на активный приём препарата [111]. Длительное наблюдение за пациентами (36 месяцев), участвовавшими в исследовании, показало, что большинство пациентов поддерживали способность передвигаться [113]. Результаты иммуногистохимического анализа экспрессии дистрофина в мышечной ткани варьировали и показали умеренное усиление окрашивания дистрофина для дрисаперсена и этеплирсена. Оба препарата были направлены в FDA для разрешения выпуска в обращение; однако на момент написания этой статьи дрисаперсен не был допущен к регистрации, а этеплирсен все еще находится на рассмотрении.
В настоящее время разрабатываются дополнительные антисмысловые препараты, нацеленные на другие экзоны, что позволит увеличить число пациентов, прошедших терапию антисмысловыми препаратами (Таблица 1). Подобные исследования ещё продолжаются и их результаты пока не опубликованы.
Миотоническая дистрофия типа 1 (МД1) представляет собой полиорганное заболевание, причиной которого является экспансия тринуклеотидного повтора (CTG) в 3′-нетранслируемой области гена миотонин-протеинкиназы (DMPK) [114]. Образующийся транскрипт, который содержит от сотен до тысяч CUG-повторов, связывается с факторами сплайсинга РНК, например, белками семейства Muscleblind, и изолирует их в отдельных участках ядра, что приводит к потере активности этих белков [115]. В качестве потенциальных методов лечения МД1 исследователи рассматривают два подхода, различных по механизму антисмыслового действия: применение недеградирующих АСО для вытеснения белков семейства Muscleblind из транскрипта [116, 117] или же, в качестве альтернативы, применение АСО, способствующих активности РНКазы Н и способствующих деградации токсичных РНК-транскриптов с попутным высвобождением белков семейства Muscleblind [118, 119]. В данный момент рандомизированное контролируемое исследование с участием больных МД1 проходит IONIS-DMPK-2.5Rx – химерный АСО, имеющий по центру разрыв в ДНК для поддержки механизма действия РНКазы H, а по краям несущий как 2′-MOE- модификации, так и cEt-модификацию (Таблица 1).
Транстиретиновый амилоидоз (семейная амилоидная полинейропатия, TTR-амилоидоз) является формой системного амилоидоза, вызываемой неправильным фолдингом белка транстиретина (TTR), который в виде токсичных амилоидных фибрилл скапливается в различных тканях, в том числе в периферических нервах, желудочно-кишечном тракте и сердце [120]. Терапевтическая стратегия заключается в применении АСО для уменьшения содержания субстрата TTR, что снижает скорость образования фибрилл. Основным источником циркулирующего TTR являются ткани печени, в которую легко можно доставить антисмысловые препараты. В настоящее время для лечения TTR-амилоидоза разрабатываются три разных антисмысловых препарата, два из которых проходят плацебо-контролируемые клинические испытания III фазы (Таблица 1). Для семейной амилоидной полинейропатии (САП), а также амилоидной кардиомиопатии разработан IONIS-TTRRx – антисмысловой препарат второго поколения, зависящий от РНКазы H [29]. В исследовании фазы I с участием здоровых добровольцев этот препарат показал дозозависимое снижение уровня TTR в плазме крови [29]. В настоящее время IONIS-TTRRx находится в фазе III клинических испытаний. Патисиран представляет собой киРНК, заключенные в липидные наночастицы, и в настоящее время проходит клинические испытания фазы III для лечения САП. В исследовании с участием здоровых добровольцев [121] было показано дозозависимое снижение TTR плазмы при внутривенном введении патисирана. У пациентов наблюдалась лёгкая или умеренная реакция на инфузию, которая исчезала спонтанно (лёгкая) или при временном прерывании инфузии с одновременным введением глюкокортикоидов или без него (умеренная реакция). В исследованиях II фазы у пациентов с полинейропатией было подтверждено дозозависимое снижение TTR плазмы с аналогичным профилем безопасности [122]. Также в настоящее время для лечения кардиомиопатии разрабатываются GalNAc-сопряженные киРНК и IONIS-TTRRx (Таблица 1) [123].
Спинальная мышечная атрофия (СМА) является тяжёлым прогрессирующим поражением моторных нейронов и обычно возникает в младенчестве или детском возрасте. Причина заболевания кроется в делециях или мутациях гена, кодирующего белок выживания моторных нейронов 1 (SMN1) [124]. У человека имеется паралогичная копия гена SMN1 – SMN2; этот ген отличается от SMN1 на несколько нуклеотидов, один из которых ослабляет сайт сплайсинга для экзона 7, что приводит к делеции экзона 7 и синтезу укороченного, быстро деградирующего белка. Для связывания с определенной последовательностью в интроне 7 гена SMN1 и двух пре-мРНК, включения экзона 7 в транскрипт и усиления продукции белка SMN был разработан препарат нусинерсен (nusinersen), полностью 2′-MOE-модифицированный олигонуклеотид [125, 126]. Недавно было завершено исследование I фазы без плацебо-контроля с участием детей, больных СМА типа 2 и типа 3. Было установлено, что нусинерсен хорошо переносится, а для детей подходит интратекальное болюсное введение препарата [27, 127]. Уже после однократной дозы, введённой интратекально, наблюдалось дозозависимое улучшение моторных функций [27]. За данным экспериментом последовали два исследования фазы Ib/IIa с несколькими вариантами дозировки — в первом из них выборка была сходна с принимавшей участие в исследовании однократного приёма препарата, в то время как второе исследование велось с участием больных, страдающих более тяжёлой СМА типа 1 [128]. На основании этих обнадеживающих результатов исследования однократного приёма препарата и исследований с несколькими вариантами дозировки без плацебо-контроля в настоящее время проводятся два плацебо-контролируемых исследования – с участием больных СМА с началом в детском и младенческом возрасте соответственно.
Хорея Гентингтона (ХГ) представляет собой аутосомно-доминантное нейродегенеративное заболевание, возникающее в результате экспансии CAG-повтора в гене гентингтина (HTT), что вызывает токсическое усиление функции белка из-за избыточной длины полиглутаминового тракта в синтезируемом белке. В моделях ХГ на животных было показано, что АСО, разработанные для снижения общего HTT, обеспечивают длительное улучшение состояния больных мышей и, что важно, уменьшают уровень HTT у приматов после интратекального введения [56]. Аналогичные АСО изучаются в плацебо-контролируемых клинических испытаниях с участием больных ХГ (Таблица 1).
Инфекционные заболевания
Для ингибирования репликации вируса можно использовать различные антисмысловые механизмы, например, связывание с вирусной мРНК для стерической блокировки трансляции белка или для деградации вирусной РНК посредством РНКазы; также возможна блокировка микроРНК хозяина, поддерживающих репликацию вируса. В настоящее время клинические испытания проходят несколько антисмысловых препаратов для терапии различных инфекционных заболеваний (Таблица 1).
Важное значение для стабильности и распространения вируса гепатита С (HCV) имеет микроРНК-122 (miR-122), в изобилии присутствующая в печени [129]. Она связывается с высококонсервативной 5′-нетранслируемой областью генома HCV, защищая его от деградации и врождённого иммунитета хозяина [129]. Кроме того, считается, что miR-122 играет роль в развитии воспаления печени [130]. У шимпанзе, инфицированных вирусом гепатита С, ингибирование активности miR-122 LNA-модифицированным АСО миравирсеном (miravirsen) приводило к подавлению репликации HCV [131]. В плацебо-контролируемом исследовании фазы IIa с участием 36 больных хроническим HCV 5 еженедельных доз миравирсена уменьшили уровень РНК HCV, при этом эффект сохранялся и спустя некоторое время после периода введения препарата [132]. У некоторых пациентов РНК HCV не определялась и к концу исследования либо оставалась необнаружимой, либо значительно возрастала. Долгосрочный ретроспективный анализ клинических испытаний не выявил проблем с безопасностью длительного приема миравирсена у пациентов с HCV, получавших препарат в пределах 35 месяцев [133]. В настоящее время продолжается исследование II фазы, изучающее эффект миравирсена в сочетании с телапревиром (telaprevir) и рибавирином у HCV-инфицированных пациентов, не отвечающих на терапию пегилированным интерфероном альфа и рибавирином.
RG-101 является aGalNAc-конъюгированным олигонуклеотидом, разработанным для ингибирования miR-122 и репликации HCV путём механизма, аналогичного стерическому блокирующему действию миравирсена. RG-101 использует cEt- и 2′-MOE-модифицированные нуклеотиды. Дизайн I фазы клинических испытаний RG-101 был разработан как для здоровых добровольцев, так и для пациентов, инфицированных HCV [134].
У здоровых добровольцев разовая доза RG-101 повышала содержание щелочной фосфатазы (прямой мишени miR-122) и снижала уровень холестерина (непрямой мишени miR-122) в сыворотке крови, что согласуется с предполагаемой фармакологией препарата. У пациентов с HCV, получивших разовую дозу 2 или 4 мг/кг RG-101, наблюдалось значительное уменьшение РНК HCV по сравнению с получавшими плацебо. Большинство пациентов, получивших RG-101, на 57-й день исследования имели уровень РНК HCV ниже определяемого количественным анализом, при этом у большинства из них этот эффект сохранялся и к 85-му дню исследования. RG-101 показал безопасность и хорошую переносимость как у здоровых добровольцев, так и у пациентов с HCV. Результаты этого клинического исследования оказались весьма обнадеживающими и способствовали дальнейшему исследованию препарата.
ЗАКЛЮЧЕНИЕ
Терапевтические методы на основе антисмысловых препаратов продолжают развиваться, при этом два препарата уже разрешены к применению, а многие другие находятся на поздних этапах клинических испытаний. Кроме того, разрабатывается более 30 препаратов для лечения широкого спектра заболеваний, и многие из них показывают многообещающие результаты и возможность применения во многих областях терапии. Несмотря на то, что за последние 25 лет технология антисмысловых препаратов добилась определенных успехов, остаётся возможность для её дальнейшего усовершенствования. Модификации олигонуклеотидов улучшают эффективность и переносимость антисмысловых препаратов, а также улучшают распределение препарата в тканях и, в конечном итоге, способствуют его поступлению к РНК-мишени внутри клетки. Дальнейшее усовершенствование антисмысловых препаратов можно обеспечить путём улучшения структуры АСО, более полного скрининга и поиска новых химических модификаций и, возможно, лекарственной формы. Более глубокое понимание молекулярных механизмов, благодаря которым олигонуклеотиды распределяются в организме и в клетках, и, в конечном итоге, связываются с РНК-мишенью, обеспечит рациональную основу для дальнейшего усовершенствования антисмысловых препаратов. Хотя исследователи достаточно осведомлены о механизмах возникновения побочных эффектов олигонуклеотидов, для дальнейшего улучшения безопасности и переносимости препаратов (особенно АСО с новыми химическими модификациями и структурой) необходимы дополнительные исследования Наконец, выявление удобных методов контроля за действием антисмысловых препаратов имеет большое значение для повышения коммерческой рентабельности технологии. Хотя в технологии антисмысловых препаратов достигнут значительный успех, ещё многое предстоит осуществить для полного раскрытия их потенциала.
