Клеточные технологии в иммунотерапии: алгоритм создания CD8+-лимфоцитов с химерными антигенными рецепторами для лечения злокачественных опухолей
В прошлой статье пристальное внимание было уделено строению и функционированию химерного антигенного рецептора (chimeric antigen receptor, CAR), пришло время коснуться клинических аспектов этого вида иммунотерапии.
Как только была показана принципиальная возможность создания CAR-CD8+-лимфоцитов, встал вопрос выбора антигенной мишени. Антигены, экспрессируемые опухолью, можно разделить на опухоль-специфичные и опухоль-ассоциированные. К первой группе относятся антигены, являющиеся продуктом специфичной мутации, такие антигены есть только в опухоли и не встречаются в нормальных тканях. Примером могут служить мутировавшие рецепторы эпидермального фактора роста (EGFvII). Эта группа также носит название «неоантигены». Вторая группа включает антигены, которые в норме экспрессируются в процессе онтогенеза в тех или иных тканях, к примеру, раково-эмбриональный антиген, а также гиперэкспрессию антигенов, характерных для той или иной ткани, например, семейство белков MAGE и HER2 (рис. 1) [1, 2].
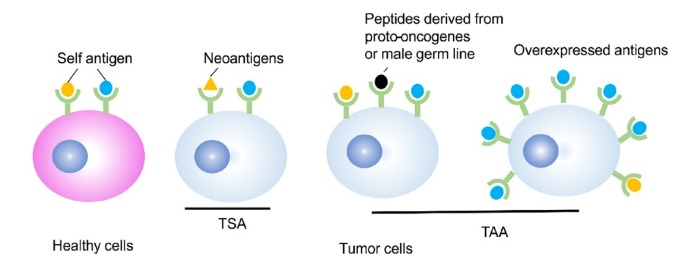
Рисунок 1 | Типы антигенов, экспрессируемых опухолевыми клетками на своей поверхности.
TSA — опухоль-специфичные антигены, TAA — опухоль-ассоциированные антигены (пояснения в тексте) [2].
Наименьшими побочными эффектами, а также наибольшей эффективностью обладают CAR, направленные против неоантигенов, поскольку такие лимфоциты высокоспецифичны в отношении опухоли. CAR на основе опухоль-ассоциированных антигенов также применяются в практике, например, CD19-CAR, применяемые при терапии острого лимфобластного B-лейкоза (ОЛЛ), хронического B-лейкоза (ХЛЛ), а также неходжкинских лимфомах. Однако такие лимфоциты активны в отношении здоровых тканей и могут вызывать тяжелые побочные эффекты вплоть до летальных исходов (on-target/off-tumor эффект) [3–5].
Технология производства CAR-СВ8+-лимфоцитов включает ряд этапов. Все начинается с афереза лейкоцитов периферической крови пациента. Необходимо собрать не менее 100×106 клеток, поэтому забор крови лучше начинать до проведения химиотерапии, поскольку она подавляет лейкопоэз [6].
На втором этапе проводится активация CD8+-лимфоцитов с помощью антител к CD3/CD28 и цитокинов (например, интерлейкина-2). В настоящее время используются более эффективные методы с использованием дендритных клеток пациента [7, 8].
Третьим важным этапом является введение в Т-лимфоциты генетической информации, необходимой для экспрессии CAR. В настоящее время используется три подхода: вирусная трансдукция, введение траспозонов и введение непосредственно мРНК.
Для трансдукции используются гамма-ретровирусные и лентивирусные векторы. Первые дешевле и могут быть получены в большом количестве, преимуществами вторых является большая стабильность и безопасность в плане злокачественной трансформации. Несмотря на потенциальные риски, до настоящего времени в клинических исследованиях не было зарегистрировано ни одного случая появления опухолевого клона Т-лимфоцитов после введения гамма-ретровирусов [8-10]. Механизм действия вирусных векторов представлен на рисунке 2.
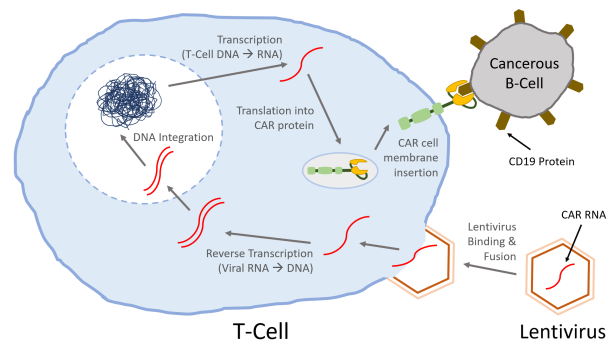
Рисунок 2 | Механизм действия вирусных векторов. С помощью специальных клеточных линий-продуцентов создается вирусная частица, несущая ген CAR вместе с белками, обеспечивающими его транскрипцию. Проникая внутрь клетки, ген CAR либо внедряется в геном, либо экспрессируется в цитоплазме, а его белковый продукт (собственно CAR) транспортируется к мембране клетки и фиксируется на ее поверхности [11].
Системы транспозон/транспозаза используют генетический вектор, транспозон, представленный закольцованным фрагментом ДНК с геном CAR, и фермент транспозазу, который вырезает необходимый фрагмент из транспозона после его внедрения в клетку и встраивает в геном, обеспечивая транскрипцию. Преимуществами этого метода являются его безопасность и дешевизна, однако он не получил широкого распространения. В настоящее время активно применяются две системы — Sleeping Beauty и Piggybag [12]. Механизм работы представлен на рисунке 3.
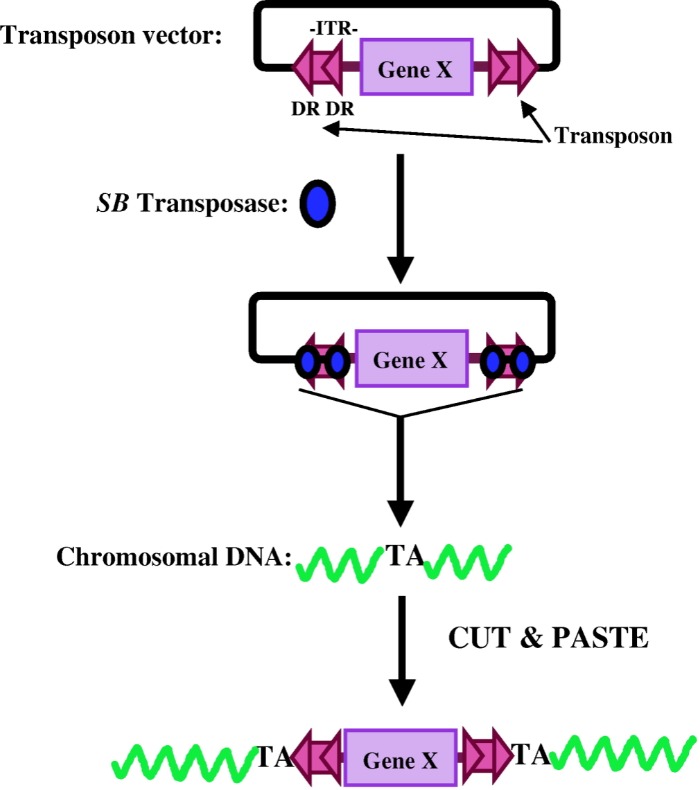
Рисунок 3 | Механизм работы системы транспозон/транспозаза (подробности в тексте) [13].
С помощью мРНК-электропорации можно ввести мРНК, кодирующую CAR, внутрь Т-лимфоцита. При этом CAR будет экспрессироваться до тех пор, пока функционирует введенная мРНК, что составляет в среднем 1–2 недели. С одной стороны это является минусом метода, поскольку в ряде случаев приходится многократно вводить новые порции CAR-CD8+-лимфоцитов. С другой же эта система может найти применение против опухоль-ассоциированных антигенов, поскольку временный эффект позволяет контролировать побочные эффекты [14, 15]. Механизм действия представлен на рисунке 4.
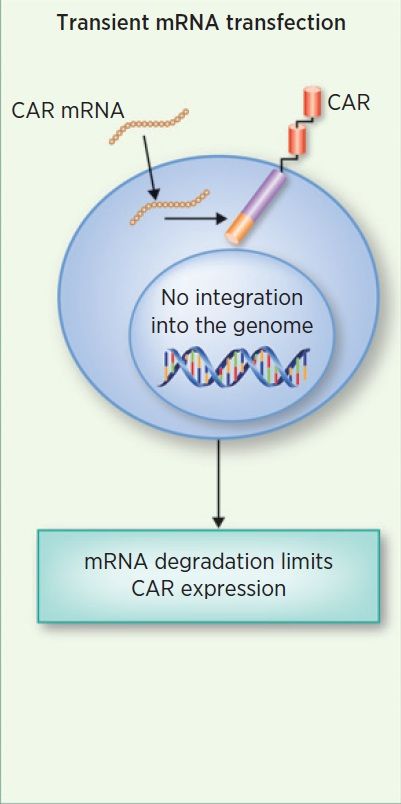
Рисунок 4 | Механизм работы мРНК-электропорации (подробности в тексте) [16].
Следующим этапом является выделение и экспансия Т-лимфоцитов с CAR. Культивирование CAR-CD8+-лимфоцитов обычно осуществляется в биореакторах, в которых поддерживается оптимальный газовый состав, содержание питательных веществ, температура и перемешивание клеток. Чтобы стимулировать пролиферацию, в среду добавляются такие цитокины, как ИЛ-2, ИЛ-7, ИЛ-15. Кроме того, возможно применение антиген-презентирующих клеток, как на втором этапе. В настоящее время часто используются системы, в которых в автоматическом режиме осуществляются этапы со второго по четвертый, например, биореактор Prodigy (Miltenyi Biotec) [17].
Последним этапом служит контроль качества полученного продукта и введение CAR-CD8+-лимфоцитов пациенту. При этом количество клеток и кратность введения зависят от вида злокачественной опухоли и характеристик используемых CAR-CD8+-лимфоцитов. Общая схема этого вида иммунотерапии представлена на рисунке 5.
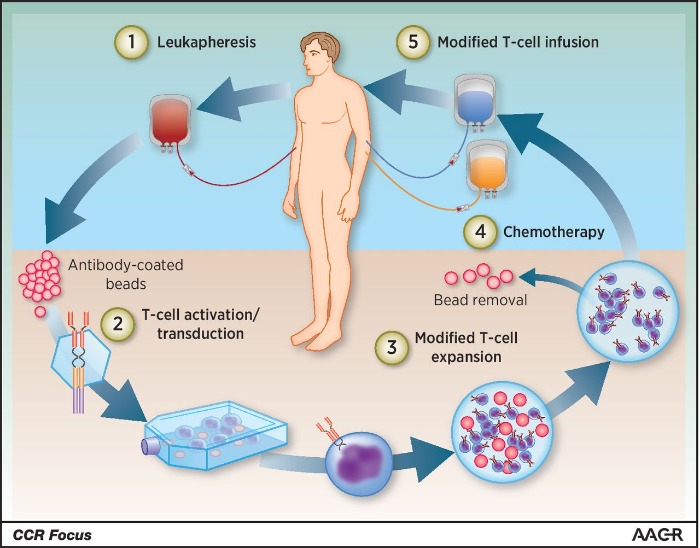
Рисунок 5 | Общая схема этапов иммунотерапии с использованием CAR-CD8+-лимфоцитов [16].
Побочные эффекты и методы их преодоления, а также реальные клинические результаты этого метода лечения онкологических заболеваний будут разобраны в следующих статьях.
Источники:
- Vigneron N. Human Tumor Antigens and Cancer Immunotherapy. BioMed Research International. 2015;2015:948501. doi:10.1155/2015/948501.
- Erratum: Borderud SP, Li Y, Burkhalter JE, Sheffer CE and Ostroff JS. Electronic cigarette use among patients with cancer: Characteristics of electronic cigarette users and their smoking cessation outcomes. Cancer. doi: 10.1002/ cncr.28811. Cancer. 2015;121(5):800.
- Maher J., Wilkie S. CAR mechanics: driving T cells into the MUC of cancer. Cancer Res 2009;69(11):4559–62. DOI: 10.1158/0008-5472.CAN-09-0564.
- Sadelain M., Brentjens R., Rivière I. The basic principles of chimeric antigen receptor design. Cancer Discov 2013;3(4):388–98.
- Wang X., Rivière I. Clinical manufacturing of CAR T cells: foundation of a promising therapy. Mol Ther Oncolytics 2016;3:16015. DOI: 10.1038/mto.2016.15.
- Kochenderfer J.N., Dudley M.E., Kassim S.H. et al. Chemotherapy-refractory diffuse large B-cell lymphoma and indolent B-cell malignancies can be effectively treated with autologous T cells expressing an anti-CD19 chimeric antigen receptor. J Clin Oncol 2015;33:540–9. DOI: 10.1200/JCO.2014.56.2025.
- Vacchelli E., Vitale I., Eggermont A. et al. Trial watch: Dendritic cell-based interventions for cancer therapy. Oncoimmunology 2013;2:e25771. DOI: 10.4161/onci.25771.
- Suerth J.D., Schambach A., Baum C. Genetic modification of lymphocytes by retrovirus-based vectors. Curr Opin Immunol 2012;24(5):598–608. DOI: 10.1016/j.coi.2012.08.007.
- Ghani K., Wang X., de Campos-Lima P.O. et al. Efficient human hematopoietic cell transduction using RD114- and GALVpseudotyped retroviral vectors produced in suspension and serum-free media. Hum Gene Ther 2009;20:966–74.
- Throm R.E., Ouma A.A., Zhou S. et al. Efficient construction of producer cell lines for a SIN lentiviral vector for SCID-X1 gene therapy by concatemeric array transfection. Blood 2009;113:5104–10. DOI: 10.1182/blood-2008-11-191049.
- Riviere, I., et al. “Hematopoietic Stem Cell Engineering at a Crossroads.” Blood, vol. 119, no. 5, 17 Nov. 2011, pp. 1107–1116., doi:10.1182/blood-2011-09-349993.
- Singh H, Huls H, Kebriaei P, Cooper LJ. A new approach to gene therapy using Sleeping Beauty to genetically modify clinical-grade T cells to target CD19. Immunol Rev. 2014;257(1):181-90.
- Geurts AM, Yang Y, Clark KJ, et al. Gene transfer into genomes of human cells by the sleeping beauty transposon system. Mol Ther. 2003;8(1):108-17.
- Zhao Y., Zheng Z., Cohen C.J. et al. High-efficiency transfection of primary human and mouse T lymphocytes using RNA electroporation. Mol Ther 2006;13(1):151–9. DOI: 10.1016/j.ymthe.2005.07.688.
- Birkholz K., Hombach A., Krug C. et al. Transfer of mRNA encoding recombinant immunoreceptors reprograms CD4+ and CD8+ T cells for use in the adoptive immunotherapy of cancer. Gene Ther 2009;16(5):596–604. DOI: 10.1038/gt.2008.189.
- Maus MV, June CH. Making Better Chimeric Antigen Receptors for Adoptive T-cell Therapy. Clin Cancer Res. 2016;22(8):1875-84.
- Kumaresan P., Figliola M., Moyes J.S. et al. Automated cell enrichment of cytomegalovirus-specific T cells for clinical applications using the cytokine-capture system. J Vis Exp 2015;(104). DOI: 10.3791/52808.
