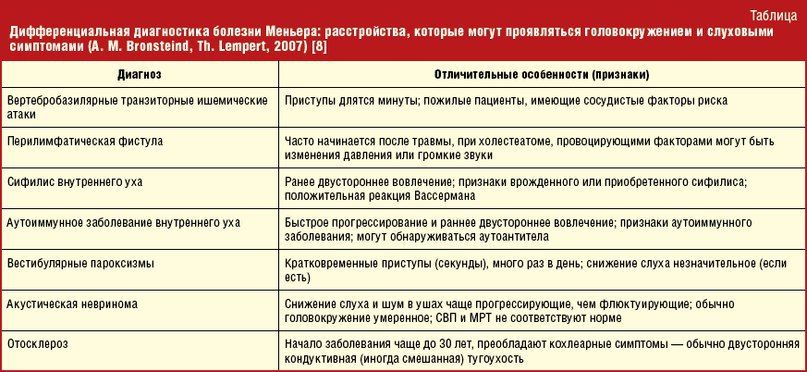
Болезнь Меньера

Головокружение, являясь крайне распространенной жалобой при первичном осмотре, нередко не рассматривается врачами как важный симптом. Однако за ним может скрываться очень грозная патология, такая как болезнь Меньера (idiopathic endolymphatic hydrops, или идиопатическая эндолимфатическая водянка, лабиринтная водянка).
Данное заболевание впервые было описано в 60-х годах девятнадцатого столетия французским врачом Проспером Меньером (Prosper Meniere, 1861) в докладе «Об особом виде тяжелой глухоты, зависящей от поражения внутреннего уха» на заседании французской Академии медицинских наук.
Что же включает в себя данная патология?
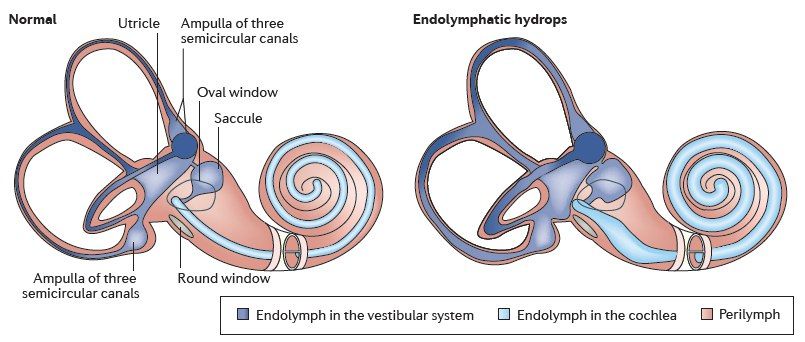
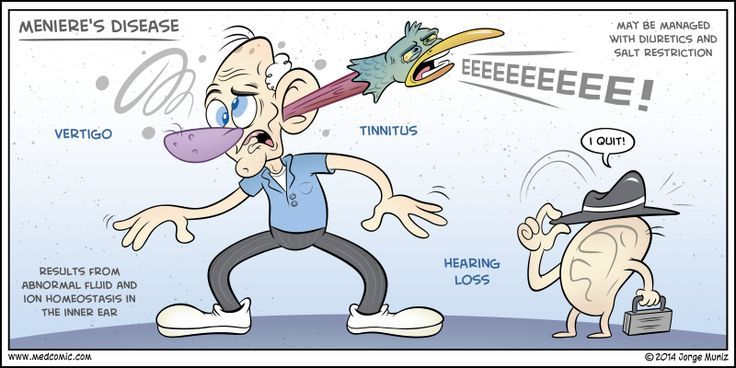
Болезнь Меньера характеризуется развитием симптомокомплекса, включающего в себя «колеблющуюся» или преходящую потерю слуха, случайные эпизодические головокружения (иногда насильственные), шум или звон в ушах (обычно ревущий, низкотональный) и слуховую «полноту» (например, чувство давления, дискомфорт, ощущения «распирания» в ухе). В основе этих симптомов лежит увеличение объема эндолимфы (лабиринтной жидкости) и повышение давления в самом лабиринте.
Этиология
По определению, болезнь Меньера является идиопатической. Другими словами, если причина известна, патологический процесс уже не может быть назван болезнью Меньера. Тем не менее, если корень проблемы заключается в повышении эндолимфатического давления, стоит рассмотреть и другие причины гидропса. Болезнь Меньера в таких случаях следует отличать от этих причин.
Существует несколько теорий, пытающихся объяснить причину возникновения данной патологии:
Аутоиммунные заболевания, такие как волчанка и ревматоидный артрит, могут вызывать воспалительную реакцию в пределах лабиринта. Аутоиммунная этиология была подтверждена после того, как было установлено, что у пациентов с БМ определяются аутоантитела к щитовидной железе, а также иммунные комплексы в эндолимфатическом мешке (иммунологическая теория).
Заболевания, которые могут привести к повышению эндолимфатического давления, включают метаболические нарушения, гормональный дисбаланс, травмы, а также различные инфекции (например, сифилитический отит и синдром Когана — интерстициальный кератит). Отдельно следует остановиться на метаболических нарушениях. Имеется предположение, что повышение уровня калия в эндолимфатическом пространстве вызывает повреждение волосковых клеток и вестибулярного эпителия, что приводит к развитию симптомов головокружения и тугоухости (метаболическая теория).
Кроме того, замечено, что при болезни Меньера частота аллергических реакций выше, чем среди населения в целом (у 50 % установлено наличие аллергии к веществам, передающимся по воздуху). Пищевые триггеры также являются важными факторами при возникновении БМ (у 45 % больных с аллергией на пищевые продукты) — аллергическая теория.
Также выделяют сосудистую теорию (в связи с частым сочетанием БМ и мигрени у больных), генетическую (аутосомно-доминантный тип наследования, участок DFNA9 гена СОСН) и анатомическую (патология височной кости, в результате чего малый по размеру эндолимфатический мешок расположен позади лабиринта).
Клиническая картина
В двух из трех случаев обращения с жалобами на головокружение или потерю слуха процесс чаще всего является односторонним.
Первыми проявлениями при БМ, как описано выше, могут стать как вестибулярные нарушения (вертиго), так и слуховые (снижение остроты слуха, наличие шума в ушах).
Выделяют 3 формы БМ:
- Классическая (слуховые + вестибулярные нарушения);
- Кохлеарная (слуховые нарушения с постепенным присоединением вестибулярных);
- Вестибулярная (картина манифестации нарушений обратна кохлеарной форме);
При классическом течении БМ выделяют 3 стадии заболевания:
- Характерна преходящая глухота в сочетании с головокружением продолжительностью от 2 до 4 часов с выраженными вегетативными проявлениями (повышенная потливость, тошнота, рвота и др.). Данный приступ может возникать в любое время суток. Больные отмечают, что практически сразу после уменьшения головокружения улучшается слух, вплоть до полного возврата к норме. Такие приступы (status meniericus) бывают нечасто, не более 2-х раз за 2–3 года.
- Происходит прогрессирование потери слуха с каждым приступом (без взаимосвязи с головокружением). Шум в ушах, чувство заложенности/ощущение распирания в пораженном ухе приобретают постоянный характер. Головокружение достигает возможного максимума, с крайней степенью выраженности вегетативных проявлений (при дальнейшем прогрессировании имеется тенденция к уменьшению тяжести проявлений). Эти приступы появляется чаще, чем при I стадии (несколько раз в месяц).
- Выраженное снижение слуха на пораженном ухе, при котором нередко вовлекается и здоровое ухо. При этом приступы головокружения не характерны. При данной стадии БМ характерны кризы Тумаркина (приступы «внезапного падения») вследствие гиперактивации вестибулярных рефлексов из-за смещения отолитовых рецепторов.
Достоверная (очевидная) БМ по рекомендациям AAO-HNS (Американская академия отоларингологии и хирургии головы и шеи), JSER (Японское общество по изучению равновесия) и EAONO (Европейская академия отологии и нейро-отологии) представляет собой:
- два или более самопроизвольно возникающих приступа головокружения продолжительностью 20 мин и более;
- потеря слуха, подтвержденная данными аудиологических исследований по меньшей мере в одном случае;
- шум в ушах или ощущение заложенности в пораженном ухе.
При исключении других причин, в результате которых может развиться вышеописанная симптоматика.
Диагностика
На данный момент универсального способа диагностики БМ не существует, учитывая специфику течения заболевания и комбинированность различных симптомов поражения. Исходя их этого, диагностика болезни Меньера носит «всеобъемлющий» характер.
Традиционные тесты:
- проба Ромберга;
- тест Фукуды/маршевая проба;
- указательная проба Барани;
- проба Бабинского-Вейля;
- проба Ринне/Вебера.
В дополнение к этому проводят калорические пробы, вращательный тест Барани и др.
Инструментальная диагностика включает в себя:
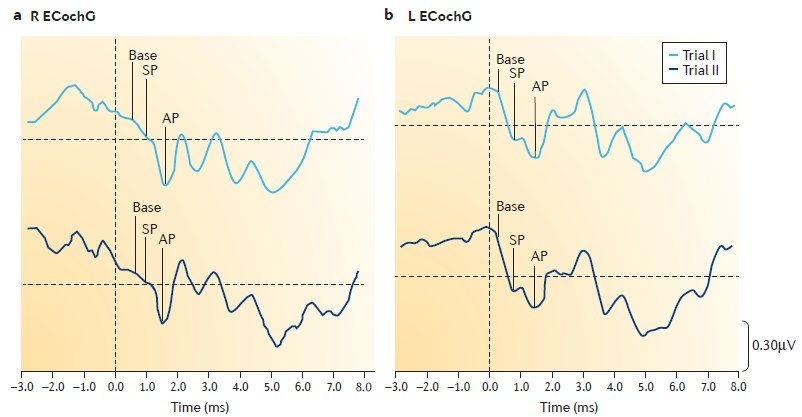
- экстра - и транстимпанальную электрокохлеографию (ЭКоГ);
- аудиометрию (тональная пороговая, надпороговая, речевая).
При ЭКоГ измеряется соотношение суммарного потенциала (СП) и потенциала действия (ПД). При БМ — СП/ПД> 0,3.
Для верификации диагноза рекомендуется применение дегидратационного теста, при котором после проведения тоновой пороговой аудиометрии больному вводят осмотический диуретик из расчёта 1–1,5 мг на кг массы тела пополам с фруктовым соком и повторяют аудиометрию через 1, 2, 3, 24 и 48 часов.
Оценка результатов дегидратации ведется по следующим критериям: проба считается «положительной», если через 2–3 часа после приема препарата пороги тонального слуха снижаются не менее чем на 5 дБ на всем диапазоне исследуемых частот или на 10 дБ на трех частотах, и улучшается разборчивость речи не менее, чем на 12 %. Проба считается «отрицательной», если пороги тонального слуха через 2–3 часа повышаются и ухудшается разборчивость речи относительно исходного уровня. Промежуточные варианты расцениваются как «сомнительные».
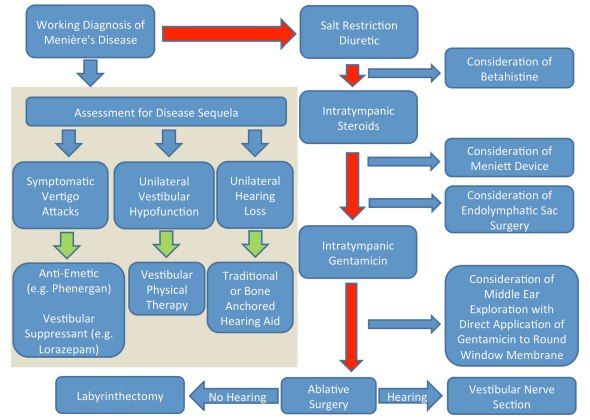
Лечение
Основной целью лечения болезни Меньера является оказание помощи при острых приступах головокружения, предотвращение повторных атак и устранение прогрессирующего ухудшения слуха и вестибулярной функции в пораженном ухе (или ушах). Несмотря на прогресс в достижении первых двух целей, устранение прогрессирующего во времени ущерба слуху и вестибулярной функции оказалось недостижимым на данный момент времени. Здесь необходимо напомнить, что БМ часто ассоциируется с такими патологиями, как мигрень, СОАС, аутоиммунными заболеваниями, коагулопатиями/васкулопатиями, поэтому было высказано предположение, что цереброваскулярная ишемия способствует увеличению частоты возникновения атак. Необходимо провести тщательный поиск факторов риска сосудистых заболеваний и по возможности их коррекцию. У людей младше 50 лет мигрень является наиболее распространенным кофактором БМ. С коррекцией приступов мигрени, а также их профилактикой в межприступный период вы можете ознакомиться в нашем обзоре. У людей старше 50 лет, для которых характерна полиморбидность, сопутствующие БМ нозологии также требуют своевременной коррекции ввиду возможного влияния на прогрессирование БМ.
Диуретики, использующиеся в качестве терапии первой линии ввиду их возможности уменьшения объема эндолимфы, в результате которого предотвращается формирование гидропса, также весьма неоднозначны в их назначении в ситуации с БМ. Существуют 2 противоположные группы исследований, одна из которых говорит, что их назначение оправдано, особенно у женщин в период менопаузы. Другие же заявляют, что эффект, полученный от их применения, сравним с плацебо. Но не стоит забывать, что комплекс проводимой терапии должен подбираться индивидуально. В случае БМ наиболее часто назначают комбинацию гидрохлортиазида с триамтереном или диакарб. Касаемо ацетазоламида, его назначение оправдано в ситуациях, когда БМ сочетается с мигренью с аурой, или в качестве терапии второй линии, когда препараты, используемые в качестве профилактики мигрени в межприступный период, не оказывают должного эффекта.
Также необходимо помнить о таком препарате, как бетагистина дигидрохлорид — синтетический аналог гистамина (Н3 подгруппа), который по некоторым данным должен составлять основу терапии острых приступов головокружений. Однако здесь стоит сказать, что существует достаточно большая подборка исследований, свидетельствующая о неоднозначности его применения. Так, в январе 2016 года British Medical Journal (BMJ) на основе данных нескольких Кокрановских обзоров пришел к выводу, что бетагистин вряд ли можно считать эффективным в отношении БМ. Они связали его широкое применение, возможно, с высокой толерантностью в отношении дозирования препарата, низкими рисками развития нежелательных реакций, а также банальным отсутствием альтернативы. В поддержку вышесказанному, в том же 2016 году было проведено многоцентровое исследование BEMED (1450 обследованных пациентов), по результатам которого показано, что назначение как низких (48 мг/сут), так и высоких доз (144 мг/сут) этого препарата не показало значительного влияния на снижение частоты острых приступов головокружений, а также на восстановление слуха и вестибулярных функций по сравнению с контрольной группой. Это еще раз подтверждает неоднозначность назначения данного препарата.
Поэтому в качестве альтернативы бетагистину можно предложить Н1-блокаторы, которые способны проникать через ГЭБ. К ним относят дименгидринат, дифенгидрамин, меклозин.
В ряде случаев оправдано использование седативных средств, например, лоразепама/диазепама при остром приступе головокружения. Симптоматический эффект седативных средств при остром головокружении связан с их общим действием, в условиях которого снижается способность вестибулярных ядер анализировать и интерпретировать импульсы, поступающие из лабиринта.
Хирургическое лечение, согласно критериям AAO-HNS, рекомендуется при неэффективности консервативной терапии в течение 6 месяцев.
Источники:
- Foster C. A. Optimal management of Ménière’s disease // Therapeutics and clinical risk management. – 2015. – Т. 11. – С. 301.
- Sharon J. D. et al. Treatment of Meniere’s disease // Current treatment options in neurology. – 2015. – Т. 17. – №. 4. – С. 14.
- Nakashima T. et al. Meniere's disease // Nature reviews. Disease primers. – 2016. – Т. 2. – С. 16028-16028.
- Zhang Y. et al. Characteristics of the Cochlear Symptoms and Functions in Meniere's Disease // Chinese medical journal. – 2016. – Т. 129. – №. 20. – С. 2445.
- Зайцева О. В. Болезнь Меньера: в помощь практическому врачу // РМЖ. – 2016. – Т. 24. – №. 21. – С. 1421-1425.
