Митохондриальные аспекты воспаления
Врожденный иммунный ответ обеспечивает эффективную защиту, когда иммунные клетки распознают молекулярные паттерны чужеродных организмов, например, липополисахариды бактерий. Нарушения в сигнальных путях способны привести к аутоиммунным расстройствам. Расширение представлений о регуляции врожденных иммунных реакций способно обеспечить совершенствование терапии таких патологий.
Обнаружено, что митохондрии могут регулировать реакцию иммунных клеток на инфекцию и альтерацию тканей. Эти органеллы могут генерировать про- или противовоспалительные сигналы, изменяя уровни метаболитов, продуцируемых в цикле Кребса, или изменяя уровень продукции активных форм кислорода (АФК).
Инфламмасома — мультипротеиновый цитоплазматический комплекс, координирующий процесс воспалительной реакции. В ее состав входят различные сенсорные элементы, адапторные белки и зимоген каспазы-1. Инфламмасомы, которые содержат белок NLRP3 (NOD-подобный рецептор 3), могут образовываться в макрофагах, и начальные этапы сборки данных комплексов изучены: если липополисахарид связывается с рецепторным белком TLR4 на поверхности макрофагов, происходит активация сигнального пути NF-κB. Это вызывает увеличение экспрессии NLRP3, активацию каспазы-1 (IL-1β конвертирующего энзима или ICE). В итоге осуществляется превращение проинтерлейкина-1β и проинтерлейкина-18 в зрелые биологически активные пептиды.
Одним из триггеров каспазной активности могут быть митохондриальные ДНК [1].
В исследовании Zhong с коллегами изучали мышей, в иммунных клетках которых отсутствовал белок TFAM (транскрипционный фактор А митохондрий), необходимый для репликации митохондриальной ДНК. Это привело к потере митохондриальной ДНК, наряду с чем регистрировалась дефектная активация воспаления. При переносе синтетической окисленной митохондриальной ДНК в клетки макрофагов, выращенные in vitro от животных с отсутствующим TFAM, обнаруживалась активация воспаления в ответ на контакт с липополисахаридами бактерий.
Связывание липополисахарида с TLR4 активирует путь регулирования экспрессии фермента цитидинмонофосфат-киназы 2 (ЦMФK2), который необходим для продуцирования цитидинтрифосфата (ЦТФ) (рис. 1). В мышиных макрофагах с отсутствием ЦMФK2 обнаруживалась недостаточная активация воспаления [2].
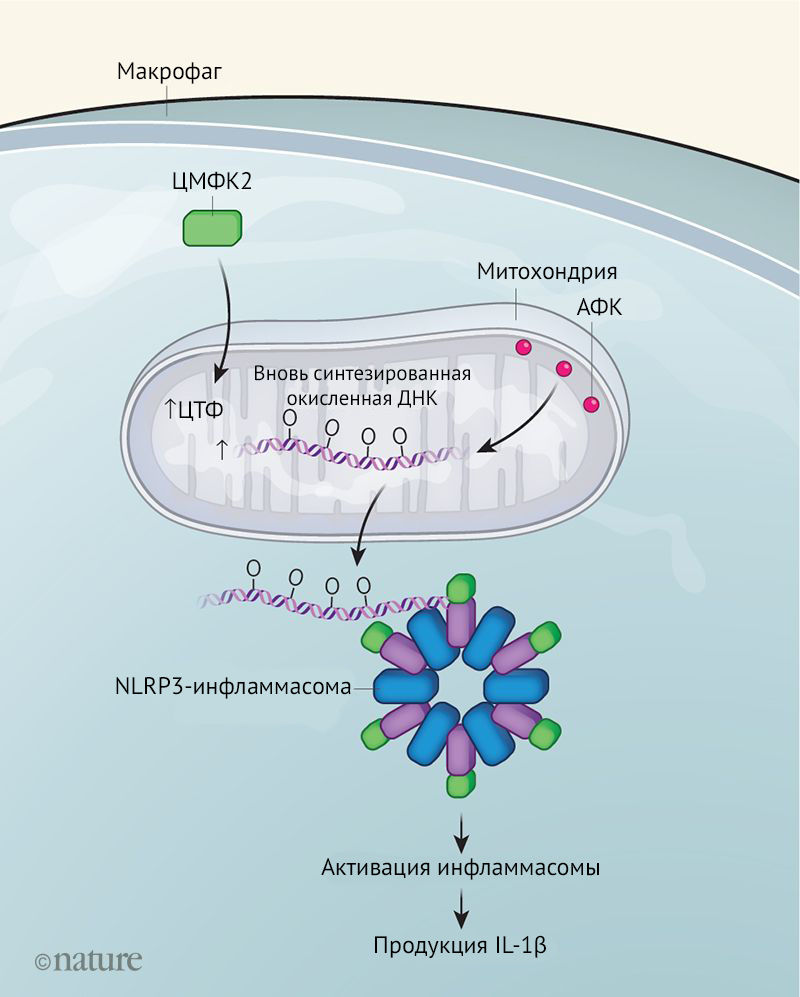
Как возникают АФК, необходимые для окисления ДНК? Во-первых, любое неспецифическое повреждение органелл способно привести к их синтезу в ходе окислительно-восстановительных реакций. Даже в нормальных, физиологических условиях 1–5 % кислорода, потребленного митохондриями, преобразуется в супероксидные анион-радикалы (О–•), которые сами относительно инертны, но являются предшественниками таких АФК, как пероксид водорода (Н2О2) и гидроксид-радикалы (ОН•). Также молекулы сукцината, которые накапливаются после стимуляции ЛПС, окисляются, чтобы стимулировать выработку митохондриальных АФК [3]. Еще один важный пункт — выход фрагментов окисленной митохондриальной ДНК в цитоплазму. Одним из кандидатов в «контрольно-пропускной пункт» является переходная пора проницаемости митохондрий, которая формируется в ответ на повышенные уровни активных форм кислорода. Также предполагается, что митохондрии могут формировать микровезикулы, содержащие окисленную ДНК [4].
Уникальное происхождение митохондрий в ходе эволюции обуславливает также и их роль в вирус-опосредованных иммунных реакциях. Митохондрии являются потомками эндосимбиотических бактерий и сохраняют важные прокариотические свойства, такие как компактный кольцевой геном. Следовательно, у млекопитающих митохондриальная ДНК подвергается двунаправленной транскрипции, которая генерирует перекрывающиеся транскрипты, способные образовывать длинные двухцепочечные структуры РНК. Обнаружено, что наличие высоко нестабильных молекул нативных митохондриальных двухцепочечных РНК в цитоплазме регулирует активность сигнального пути MDA5 (melanoma-differentiation-associated gene 5, член семейства РНК-хеликазных рецепторов), который запускает реакцию на интерферон I типа [5].
Возникновение митохондрий как отдельных, первоначально чужеродных организмов (теория симбиогенеза) объясняет их важную роль при аутоиммунных воспалительных реакциях и делает их перспективной мишенью иммунорегуляторной терапии.
Источники:
- Swanson K.V. The NLRP3 inflammasome: molecular activation and regulation to therapeutics. Nature Reviews Immunology.2019;19:477–489.
- Zhong Z.et al. New mitochondrial DNA synthesis enables NLRP3 inflammasome activation. Nature.2018; 560(7717):198.
- Bambouskova M. et al. Electrophilic properties of itaconate and derivatives regulate the IκBζ-ATF3 inflammatory axis. Nature. 2018;556(7702):501-504.
- Mills E.L.et al. Itaconate is an anti-inflammatory metabolite that activates Nrf2 via alkylation of KEAP1. Nature. 2018;556(7699):113-117.
- Dhir A.et al. Mitochondrial double-stranded RNA triggers antiviral signalling in humans. Nature. 2018;560(7717):238-242.
