Мелкоклеточный рак легкого
Заболеваемость и смертность от мелкоклеточного рака легких во всем мире делают эту болезнь заметной проблемой для здравоохранения. Диагноз основывается на результатах гистологии, для подтверждения проводят иммуногистохимические исследования в сложных случаях. Типичными пациентами являются мужчины старше 70 лет, которые были раньше или являются сейчас заядлыми курильщиками и которые имеют сопутствующие заболевания дыхательной и сердечно-сосудистой систем. Симптомы могут начать быстро проявляться из-за локального внутригрудного роста опухоли, внелегочного отдаленного распространения, паранеопластических синдромов или комбинации этих особенностей [2]. Термин МРЛ впервые введен в 1926 году, когда было признано его эпителиальное происхождение [2].
Эпидемиология
Рак легких является причиной 12 % всех выявленных случаев рака во всем мире и основной причиной смерти от рака в США [4]. МРЛ представляет 13 % всех вновь диагностированных случаев рака легких во всем мире, или более 180 000 случаев в год. В развитых странах распространенность МРЛ снизилась за последние 30 лет, вероятно, из-за антитабачной политики. Ожидается увеличение заболеваемости в странах, где распространенность курения остается высокой [2].
Гистология
Хотя в 95% случаях мелкоклеточный рак развивается в легких, он также может возникать во внелегочных участках, включая носоглотку, желудочно-кишечный тракт и мочеполовой тракт. 11-13 Мелкоклеточный рак, как легочный, так и внелегочный, имеющие сходное клиническое и биологические течение, склонны к быстрому метастазированию [3].
МРЛ — это злокачественная опухоль, состоящая из мелких эпителиальных клеток с небольшим количеством цитоплазмы, плохо очерченными клеточными границами, мелкозернистым ядерным хроматином и отсутствующими или незаметными ядрышками» (рис. 1). Клетки могут иметь круглую, овальную или веретенообразную формы. Типичный МРЛ включает только небольшие клетки и составляет около 90% всех случаев. Есть случаи, при которых опухоль содержит крупноклеточные компоненты [2,3]. С вероятностью 30 % при вскрытиях у пациентов с МРЛ выявляют участки немелкоклеточной дифференцировки карцином. Это чаще всего выявляется в образцах, полученных от ранее пролеченных пациентов и предполагает, что канцерогенез в легких происходит в плюрипотентных стволовых клетках, способных к дифференцировке по разным путям [3].
.
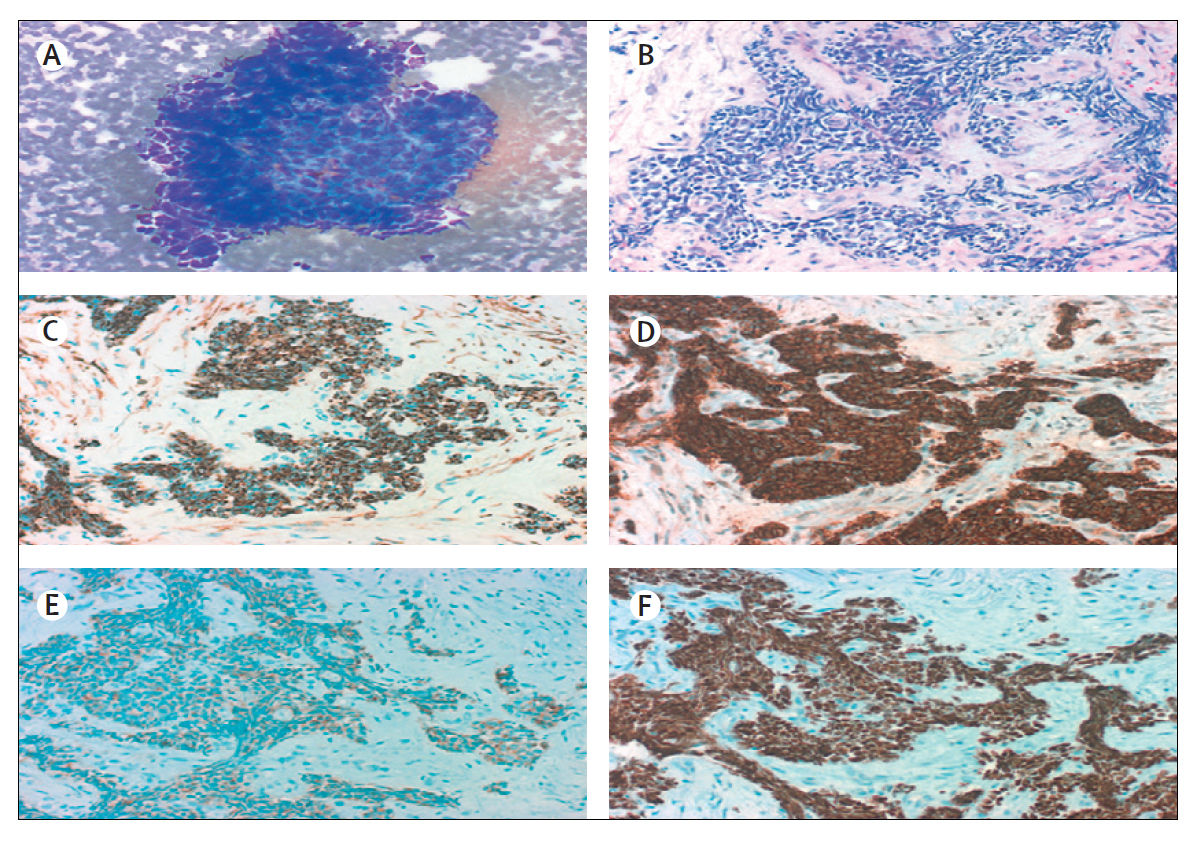
(B) Клетки могут быть круглыми, овальными или веретенообразными, и клеточная стенка видна редко. Группы клеток могут формировать розетки. В опухоли часто определяются некрозы (окраска гематоксилином и эозином, увеличение × 200).
При иммуногистохимии результаты для (C) CK-7, нейроэндокринных маркеров (D) CD56 и (E) синаптофизина; и (F) TTF-1 положительны.
Все фотографии предоставлены с разрешения М. Праета и Л. Фердинанде, Гентский университет, Бельгия.
МРЛ можно заподозрить при наличии определенных симптомов и признаков. Для подтверждения диагноза требуются гистологические и цитопатологические исследования. Образцы из первичной опухоли, лимфатических узлов или других метастатических участков получают с помощью бронхоскопии или тонкоигольной аспирационной пункционной биопсии (ТАПБ). Опухоль растет под слизистой бронхов, и, следовательно, бронхоскопия или исследование мокроты могут не дать результатов. Иммуногистохимические исследования проводятся для подтверждения диагноза в сложных случаях. Тест на нейроэндокринные маркеры, такие как хромогранин, синаптофизин и CD56, также может быть полезным — менее 10 % опухолей МРЛ являются отрицательными для всех нейроэндокринных маркеров. Почти все МРЛ являются иммунореактивными в отношении кератина, антигена эпителиальной мембраны и фактора транскрипции щитовидной железы-1 (TTF-1) [3]. Реакция МРЛ на TTF-1 положительна в 90% случаев. Эпителиальные маркеры, такие как цитокератины, обнаруживаются во многих опухолях МРЛ и помогают отличить их от лимфом и других маленьких круглых опухолей. Но отличить мелкоклеточный от немелкоклеточного с помощью маркеров трудно [2].
Первыми описали отчетливые клинические особенности МРЛ Watson и Berg: центральное расположение на рентгенографии грудной клетки, тенденцию к раннему распространению, высокую чувствительность к химиотерапии и высокую частоту метастазов при вскрытии. Симптомы начинают проявляться, как правило, в течение 8–12 недель. Наиболее частыми симптомами являются кашель, хрипы, одышка, кровохарканье, вызванное локальным внутрипульмональным ростом опухоли; симптомы, обусловленные внутригрудным распространением на стенку грудной клетки, верхней полой веной или пищеводом, боль, усталость, анорексия и неврологические жалобы, вызванные отдаленное распространение и паранеопластические синдромы [2].
Предпочтительными участками для метастазирования являются мозг, печень, надпочечники, кости и костный мозг. МРЛ является наиболее частой причиной паранеопластических синдромов. Эти синдромы следует активно исключать всякий раз, когда у пациента проявляются какие-либо из их признаков. Наиболее частыми проявлениями синдромов со стороны эндокринной системы являются синдром неадекватного антидиуреза и синдром Кушинга. Известно о субклинических проявлениях обоих. Дерматологические аномалии, специфически связанные с МРЛ, включают приобретенный тилоз, трипальные пальмы и эритему. Редкими проявлениями являются дерматомиозит, гипергликемия, гипогликемия, гиперкальциемия и гинекомастия [2,4].
Классификация
Мелкоклеточный рак легкого входит в группу эпителиальных бронхопульмональных нейроэндокринных (НЭ) опухолей. Все НЭ опухоли легкого являются злокачественными новообразованиями и представлены четырьмя основными подтипами [1]:
1) типичный карциноид (ТК);
2) атипичный карциноид (АК);
3) крупноклеточный НЭ рак (КНЭР);
4) мелкоклеточный рак (МРЛ).
При этом ТК и АК являются высокодифференцированными нейроэндокринными опухолями с низкой степенью злокачественности (G1 и G2), а КНЭР и МРЛ — это низкодифференцированные нейроэндокринные опухоли с высокой степенью злокачественности (G3) [1,4].
Оценка распространенности опухолевого процесса влияет на решение о назначении терапии. После морфологического подтверждения диагноза (бронхоскопия с биопсией, трансторакальная пункция, биопсия метастатических узлов) проводится компьютерная томография (КТ) грудной клетки и брюшной полости, а также КТ или магнитно-резонансная томография (МРТ) головного мозга (с контрастированием) и сканирование костей [1,4].
Классификация, по которой выделяют пациентов с локализованным и распространенным мелкоклеточным раком легкого актуальна [1].
Локализованная стадия — опухоль занимает одну половину грудной клетки с регионарными метастазами в лимфоузлы корней легких с обеих сторон, с метастазами в надключичные узлы и лимфоузлы средостения, а также с выпотом в плевральной полости с этой же стороны.
Распространенная стадия — процесс, выходящий за пределы локализованного. Наличие М1 — это всегда распространенная стадия.
Лечение МРЛ
Распространенная стадия
Первая линия химиотерапии. В течение последних десяти лет комбинации ЕР или ЕС (этопозид + цисплатин / карбоплатин) является стандартом для лечения пациентов с МРЛ. Доказано, что противоопухолевая активность данного лечения при распространенном МРЛ составляет 60–78 % (полный эффект — у 10–20 % больных). Медиана выживаемости — 7,3–11,1 мес. Большинство новых режимов современной химиотерапии основыввется на комбинации ЕР (или ЕС) или путем замены этопозида на другое средство [1].
Вторая линия химиотерапии. Несмотря на высокую чувствительность МРЛ к химио- и лучевой терапии, в большинстве случаев приходится сталкиваться с рецидивом заболевания. В такой ситуации выбор дальнейшей лечебной тактики (химиотерапия второй линии) зависит от ответа пациентов на первую линию лечения, интервала времени, прошедшего после ее окончания, и от расположения метастазов [1,4].
Различают [1]:
• «чувствительный» рецидив — полный или частичный эффект от первой линии химиотерапии и прогрессирование опухолевого процесса не ранее 3 мес. после окончания индукционной терапии)
• «рефрактерный» рецидив, прогрессировавший в процессе индукционной терапии или менее чем через 3 мес. после ее окончания.
У пациентов с рецидивом МРЛ прогноз сомнительный, в особенности при рефрактерном рецидиве. Медиана выживаемости после обнаружения рецидива не превышает 4 месяца. В настоящее время схема CAV стала второй линией лечения МРЛ. Больным с резистентной формой МРЛ назначают химиотерапию второй линии. При этом эффективность отмечается у небольшого процента больных, но применение химиотерапии может стабилизировать болезни и/или замедлить прогрессирование [1].
Третья линия химиотерапии. Эффективность третьей линии химиотерапии распространенного МРЛ остается неизвестной. Больные в третьей линии могут получать таксол, гемцитабин, ифосфамид как в монотерапии, так и в комбинации с цисплатином или карбоплатином. Выживаемость больных с распространенным МРЛ следующая: 1 год после постановки диагноза живут 44 % больных, 1,5 года — 24 %, 2 года — 12 %, 3 года — 6 %, от 3,5 до 5 лет — 4 % больных [1].
Локализованная стадия МРЛ
У 50 % пациентов отмечается полная ремиссия и у них хорошие шансы на полное излечение. Стандартом современного лечения локализованного МРЛ является химиолучевая терапия, которая может проводиться как в одновременном, так и в последовательном режиме. Из всех схем комбинированной химиотерапии для комбинации с облучением наиболее удобной и подходящей оказалась схема этопозид + цисплатин. Лучевая терапия, начинающаяся на первой или второй неделе химиотерапии («ранняя ЛТ»), может проводиться в разовой дозе 1,5–2 Гр и суммарной дозе 45–50 Гр. Эффективность современной терапии при локализованном МРЛ колеблется от 65 до 90 %, с полной регрессией опухоли у 45–60 % больных и медианой выживаемости 18–24 мес [1].
Лучевая терапия МРЛ
Применяется у пациентов с локализованной и распространенной стадиями болезни. В результате отмечается регрессия опухоли в 60–80 % случаях, но отдельно от химиотерапии не увеличивает продолжительность жизни из-за появления отдаленных метастазов. Без облучения локальное прогрессирование болезни встречается у 80 % больных с локализованным МРЛ, получавших только химиотерапию. Лучевая терапия также проводится у больных с распространенной стадией (при метастазах в кости, в мягкие ткани, мозг). При появлении метастазов в мозге ЛТ является основным методом лечения. Химиолучевая терапия улучшает результаты лечения и увеличивает продолжительность жизни [1,4].
Профилактическое облучение мозга
Метастазы в головной мозг появляются у 20–30 % пациентов к моменту установления диагноза МРЛ и часто протекают бессимптомно. Иногда появление метастазов в головном мозге является первым симптомом МРЛ. Профилактическое облучение (ПОМ) показано больным с невыявленными метастазами в мозге, т. к. шансы на появление их в ближайшие 1,5–2 года достигают 70 % [1].
Таргетная терапия МРЛ
Молекулярно-генетические механизмы МРЛ разнообразны и пока недостаточно изучены. Для МРЛ характерны делеция хромосомы 3р, мутации гена р53, экспрессия Bcl-2, активация теломеразы и немутантного c-kit у 75–90 % пациентов. При МРЛ наблюдаются и другие молекулярные нарушения: экспрессия VEGF, потеря гетерозиготности хромосом 9р и 10q у большинства пациентов. Аномалии KRAS и р16 при МРЛ относительно редки. Многие таргетные препараты были изучены при МРЛ, но это не изменило клинические подходы и возможности терапии этого заболевания [1,2].
Хирургическое лечение МРЛ
Хирургическое лечение является доказанным методом выбора только у пациентов с I стадией болезни. Операция возможна у больных МРЛ и со II стадией, но клинических исследований недостаточно. При I стадии МРЛ 5-летняя выживаемость после операции — 48–50 %, а при II стадии — 32–39 %. Хирургическое лечение МРЛ также возможно у пациентов с неуточненным морфологичеким диагнозом и при наличии смешанных форм (с мелкоклеточным и немелкоклеточным компонентами). Во всех случаях через 2–3 нед. после оперативного вмешательства необходимо проведение адъювантной ХТ (4 курса с интервалами 3–4 нед.). Схемы адъювантной ХТ: этопозид + карбоплатин или этопозид + цисплатин [1].
Источники:
1. Бычков М.Б., Горбунова В.А. Клинические рекомендации по диагностике и лечению больных раком легкого // М.: Общероссийский союз общественных объединений ассоциация онкологов России. – 2014.
2. Fennell D. A. et al. Small-cell lung cancer //Lancet (London, England). – 2011. – Т. 378. – №. 9804. – С. 1741-1755.
3. Kalemkerian G. P. et al. Small cell lung cancer //Journal of the National Comprehensive Cancer Network. – 2013. – Т. 11. – №. 1. – С. 78-98.
4. Kalemkerian G. P. et al. NCCN guidelines insights: Small cell lung cancer, Version 2.2018 //Journal of the National Comprehensive Cancer Network. – 2018. – Т. 16. – №. 10. – С. 1171-1182.
