Изучена связь между воспалением и раком поджелудочной железы
Новое открытие исследователей из Онкологического центра им. М. Д. Андерсона Техасского университета проясняет аспекты давно установленной связи между воспалением и развитием рака поджелудочной железы. Согласно результатам исследования, опубликованного 16 сентября в «Science», в клетках поджелудочной железы обнаружены признаки адаптационной реакции в ответ на рекуррентные эпизоды воспаления, изначальное значение которой состоит в обеспечении защиты от повреждения тканей. Однако такой адаптивный ответ может способствовать развитию опухолевой ткани в присутствии мутантного гена KRAS.
В своей работе авторы показали, что действие мутантного гена KRAS, обнаруживаемого в 95 % всех случаев рака поджелудочной железы, способствует поддержанию такой адаптивной реакции, что выражается в давлении естественного отбора в пользу канцерогенной мутации.
По заявлению Андреа Виале, автора-корреспондента, M.D. и доцента кафедры геномной медицины, ученым удалось обнаружить длительное транскриптомное и эпигенетическое перепрограммирование эпителиальных клеток вследствие единичного преходящего эпизода воспаления. Также удалось выяснить, что внутриклеточные взаимодействия с онкогеном KRAS способствовали развитию опухолей поджелудочной железы даже по прошествии длительного периода времени от момента разрешения воспаления. В условиях хронического панкреатита мутации KRAS могут сформироваться на ранней стадии заболевания, дабы ограничить распространение воспалительного процесса, повреждающего ткани. Это предполагает наличие выраженного давления эволюционного отбора в пользу мутантных клеток и служит возможным объяснением практически повсеместного присутствия клеток с мутантным геном KRAS при раке поджелудочной железы.
Уточнение связи между воспалением и канцерогенезом
Уже давно воспаление связывают с развитием нескольких злокачественных новообразований, однако явные причинно-следственные связи еще не удалось раскрыть. Группа исследователей во главе с Эдоардо Дель Поггетто, Ph.D., докторантом, и И-Линь Хо, аспирантом лаборатории Виале, задалась целью изучить влияние панкреатита (известно, что воспалительные процессы при этом патологическом состоянии связаны с более высоким риском развития рака поджелудочной железы) на эпителиальные клетки поджелудочной железы.
Исследователи стимулировали преходящее воспаление в модели индуцибельного посредством KRAS рака поджелудочной железы. Воспаление приводило к немедленным патологическим изменениям в клетках поджелудочной железы, но они разрешались в течение одной недели. Однако активация KRAS даже спустя несколько месяцев после исчезновения воспаления привела к ускоренному образованию опухоли по сравнению с контрольной моделью. Это позволило предположить, что воспаление стимулирует долгосрочные изменения в эпителиальных клетках, при которых происходит в том числе взаимодействие с мутантным KRAS, что способствует развитию рака.
В ходе глубокого молекулярно-биологического исследования эпителиальных клеток после эпизода воспаления обнаружились признаки значительного перепрограммирования экспрессии генов и эпигенетической регуляции, которые сохранялись в течение длительного времени после восстановления поврежденных тканей. Данный процесс исследователи назвали «эпителиальной памятью». Такое внутриклеточное перепрограммирование приводило к активации путей, связанных с выживанием, пролиферацией и эмбриональным развитием линий клеток, что было аналогично путям, активным во время канцерогенеза.
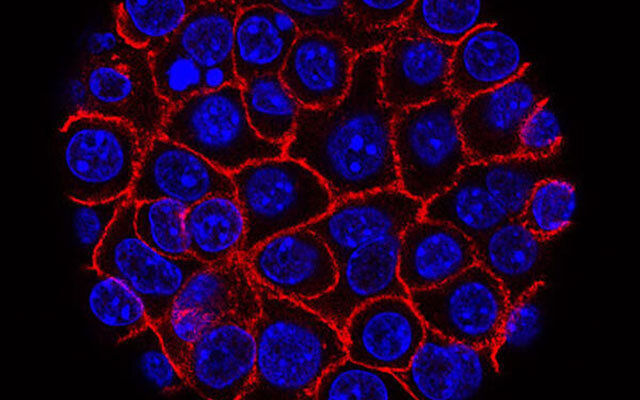
Раковые клетки поджелудочной железы (окрашены синим), заключенные в соединительнотканные мембраны (окрашены в красный цвет) и развивающиеся внутри них.
Благодаря эпителиальной памяти формируется быстрая реакция, ограничивающая повреждение тканей при рецидивирующем панкреатите
Вследствие воспаления стимулируется перепрограммирование клеток, что также облегчает развитие ацинарно-протоковой метаплазии (АПМ) — обратимого процесса, при котором ацинарные клетки поджелудочной железы приобретают черты протоковых клеток. Ацинарные клетки синтезируют и секретируют пищеварительные ферменты, а протоковые клетки доставляют эти ферменты в тонкий кишечник. Считается, что АПМ — процесс, который обычно развивается в ответ на повреждение тканей поджелудочной железы, — является для нее предраковым.
С позиции эпителиальной памяти как явления, рекуррентные эпизоды воспаления приводят к быстрому и повсеместному развитию АПМ с минимальными признаками клеточного повреждения. Следовательно, можно предположить, что внутриклеточное перепрограммирование служит для защиты поджелудочной железы от накопления клеточных и тканевых повреждений. Согласно этому, AПM является скорее не предраковым состоянием, а адаптационной реакцией на воспаление.
Согласно результатам предыдущих исследований, мутации гена KRAS могут индуцировать и стабилизировать состояние АПМ. Здесь авторы продемонстрировали, что активация мутантного гена KRAS во время эпизодов рекуррентного воспаления приводит к более выраженной АПМ и почти полному отсутствию повреждения тканей. Таким образом, авторы предполагают, что клетки, подвергшиеся воспалению, будут подвержены более выраженному положительному отбору в отношении мутаций гена KRAS или других внутриклеточных изменений, которые стимулируют AПM и ограничивают накопление тканевых повреждений.
По словам Хо, в данный момент ученые работают над тем, чтобы лучше понять, каким образом клеткам удается поддерживать эпителиальную память. Однако, согласно полученным выводам, ген KRAS изначально играет эволюционно полезную роль при панкреатите. Автор продолжает, что подобное явление может происходить и в случае с другими типами рака, и с универсальными движущими мутациями, когда существует сильное давление отбора этих мутаций для некоей эволюционной цели, не связанной с канцерогенезом.
В настоящее время группа исследователей занята разработкой стратегии стимуляции АПМ в тканях поджелудочной железы с одновременным противодействием давлению отбора в пользу мутантного гена KRAS. Если работа принесет явные положительные результаты, ее можно будет использовать в качестве теоретической базы для новых методов лечения хронического панкреатита, которые в свою очередь также смогут предотвращать развитие рака поджелудочной железы.
