Истинные возможности дофамина позволят пересмотреть методы лечения психических заболеваний и зависимостей

Согласно передовым исследованиям, уровень дофамина повышается в ответ не только на «приятные», но и на стрессорные стимулы, что служит поводом пересмотреть факты об этом гормоне «хорошего самочувствия» и важнейшем посреднике при развитии многих психических заболеваний. Это открытие предлагает переосмыслить методы лечения психических расстройств и зависимостей.
Исследование возглавили Эрин Калипари и Коди Сицилиано — доценты фармакологии, а также Мунир Гунес Кутлу — научный сотрудник лаборатории Калипари.
По словам Калипари, который также является преподавателем Вандербильтского исследовательского института головного мозга и Центра исследований наркозависимости, в популярной литературе дофамин часто называют «молекулой удовольствия» или «молекулой поощрения». В научном сообществе исследование помогло понять, что роль дофамина в процессах обучения и запоминания оказалась более сложной, чем было принято считать, ведь не существовало полноценной и точной теории, которая могла бы объяснить спектр функций дофамина в головном мозге.
Доминирующая модель, называемая теорией ошибки предсказания вознаграждения (ОПВ), основывается на предположении, что дофамин сигнализирует о скором получении поощрения. Согласно этой теории, выделение дофамина следует за каждой совершенной ошибкой в попытке добиться поощрения. Авторы показывают, что теория ОПВ подтверждается только в ограниченном количестве сценариев процесса обучения. Как заявляет Калипари, это доказывает, что хотя получение поощрения приводит к еще большему выбросу дофамина, также увеличивается и количество стрессовых стимулов. Далее авторы демонстрируют, что дофамин вовсе не является молекулой поощрения. Вместо этого он способствует кодированию информации обо всех важных и значимых событиях, а также управлению адаптивным поведением — независимо от того, будет ли оно положительным или отрицательным.
Чтобы применить передовые технологии для изучения удивительного разнообразия нейро-поведенческих процессов, связанных с выделением дофамина, исследователи обратились к Лин Тяню, профессору и заместителю заведующего кафедрой биохимии и молекулярной медицины Калифорнийского университета в Дэвисе. Для анализа данных авторы использовали машинное обучение и компьютерное моделирование, а также применяли оптико-генетические методы, в которых световая энергия служит для управления активностью генетически модифицированных нейронов.
В ходе анализа была создана новая компьютерная модель поведения, которая позволяет «точно прогнозировать поведенческие эффекты, вызванные выделением дофамина». Калипари заключает, что это исследование меняет текущие представления относительно роли дофамина в центральной нервной системе. Авторы предлагают четко сформулированную и экспериментально подтвержденную теорию и призывают к пересмотру соответствующих фактов в учебниках.
По словам Дэнни Уиндера, директора Вандербтльтского центра исследований зависимостей, общая черта всех наркотических веществ — усиление выделения дофамина в мозге, что способствовало закреплению за дофамином представления как о молекуле вознаграждения. Настоящее исследование четко демонстрирует гораздо более сложную роль этого нейромедиатора, и это означает, что модели зависимости, в основе которых лежит теория «вознаграждения» дофамином / наркотическим веществом, требуют пересмотра.
Калипари подчеркивает, что эти данные побуждают переписать сведения о функции дофамина, включая данные о том, что он кодирует в мозге и как управляет поведением. Это невероятно важно, утверждает она, поскольку при болезни Паркинсона и почти при любом психиатрическом заболевании — наркомании, тревожном расстройстве, депрессии, шизофрении и др. — присутствуют нарушения дофаминовой системы. Знание о том, что означает этот дефицит дофамина, будет иметь решающее значение для понимания симптоматики у пациентов и разработки более эффективных методов лечения этих заболеваний, основанных на фактических данных.
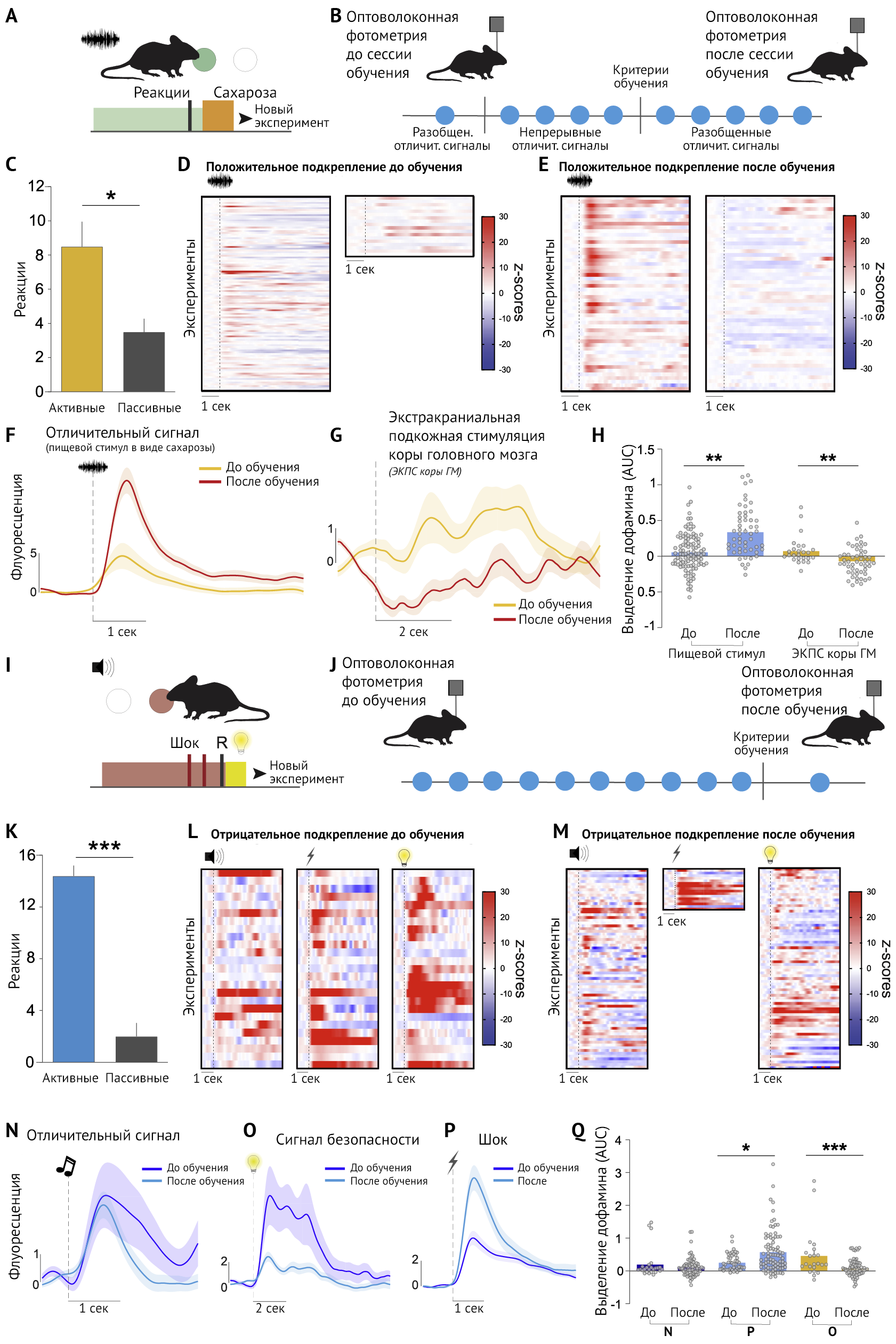
(B) Выделение дофамина регистрировалось с помощью волоконной фотометрии с использованием устройства dLight1.1.
(C) У мышей отмечались более активные реакции на раздражители в эксперименте, проведенном после сессии обучения (т. н. тренировки) (t6 = 3,18, p = 0,024; n = 6).
(D и E) Тепловые карты, демонстрирующие выделение дофамина, согласованное с отличительным сигналом пищевого раздражителя сахарозой (слева) и экстракраниальной подкожной стимуляцией коры головного мозга (справа) в периоды до сессии обучения (D) и после нее (E). Каждая строка схемы представляет собой отдельную запись отличительного сигнала в виде сахарозы или экстракраниальной подкожной стимуляции коры головного мозга.
(F и G) Кривые усредненных значений, демонстрирующие реакции на пищевой стимул в виде сахарозы (F) и экстракраниальной подкожной стимуляции коры головного мозга (G) до и после сессии обучения.
(H) Выделение дофамина увеличилось после получения сахарозы (F1 153 = 10,79, p = 0,0013) и снизилось после экстракраниальной подкожной стимуляции коры головного мозга (F1,75 = 11,17, p = 0,0013) за время обучения животного.
(I) Эксперимент с отрицательным подкреплением.
(J) Модель записи оптоволоконной фотометрии.
(K) Поведенческие показатели в момент отрицательного подкрепления после сессии обучения (t4 = 9,35, p < 0,001; n = 5).
(L и M) Тепловые карты выделения дофамина в соответствии с отличительным стимулом в виде шока (слева), раздражения конечности (в центре) и сигнала о безопасности (справа) в моменты до (L) и после (M) сессии обучения животного.
(N–P) Следы выделения дофамина до шока (N), сигнала безопасности (O) и раздражения конечности (P) до и после сессии обучения.
(Q) Дофаминовая реакция на отличительный сигнал в виде шока (F1,96 = 1,52, p = 0,220), раздражение конечности (F1,127 = 4,00, p = 0,047) и сигналы безопасности (F1,95 = 15,46, p = 0,0002). Планки погрешностей представляют ± S.E.M. ∗ p < 0,05, ∗∗ p < 0,01, ∗∗∗ p < 0,001.
Будущее проекта
По словам Калипари, авторы планируют исследовать, как предложенная ими концепция вписывается в понимание патогенеза наркомании и как наркотики изменяют дофаминовый сигнальный путь, приводя к нарушению поведения. Понимание нейробиологии наркомании преимущественно сосредоточено на дофамине и дофаминергической системе, и, соответственно, именно на него направлены многие фармакологические методы лечения наркомании. Однако воздействие на дофаминовую систему без полного понимания функций этого нейромедиатора может привести ко многим непредвиденным побочным эффектам и, что более важно, неудачам при лечении. Полученные новые сведения о функциях дофамина затронут многие сферы помимо нейробиологии, что, безусловно, будет иметь сильное влияние на жизни людей и эффективность лечения.
Статья авторов под названием "Dopamine release in the nucleus accumbens core signals perceived saliency" была опубликована в открытом доступе в журнале "Current Biology". Полный текст вы можете прочитать по ссылке.
