CAR-T-клеточная терапия: персонализированная атака на рак
1.Введение
В 2025 году Nature Medicine [1] опубликовал уникальное клиническое наблюдение: пациентка с нейробластомой, получившая CAR-T-клеточную терапию более 18 лет назад, продолжает находиться в полной ремиссии и за это время родила двоих детей. Это самый продолжительный зарегистрированный эффект после данной терапии. Этот случай служит не только иллюстрацией эффективности метода, но и символом того, как фундаментальные иммунологические открытия середины XX века легли в основу одной из самых передовых технологий современной онкологии.
Термин адоптивный (от лат. adoptare – “принимать”, “усыновлять”, прим. ред.) перенос был предложен в 1956 году Питером Медаваром, Лесли Биллингемом и Руфусом Брентом в контексте изучения иммунологического отторжения трансплантатов [2,3]. Эти исследования стали краеугольным камнем для будущей трансплантационной иммунологии и доказали, что иммунная система способна «обучаться» и формировать устойчивую память против чужеродных антигенов.
В 1960-х годах британский иммунолог Джеймс Митчисон и его коллеги впервые экспериментально продемонстрировали возможность направленного подавления опухолевого роста путём переноса лимфоцитов от иммунизированных доноров – задолго до того, как концепция «противоопухолевого иммунитета» стала общепринятой [4]. Эти ранние эксперименты показали, что Т-клетки обладают потенциалом распознавать и уничтожать опухолевые клетки, если они снабжены необходимой специфичностью.
В последующие десятилетия происходил постепенный переход от фундаментальных моделей к терапевтическим стратегиям. Первоначально попытки использовать Т-клетки включали экспансию опухоль-инфильтрирующих лимфоцитов и лимфоцитов, специфичных к вирусам, у пациентов с ВЭБ-ассоциированными лимфомами, однако широкому клиническому применению препятствовали низкая эффективность и технологические ограничения.
Принципиальный сдвиг произошёл в 1989 году, когда Зелик Эшар сконструировал первый гибридный рецептор, объединив антиген-связывающие домены антител с сигнальными элементами Т-клеточного рецептора [5]. Так была заложена основа технологии химерных антигенных рецепторов (chimeric antigen receptor – CAR), которая объединила адаптивность Т-клеток со специфичностью антител. Несмотря на техническую реализуемость, первые десятилетия развития CAR-Т сопровождались ограниченным клиническим успехом, главным образом из-за слабой выживаемости и нестабильности модифицированных клеток.
Только на рубеже 2010-х с внедрением методов ко-стимуляции, вирусной трансдукции и стандартизации клеточного производства, CAR-T-клеточная терапия впервые продемонстрировала впечатляющие результаты у пациентов с рефрактерными формами острого лимфобластного лейкоза и B-крупноклеточной лимфомы. Эти успехи привели к стремительному росту интереса к технологии, кульминацией которого стало одобрение первого CAR-T-клеточного препарата tisagenlecleucel (tisa-cel, “Kymriah”) FDA в 2017 году.
С тех пор CAR-T-клеточная терапия прошла путь от экспериментального подхода к инструменту лечения агрессивных онкогематологических заболеваний. Вместе с тем она остается высокотехнологичным, дорогостоящим и не лишенным рисков методом, требующим глубокого понимания иммунобиологии, молекулярной инженерии и клинической логистики.
2. Строение и поколения CAR-T-клеток
CAR — это сконструированные молекулы, которые распознают специфические белки на поверхности опухолевых клеток. Клетки с CAR представляют собой модифицированные Т-лимфоциты пациента или донора, что позволяет им избирательно атаковать опухолевые клетки [7].
Классическая структура CAR включает четыре ключевых элемента [8]:
- Антигенсвязывающий внеклеточный домен — одноцепочечный вариабельный фрагмент (scFv), полученный из антител, распознающих специфические поверхностные антигены опухоли. Конфигурация взаимодействия между VH и VL, а также длина линкера между ними критически важны для аффинности и специфичности распознавания [9].
- Шарнирная (спейсерная) область, обеспечивающая гибкость рецептора и оптимальное расстояние для взаимодействия с мишенью. Длина и состав этой области могут значительно влиять на эффективность и селективность CAR T-клеточной терапии, особенно при нацеливании на антигены, экспрессируемые с различной плотностью [10].
- Трансмембранный домен, якорящий рецептор в мембране Т-клетки и участвующий в передаче сигнала. Обычно используется трансмембранная часть молекул CD3ζ, CD8α или CD28. Выбор трансмембранного домена влияет на стабильность экспрессии и формирование иммунологического синапса [8].
- Внутриклеточный сигнальный домен, содержащий цепь CD3ζ и один или два ко-стимулирующих домена, ответственных за активацию Т-клетки. Комбинации CD28, 4-1BB, ICOS и OX40 модулируют различную степень цитокиновой продукции, персистенции и фенотипа эффекторных клеток [11–14].
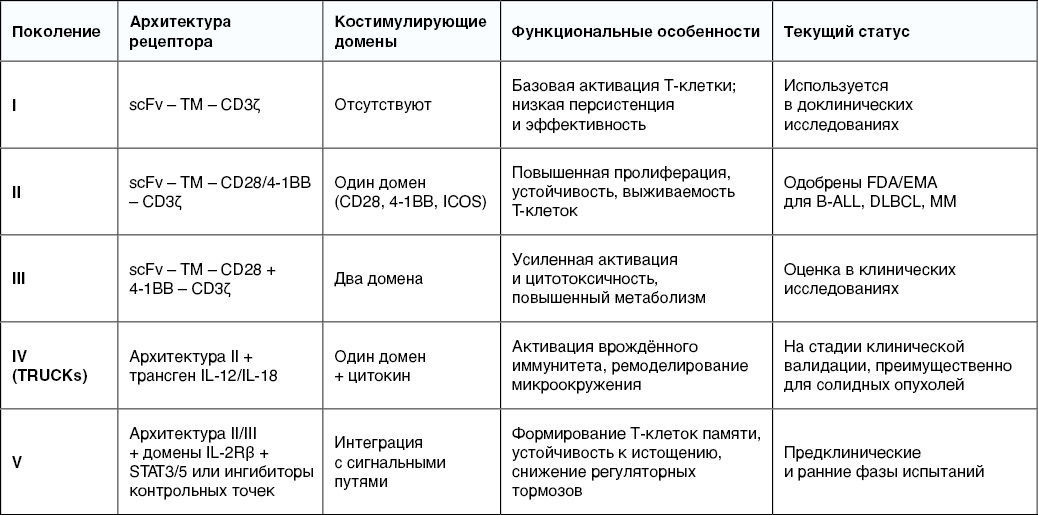
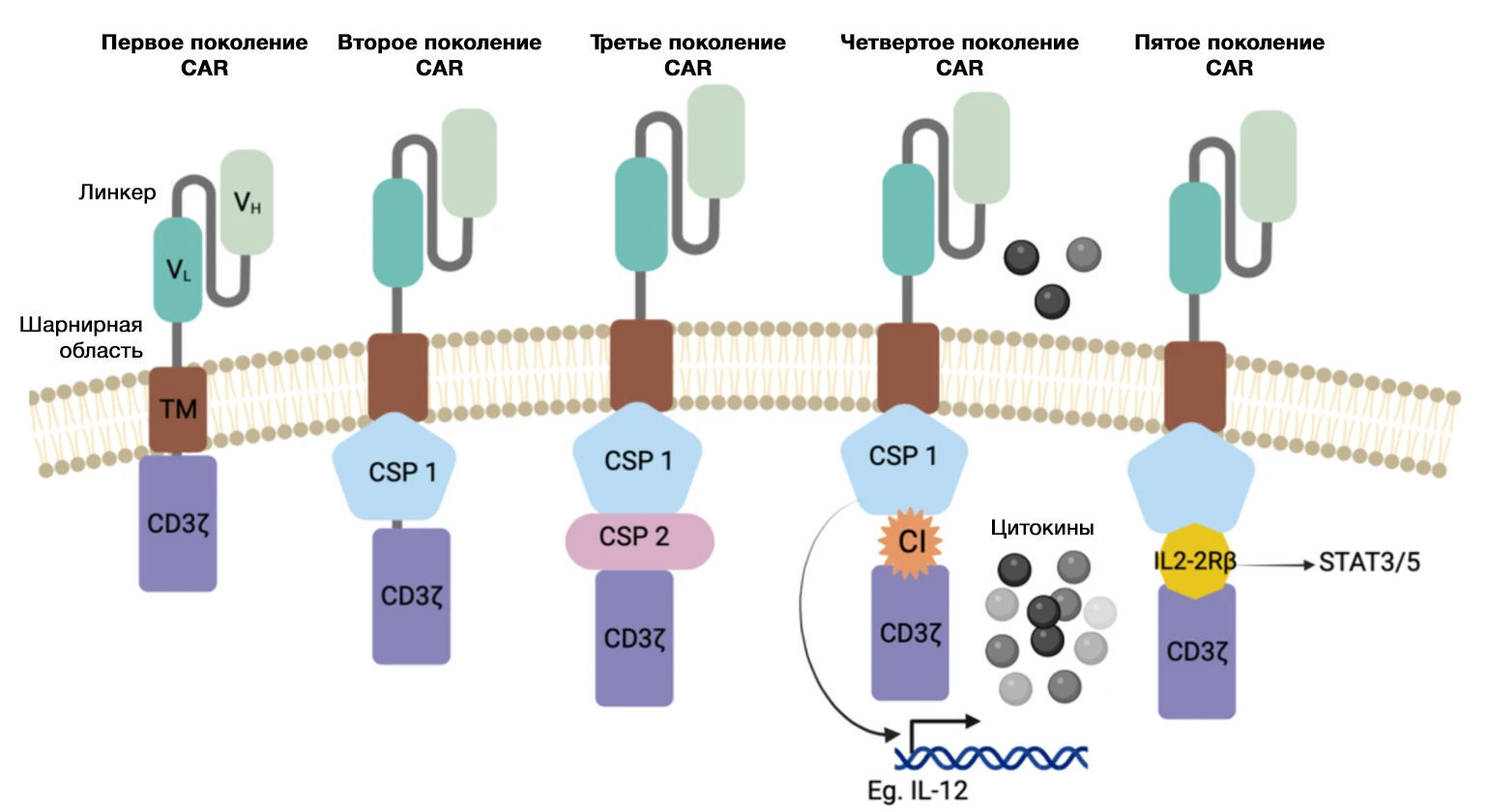
Помимо этого, можно проследить развитие CAR-T-клеток по следующим поколениям (рис.1, табл.1):
- Первое поколение содержало только CD3ζ-домен. Такие рецепторы активировали Т-клетки, но не обеспечивали стойкой пролиферации и персистенции. Клинический эффект был кратковременным и непредсказуемым [15].
- Второе поколение включало один ко-стимулирующий домен (наиболее часто CD28 или 4-1BB), что обеспечивало более сильную и продолжительную активацию, повышенную выживаемость и функциональность Т-клеток. Эти конструкции составляют основу большинства одобренных на сегодняшний день препаратов [16].
- Третье поколение содержит уже два ко-стимулирующих домена, часто сочетающих CD28 и 4-1BB. Это позволило усилить сигналинг и потенциально повысить противоопухолевую активность, хотя клинические преимущества по сравнению со вторым поколением пока обсуждаются. Некоторые исследования указывают на увеличение риска токсичности при использовании двойной ко-стимуляции [17,18].
- Четвёртое поколение (T-cells Redirected for Universal Cytokine Killing — TRUCKs) строится на основе второго, но дополнительно включает трансгены, кодирующие провоспалительные цитокины, такие как IL-12, IL-15 или IL-18. Эти клетки способны модифицировать опухолевое микроокружение, активируя врождённый иммунитет и снижая иммунную супрессию. Отдельные модификации включают доминирующие негативные рецепторы к TGF-β или секретируемые ингибиторы иммунных чекпойнтов [19].
- Пятое поколение — это более сложные конструкции, включающие внутриклеточные мотивы сигнальных путей цитокиновых рецепторов (например, IL-2Rβ) и активаторы транскрипции (STAT3/5) [19]. Некоторые варианты также содержат элементы для ингибирования чекпойнт-сигналов (PD-1, CTLA-4), повышая устойчивость к истощению.
Таблица 1. Поколения CAR-T-клеток.
Кроме того, современные подходы к дизайну CAR учитывают возможность создания так называемых универсальных CAR, в которых антигенраспознающий модуль отсоединён от сигнального комплекса и может быть направлен на разные мишени с помощью адаптеров (например, платформы SUPRA CAR и UniCAR) [20]. Это позволяет гибко настраивать терапию, снижая риск токсичности и увеличивая контроль над действием CAR-T-клеток.
Помимо состава сигнальных доменов, на эффективность CAR-Т-клеточной терапии влияет конфигурация внеклеточной части. Изменения длины и гибкости спейсерной области, а также выбор трансмембранного домена (CD8α, CD28, CD3ζ) могут значительно повлиять на уровень экспрессии, устойчивость и силу сигнала [10]. Более того, структурные детали scFv, такие как относительная ориентация вариабельных цепей VH и VL, а также длина линкера между ними, напрямую влияют на аффинность, специфичность и кинетику связывания антигена [9]. Даже небольшие изменения в конформации могут кардинально повлиять на функциональные характеристики рецептора и его поведение in vivo.
Современные исследования также указывают на важность выбора изотипа и гликозилирования CAR, что может влиять на внутриклеточный трафик и деградацию рецептора, а следовательно — на его стабильность и длительность действия. Применение гуманизированных или полностью человеческих scFv снижает риск иммуногенности и истощения CAR-T-клеток [21]. Наконец, современные платформы позволяют разрабатывать универсальные CAR с настраиваемыми лиганд-связывающими доменами, модулями «включения/выключения», логическими схемами (например, AND/OR/NOT), индуцируемыми сигнальными каскадами и даже способностью к саморегуляции экспрессии [7].
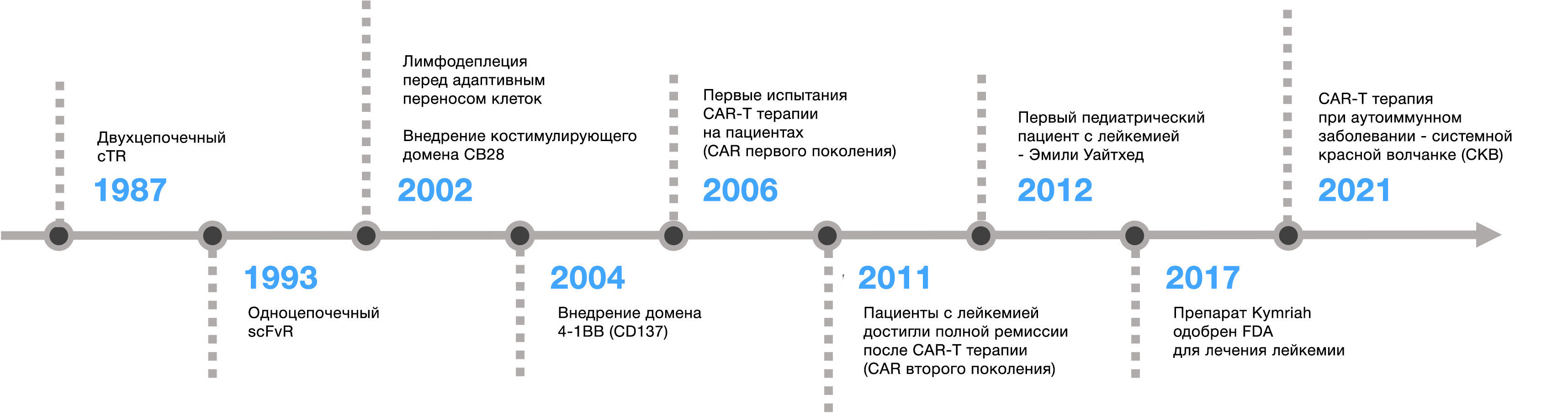
Рисунок 2. Таймлайн развития СAR-T-клеточной терапии. Адаптировано из Mitra A. et al. From bench to bedside: the history and progress of CAR T cell therapy // Frontiers in Immunology. 2023. Vol. 14.[22].
3.Производство CAR-T-клеток
Процесс получения CAR-T-клеток представляет собой многоэтапную высокотехнологичную процедуру, включающую выделение, модификацию, экспансию и введение генетически изменённых Т-лимфоцитов, способных к специфическому распознаванию опухолевых антигенов и реализации эффекторной функции in vivo.
3.1 Сбор и изоляция Т-клеток
Процедура начинается с лейкафереза — выделения мононуклеарных клеток из периферической крови пациента. Продукты лейкафереза содержат гетерогенную смесь клеток, включая Т-лимфоциты, NK-клетки, дендритные и миелоидные клетки (моноциты, нейтрофилы), а также элементы опухолевого происхождения [23].
Даже при применении методов положительного или отрицательного отбора (например, селекция CD3+ клеток) возможно остаточное загрязнение клеточной популяции иммуносупрессивными компонентами, особенно CD14+ моноцитами [24]. Исследования указывают на корреляцию между их содержанием и пониженной эффективностью ex-vivo экспансии, снижением уровня трансдукции и ослаблением эффекторного потенциала CAR-T-клеток [25].
3.2 Генетическая модификация
После изоляции Т-клетки подвергаются активации и трансдукции генетическим материалом, кодирующим CAR.
Наиболее широко используются:
- Лентивирусные векторы третьего поколения (самоинактивирующиеся, SIN) — обеспечивают стабильную экспрессию с минимальным риском инсерционного мутагенеза благодаря удалению энхансеров из LTR [26];
- Гаммаретровирусы — применялись в ранних клинических испытаниях, но обладают более высокой вероятностью активации онкогенов в стволовых клетках [27].
Несмотря на общую безопасность, описаны случаи клональной экспансии CAR-T-клеток в связи с нарушением экспрессии гена Tet2 при лентивирусной интеграции [28].
Перспективным направлением является таргетированная интеграция трансгена в безопасные локусы генома, такие как AAVS1, CCR5 или TRAC, с использованием CRISPR/Cas9, TALEN или редактирования на основе интегразонезависимых платформ.
3.3 Экспансия
После трансдукции клетки культивируются в течение 7–14 суток в присутствии цитокинов: IL-2, IL-7, IL-15 или IL-21. Целью этого этапа является достижение необходимой численности, сохранение функциональности и предпочтительного фенотипа (часто CD45RO−CCR7+ TCM или TSCM) [24]. Платформы, такие как CliniMACS Prodigy и FasTCAR, позволяют автоматизировать экспансию и сократить производственный цикл до 1–3 дней [29].
3.4 Криоконсервация и логистика
Готовый препарат криоконсервируют с применением контролируемого замораживания и хранят в жидком азоте до момента доставки в клинику. Перед инфузией пациенту проводят лимфодеплеционную химиотерапию (обычно флударабин + циклофосфамид), которая снижает конкуренцию со стороны эндогенных лимфоцитов, создаёт пространство для экспансии CAR-T-клеток и повышает уровень циркулирующих цитокинов (например, IL-15) [30].
3.5 Инфузия и клиническое наблюдение
CAR-T-клетки вводятся внутривенно. В течение 4–10 дней наблюдается их экспансия, миграция в опухолевые ниши и реализация цитотоксического эффекта. На этом этапе наиболее часто встречаются следующие побочные эффекты:
- Синдром высвобождения цитокинов (СВЦ): уровень тяжести коррелирует с опухолевой нагрузкой и скоростью пролиферации введенных клеток;
- Синдром нейротоксичности, ассоциированный с иммунными эффекторными клетками (ICANS): проявляется энцефалопатией, афазией, судорогами, отёком мозга.
Контроль их проявлений включает отслеживание температуры, сатурации, давления, биомаркеров воспаления (IL-6, С-реактивный белок, D-димер, ферритин), оценку по шкале ICE (Immune Effector Cell Encephalopathy) [31,32]. При развитии осложнений применяют тоцилизумаб (анти-IL-6R), анакинру (анти-IL-1R) и ГКС [33].
3.6 Долгосрочный мониторинг
В соответствии с рекомендациями FDA наблюдение за пациентами после CAR-T клеточной терапии должно составлять минимум 15 лет [34]. Целями наблюдения за такими пациентами являются: выявление поздних токсичностей (вторичные неоплазии, пролиферация клонов), контроль длительности ремиссии (через МОБ – минимальная остаточная болезнь, ПЭТ-КТ), оценка персистенции CAR-T (через кПЦР, проточную цитометрию, scRNA-seq) [35,36].
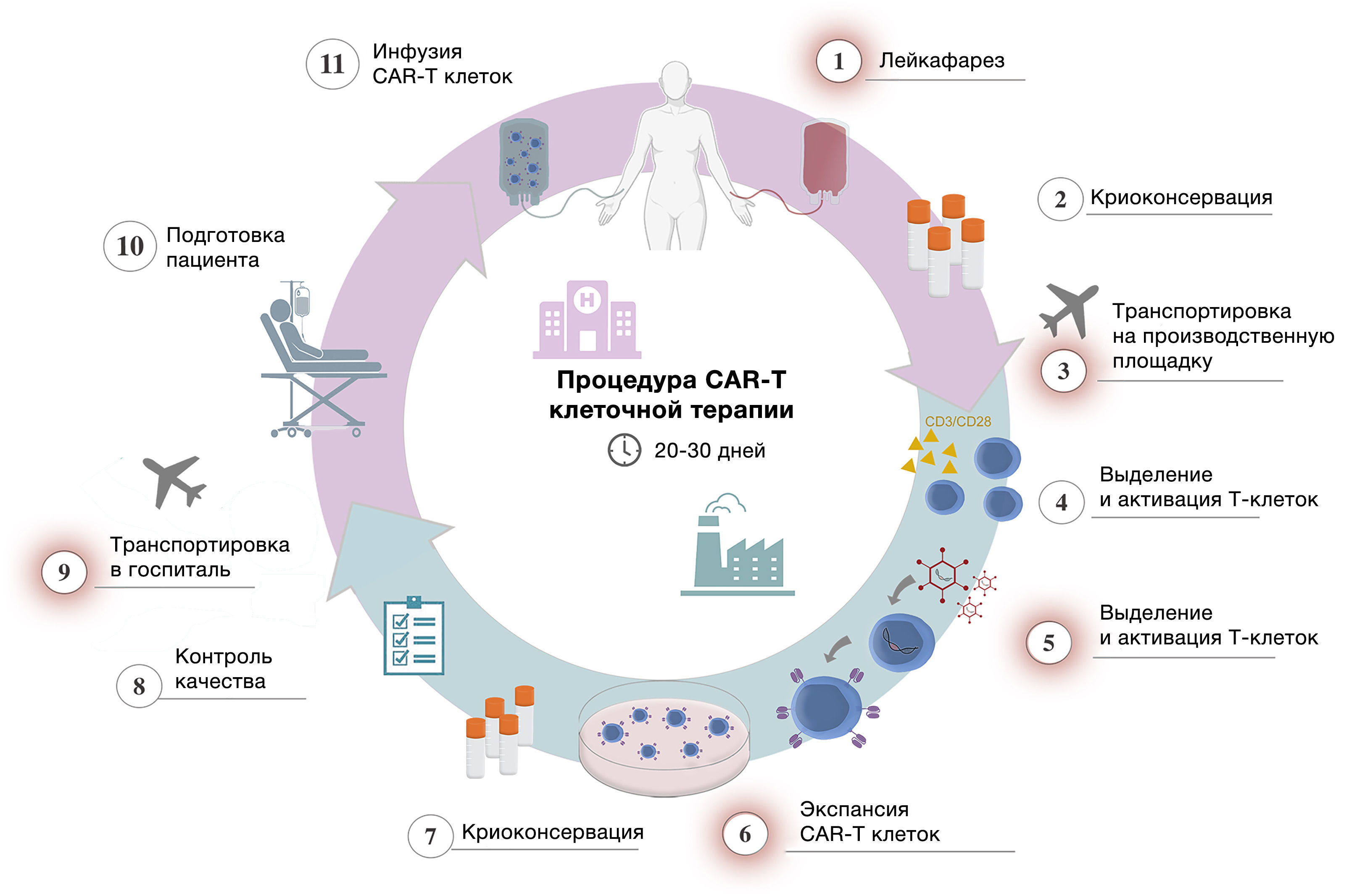
Рисунок 3. Цикл производства CAR-T. Адаптировано из Abdo L., Batista-Silva L.R., Bonamino M.H. Cost-effective strategies for CAR-T cell therapy manufacturing // Molecular Therapy Oncology. 2025. Vol. 33, № 2. P. 200980. [37].
4. Прогнозирование ответа на CAR-T клеточную терапию
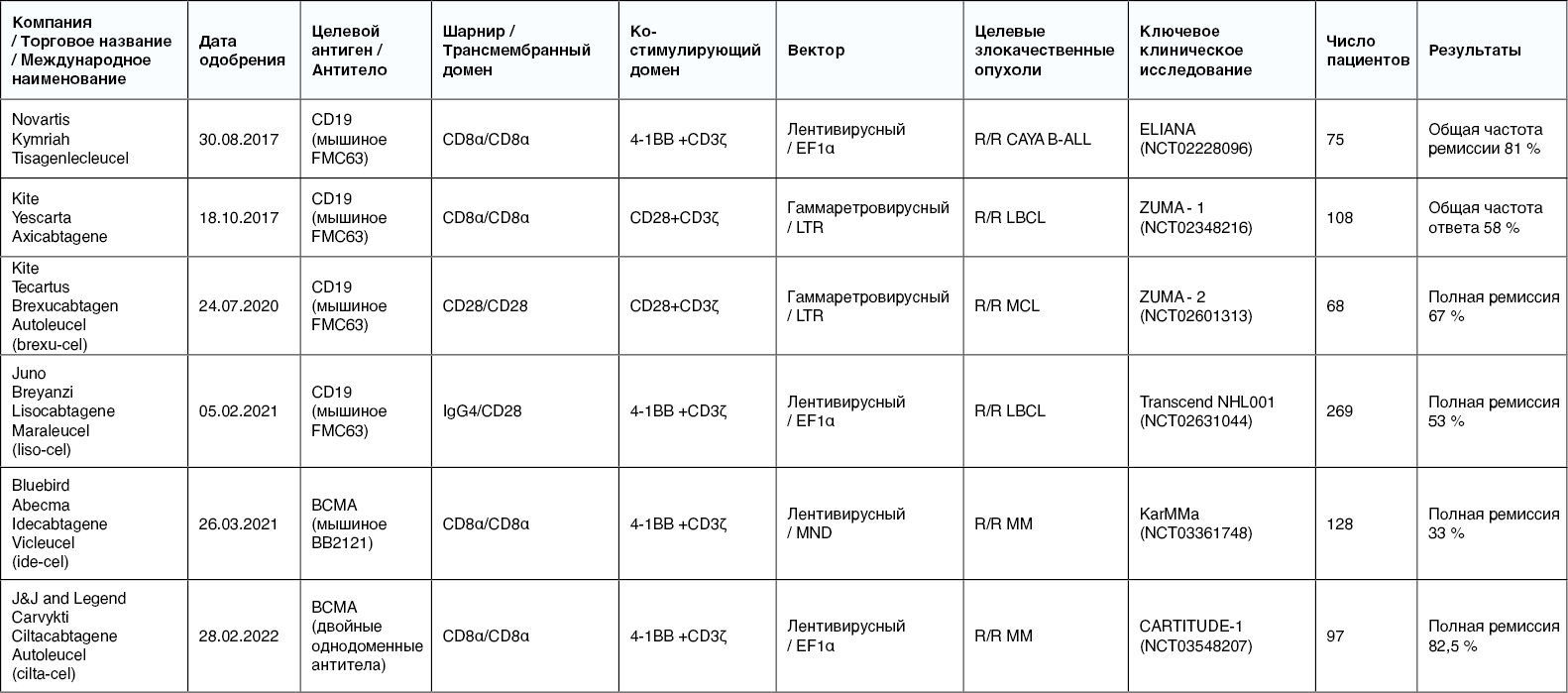
CAR-T-клеточная терапия одобрена во многих странах для лечения рецидивирующих и рефрактерных (R/R) гематологических злокачественных опухолей. По состоянию на 2024 год, девять препаратов прошли регистрацию и получили разрешение на клиническое применение в США, ЕС, Китае и других странах [38]. Большинство из них нацелены на антиген CD19, используемый при В-клеточных лимфомах и острых лимфобластных лейкозах, и BCMA (B-cell maturation antigen). CD19 — это специфичный маркёр плазматических клеток, применяемый для терапии множественной миеломы (табл.2) [39].
Таблица 2. Одобренные препараты для CAR-T-клеточной терапии [22].
5.Заболевания, для которых применяются препараты CAR-T-терапии
5.1 Диффузная В-крупноклеточная лимфома
Диффузная В-крупноклеточная лимфома (ДВКЛ) — наиболее распространённая агрессивная неходжкинская лимфома. Первая линия терапии включает схему R-CHOP (ритуксимаб, циклофосфамид, гидроксидаунорубицин, винкристин, преднизон), обеспечивающую ремиссию у 70–80 % пациентов. Однако у 30–40 % развивается рецидив или рефрактерность, при этом 2-летняя общая выживаемость (OS) составляет всего 20–40 % [46]. В этой когорте CAR-T-клеточная терапия показала выдающуюся клиническую эффективность. Исследование ZUMA-1 (NCT02348216) продемонстрировало, что axicabtagene ciloleucel (axi-cel) обеспечивает общую частоту ответа на терапию (overall response rate, ORR) в 83 %, полный ответ (complete response, CR) в 53 %, медиану общей выживаемости (overall survival, OS) 25,8 месяцев и 5-летнюю выживаемость 42,6 % [41]. ZUMA-7 (NCT03391466) сравнивало axi-cel со стандартом лечения во 2-й линии: медиана выживаемости без событий (event-free survival, EFS, под событиями имеется в виду прогрессия, рецидив, смерть — прим. ред.) — 8,3 против 2,0 месяцев, CR — 65 % против 32 % соответственно [47]. Tisa-cel, согласно данным исследования JULIET (NCT02445248), демонстрировал ORR 52 %, CR 40 % у пациентов с R/R ДВКЛ после ≥2 линий терапии [48]. Liso-cel, в рамках TRANSCEND NHL 001 (NCT02631044), обеспечил ORR 73 %, CR 53 %, медиану выживаемости без прогрессирования (progression-free survival, PFS) 6,8 мес [49]. Эти данные подтверждают высокую клиническую эффективность трёх CD19-CAR-T продуктов при ДВКЛ, с разными профилями токсичности и экспансии in vivo.
5.2 Острый лимфобластный лейкоз
Острый лимфобластный лейкоз (ОЛЛ) характеризуется высокой излечимостью у детей (5-летняя OS >90 %), однако у взрослых выживаемость составляет лишь 35–45 %, в основном из-за химиорезистентности. У пациентов с R/R ОЛЛ долгосрочная выживаемость снижается до 15–50 % [50]. Первым одобренным препаратом для терапии R/R ОЛЛ стал tisa-cel, одобренный FDA в 2017 году для лечения пациентов в возрасте до 25 лет. В ключевом исследовании ELIANA (NCT02435849), которое включало детей и молодых взрослых, ORR составил 81 %, CR — 60 %, 6-месячная OS — 90 % [51]. При медиане наблюдения 13,1 месяца, 1-летняя OS достигала 76 %. Другие платформы, включая brexu-cel (brexucabtagene autoleucel), также демонстрируют эффективность у взрослых пациентов. В исследовании ZUMA-3 (NCT02614066) brexu-cel достиг ORR 70,9 % и CR/CRi 56,4 %, с медианой OS 18,2 месяца [52]. В качестве альтернативной мишени может использоваться CD22, который экспрессируется у 90 % пациентов с ОЛЛ и используется для создания CAR-конструкций при рецидивах после анти-CD19 терапии. В исследовании фазы I CD22 CAR-T-клетки показали дозозависимый ответ с CR 73 % у пациентов, получивших ≥1×10⁶ CAR+ T-клеток/кг [53]. В более крупном исследовании [54] применение анти-CD22 CAR-T клеток сопровождалось CRS у 86,2 % пациентов (преимущественно 1–2 степени), нейротоксичностью у 11 % и ORR 70 %. Медиана OS составила 13,4 месяца. Это подтверждает клиническую применимость CD22 CAR-T как “спасительного” подхода после CD19-направленной терапии.
5.3 Множественная миелома
Множественная миелома остаётся в значительной степени неизлечимым заболеванием, характеризующимся последовательными рецидивами и укорачивающимися интервалами ремиссии. Применение CAR-T-клеточной терапии, особенно направленной против BCMA, стало важным прорывом для пациентов с рефрактерной миеломой. BCMA преимущественно экспрессируется на зрелых плазматических клетках и отсутствует на гемопоэтических стволовых клетках, что делает его высокоспецифичной терапевтической мишенью.
FDA одобрило два препарата: ide-cel (idecabtagene vicleucel) в 2021 году и cilta-cel (ciltacabtagene autoleucel) в 2022 году. В Китае в 2023 году был зарегистрирован CT103A, основанный на гуманизированном scFv. В исследовании KarMMa (NCT03361748) ide-cel показал ORR 73 %, CR 33 %, медиану PFS 8,8 мес [44]. В фазе III KarMMa-3 (NCT03651128) ide-cel сравнивался со стандартом лечения у пациентов с ≥2 линиями терапии: медиана PFS составила 13,3 мес против 4,4 мес в контроле, ORR — 71 % против 42 % [55]. В исследовании CARTITUDE-1 (NCT03548207) cilta-cel достиг ORR 97 %, sCR 67 %, а 2-летняя PFS составила около 60 % [45]. Частота CRS — 95 %, но тяжёлые формы возникали только у 9 % пациентов. CARTITUDE-4 (фаза III) подтвердило превосходство cilta-cel над стандартной терапией у пациентов в первой рецидивной линии.
Китайская разработка CT103A (NCT05066646, FUMANBA-1) продемонстрировала ORR 96 %, sCR 74,3 %, включая ремиссии у 9 из 12 пациентов с предшествующей CAR-T терапией [56]. У 4 пациентов sCR сохранялась >18 мес.
Разрабатываются альтернативные мишени для преодоления BCMA-негативных рецидивов: CD138, CD38, CD229, FcRH5, CD56, SLAMF7 (CS1), GPRC5D, TACI, APRIL и др. OriCAR-017 — первый продукт, нацеленный на GPRC5D, в исследовании POLARIS (NCT05016778) дал ORR 100 %, CR 60 % без тяжёлой токсичности.
Испытания двойных CAR, например BM38 (BCMA+CD38), показали ORR 87 %, CR 52 % и медиану PFS 17,2 мес [57]. Исследования SLAMF7-CAR продемонстрировали in vivo эффективность, несмотря на риск фратрицидного эффекта (явление, при котором Т-клетки начинают уничтожать друг друга) при CS1-экспрессии на Т-клетках [58].
Несмотря на значительный прогресс, CAR-T клеточная терапия при множественной миеломе применяется преимущественно на поздних стадиях, остаётся дорогостоящей, требует длительной подготовки и сопровождается рецидивами.
5.4 Мантийноклеточная лимфома
Мантийноклеточная лимфома — это редкая, но агрессивная форма В-клеточной лимфомы, характеризующаяся частыми рецидивами и неблагоприятным прогнозом, особенно у пациентов с рефрактерным течением заболевания. Несмотря на достижения в терапии, включая применение высокодозной химиотерапии и аутологичной трансплантации гемопоэтических стволовых клеток, долгосрочная безрецидивная выживаемость остаётся низкой. Медиана общей выживаемости после рецидива составляет примерно 3 года.
Появление CAR-T-клеточной терапии открыло новые перспективы для пациентов с R/R МКЛ. Препарат brexu-cel стал первым и пока единственным одобренным средством в этой нише. В регистрационном исследовании ZUMA-2 (NCT02601313), которое включило пациентов, ранее получивших ингибиторы BTK (Ибрутиниб, Акалабрутиниб), были достигнуты ORR 91 % и CR 68 %. При медиане наблюдения 35,6 месяцев медиана общей выживаемости не была достигнута, 3-летняя выживаемость составила 47 %, медиана PFS — 25,8 месяцев. Особенно важно, что эффективность сохранялась вне зависимости от исходного статуса TP53 или количества предшествующих линий терапии [42,59].
На ранних этапах разрабатываются и альтернативные подходы. В исследовании TRANSCEND NHL 001 (NCT02631044) использование liso-cel у пациентов с мантийноклеточной лимфомой показало ORR 84 % и CR 59 %, при благоприятном профиле токсичности [43]. Эти данные подчеркивают потенциал использования разных платформ CAR-T клеток и необходимость индивидуализации подхода к выбору продукта в будущем.
Несмотря на высокую эффективность CAR-T клеток, ответ на терапию остаётся вариабельным. У части пациентов достигается длительная ремиссия, тогда как у других наблюдаются истощение клеток, недостаточная экспансия или рецидив заболевания. Ключевым направлением текущих исследований становится разработка биомаркеров, позволяющих прогнозировать эффективность терапии.
Ключевые биомаркеры и подтверждающие исследования:
- CD3+CD8+CD27+CD45RO − T-клетки. Повышенная частота обнаружения этих клеток в инфузионном продукте связана с лучшим клиническим ответом. В исследовании [60] у пациентов с хроническим лимфолейкозом, получавших анти-CD19 CAR-T-клетки, выявлена сильная корреляция между наличием ранних эффекторов памяти и глубиной ответа.
- IL-15. Повышенные уровни интерлейкина-15 до терапии способствуют формированию фенотипа T-клеток памяти со свойствами стволовости (TSCM), что обеспечивает устойчивую экспансию и пролиферацию CAR-T-клеток in vivo [61].
- Гены STAT3/TCF7. Продукты, демонстрирующие высокий уровень экспрессии сигнатур транскриптов STAT3 и TCF7, ассоциированы с персистенцией и высокой цитотоксической активностью CAR-T-клеток [62].
- Полифункциональность T-клеток. Способность CAR-T-клеток одновременно секретировать IFN-γ, TNF-α и IL-2 коррелирует с лучшим контролем заболевания [63].
- Экспансия ex vivo и in vivo. Пролиферация в культуре и скорость расширения после инфузии предсказывают стойкость клинического ответа [64].
- Метаболический профиль. Активность гликолиза и митохондриального метаболизма в CAR-T-клетках коррелирует с их персистенцией. Продемонстрировано, что улучшение митохондриального биогенеза усиливает противоопухолевую активность [65].
- Эпигенетический статус. Эпигенетическая пластичность, в частности уровни ацетилирования H3K27 и метилирования промоторов, влияет на устойчивость экспрессии CAR и устойчивость к истощению [66].
Fraietta et al. [60] продемонстрировали, что предикторами успеха терапии являются не только свойства CAR, но и функциональное качество инфузионного клеточного продукта. Это подтверждается и другими исследованиями, включая данные по хроническому лимфолейкозу и неходжкинской лимфоме, где была показана корреляция между полифункциональностью Т-клеток и длительностью ответа. Учитывая стоимость и возможную токсичность терапии, разработка достоверных прогностических биомаркеров остаётся приоритетом.
6. Преодоление резистентности к CAR-T-клеточной терапии гемопоэтических злокачественных новообразований
Одним из ключевых препятствий к устойчивому клиническому эффекту CAR-T-клеточной терапии, особенно при ОЛЛ, остаётся развитие резистентности опухоли. Наиболее характерным механизмом отказа терапии у детей с В-клеточным ОЛЛ является потеря антигена CD19, несмотря на сохранённую персистенцию CAR-модифицированных Т-клеток. Этот феномен связан с клональным отбором CD19-негативных субпопуляций под действием иммунного давления, создаваемого CAR-T-клетками. Учитывая ключевую роль CD19 в дифференцировке B-клеточной линии, подобное ускользание ранее считалось маловероятным [67].
Первоначально в качестве основного молекулярного механизма был описан альтернативный сплайсинг мРНК CD19, приводящий к образованию либо укороченных немембранных форм (например, Δexon 5-6), либо белков, лишённых эпитопов, распознаваемых CAR-рецепторами (Δexon 2) [68]. Позднее было показано, что иммунное давление со стороны CAR-T может вызывать переход опухоли в другое клеточное направление дифференцировки, особенно при наличии смешанных фенотипов в исходной популяции[69].
Было выявлено, что преобладающим механизмом ускользания у пациентов с рецидивами после CAR-T-терапии являются биаллельные мутации со сдвигом рамки считывания в гене CD19, опровергая ранее доминирующее мнение о ключевой роли только альтернативного сплайсинга [70].
Ещё одним механизмом резистентности является недостаточная экспансия или истощение CAR-T-клеток in vivo. Как показывают исследования, Т-клетки с фенотипом ранней памяти (TSCM и TCM) обладают более высоким потенциалом персистенции и противоопухолевой активности. У пациентов с ОЛЛ, по сравнению с В-клеточной неходжскинской лимфомой, чаще наблюдается более высокая частота наивных и малодифференцированных T-клеток, однако даже в этой группе остаётся значительная гетерогенность [60,71].
В ряде исследований было показано, что плохой ответ на CAR-T-терапию коррелирует с высоким уровнем ингибирующих рецепторов на CD4⁺ и CD8⁺ T-клетках (PD-1, TIM-3, LAG-3), что свидетельствует о предсуществующем T-клеточном истощении в аутологичном клеточном материале [60,72].
Перспективный способ реактивации CAR-T-клеток у пациентов с рецидивом представляет собой блокада контрольных иммунных точек (чекпоинтов). В клинических случаях было показано, что введение ингибиторов PD-1 (например, ниволумаб) после CAR-T приводит к повторной экспансии CAR-клонов и восстановлению противоопухолевого ответа [73]. Однако универсальность этой стратегии требует дальнейшей валидации в рандомизированных исследованиях.
Одним из путей решения проблем, связанных с качеством аутологичных Т-клеток, является разработка универсальных аллогенных CAR-T-клеток, основанных на донорском материале. Такие платформы требуют точного редактирования генома (TALEN, ZFN, CRISPR/Cas9) с выключением рецептора TCR и молекул HLA для предотвращения реакции трансплантат против хозяина [74]. Подобные продукты уже тестируются в клинических испытаниях (например, ALLO-501, UCART19, PBCAR0191).
7. Побочные эффекты CAR-T-клеточной терапии
7.1 Синдром высвобождения цитокинов
Синдром высвобождения цитокинов (СВЦ) представляет собой наиболее частое осложнение CAR-T-клеточной терапии. Он возникает в результате системного воспалительного ответа, индуцируемого массивным высвобождением провоспалительных цитокинов и хемокинов после активации CAR-T-клеток при распознавании опухолевого антигена. По данным мета анализов, СВЦ регистрируется у ~55 % пациентов, получающих CAR-T-клеточную терапию при гематологических злокачественных новообразованиях [75]. Американское общество трансплантации и клеточной терапии (ASPECT) определяет СВЦ как «супрафизиологический ответ после любой иммунотерапии, приводящий к активации или вовлечению инфузионных или эндогенных Т-клеток и/или других иммунных эффекторных клеток». Ключевыми медиаторами в развитии СВЦ считаются интерлейкины IL-6 и IL-1, преимущественно секретируемые моноцитами, макрофагами и дендритными клетками. Недавние исследования показали, что активация гасдермина E (GSDME) в CAR-T-клетках может запускать пироптоз — форму программируемой клеточной гибели, способствующую бурному выбросу перфорина и гранзима B, усиливающих воспалительный каскад [76].
Клинические проявления СВЦ варьируют по тяжести:
- Лёгкие формы: лихорадка, миалгия, головная боль, анорексия, скованность.
- Среднетяжёлые и тяжёлые формы: гипотония, гипоксия, капиллярная утечка, полиорганная недостаточность, ДВС-синдром, шок.
Первые симптомы обычно развиваются через 1–3 дня после инфузии и могут сохраняться в течение 1–3 недель.
ASTCT и NCCN ( American Society for Transplantation and Cellular Therapy и National Comprehensive Cancer Network) разработали стандартизированные критерии оценки тяжести СВЦ (градации от 1 до 4 степени). Поддерживающая терапия варьируется от симптоматического контроля до интенсивной иммуносупрессии. Ключевым принципом лечения СВЦ является баланс между подавлением воспаления и сохранением активности CAR-T-клеток. Идеальным сценарием считается ранняя стратификация риска, основанная на биомаркерах (С-реактивный белок, IL-6, ферритин, d-димер) и параметрах опухолевой нагрузки до инфузии. Перспективным направлением является разработка синтетических CAR-платформ с возможностью временного ингибирования активации, а также внедрение дозоконтролируемых CAR (например, SUPRA-CAR, switch-CAR).
Таким образом, по мере расширения показаний CAR-T-терапии возрастает важность ранней диагностики и эффективного лечения СВЦ. Совершенствование предикторов и создание персонализированных стратегий позволит значительно повысить безопасность и переносимость этого мощного метода иммунотерапии.
7.2 Синдром нейротоксичности, связанный с иммунными эффекторными клетками
Иммуноэффекторная клеточная нейротоксичность (Immune Effector Cell-Associated Neurotoxicity Syndrome, ICANS) является вторым по частоте серьезным осложнением CAR-T-клеточной терапии после СВЦ. По данным метаанализа, ICANS развивается приблизительно у 37 % пациентов, получающих лечение по поводу гематологических злокачественных заболеваний [77]. ASTCT определяет ICANS как «патологическое состояние, вовлекающее центральную нервную систему и возникающее в результате активации инфузионных или эндогенных Т-клеток/иммунных эффекторов после иммунотерапии». ICANS может развиваться параллельно с СВЦ, следом за ним или независимо.
Клинические проявления ICANS:
- Ранние симптомы: экспрессивная афазия, дизграфия, нарушение концентрации.
- Прогрессия: изменённый уровень сознания, спутанность, судорожный синдром, отек головного мозга, кома.
По шкале ICE (Immune Effector Cell-Associated Encephalopathy) оцениваются когнитивные функции, ориентация, речь и моторика. Снижение баллов служит предиктором тяжёлого ICANS.
Потенциальные механизмы развития
Несмотря на активные исследования, точный механизм ICANS остаётся не до конца ясным. Предполагается, что основную роль играет нарушение целостности гематоэнцефалического барьера и инфильтрация ЦНС цитокинами и активированными Т-клетками.
Некоторые данные указывают на возможность on-target/off-tumor (OTOT) эффекта при CD19-направленной терапии — CD19 экспрессируется на периваскулярных клетках в головном мозге, что может способствовать нейротоксичности [78].
Показано, что для минимизации риска тяжёлых исходов критически важны раннее начало терапии, постоянный мониторинг неврологического статуса (ежедневная ICE-шкала) и поддерживающая терапия (гидратация, нутритивная поддержка, коррекция электролитных нарушений).
Продолжительность ICANS варьируется, но чаще всего составляет 5–10 дней. При своевременной терапии у большинства пациентов симптомы обратимы.
Ведутся клинические исследования по определению биомаркеров ICANS: повышенный уровень ANG2, ICAM-1 и низкий уровень ANG1 ассоциированы с нарушением гематоэнцефалического барьера. Предикция ICANS на раннем этапе терапии поможет индивидуализировать подход к мониторингу и профилактике. Таким образом, ICANS является серьёзным, но контролируемым осложнением CAR-T-терапии. Совершенствование мониторинга, разработка таргетных противовоспалительных агентов и персонализированных алгоритмов вмешательства позволит повысить безопасность терапии и расширить её применение в более уязвимых популяциях.
7.3 Другая сопутствующая токсичность
7.3.1 Прочие побочные эффекты и on-target/off-tumor токсичность
Тяжёлая OTOT-токсичность представляет собой существенное ограничение при разработке CAR-T-клеточной терапии, особенно для солидных опухолей. OTOT возникает в результате распознавания и разрушения нормальных тканей, экспрессирующих опухолеассоциированные антигены (ОАА), которые в силу своей природы не являются строго опухолеспецифичными. Это приводит к поражению здоровых органов-мишеней, несмотря на высокую селективность CAR.
Наиболее частые проявления OTOT включают:
- B-клеточную аплазию и гипогаммаглобулинемию при анти-CD19 терапии;
- Гепатотоксичность, пневмонит, гастроинтестинальные поражения при таргетировании на мезотелин, CEA и другие ОАА в терапии солидных опухолей.
В клинических испытаниях наблюдались тяжёлые летальные осложнения, связанные с экспрессией CAR на тканях, не являющихся опухолевыми [18].
7.3.2 Инфекции
Гипогаммаглобулинемия, вызванная продолжительной B-клеточной аплазией при анти-CD19 терапии, приводит к повышенному риску бактериальных, вирусных и грибковых инфекций, особенно в первые 6–12 месяцев. Частота инфицирования составляет до 55 %, а смертность от инфекций во время СВЦ/ICANS может достигать 15–20 % [79].
Пациентам может потребоваться длительная заместительная терапия иммуноглобулинами, особенно при стойкой B-клеточной деплеции > 6 мес. Также рассматривается профилактика против Pneumocystis jirovecii, ВПГ и ЦМВ [80].
7.3.3 Гематологические и системные осложнения
CAR-T-клеточная терапия сопровождается широким спектром побочных эффектов, выходящих за пределы хорошо охарактеризованных синдромов СВЦ и ICANS. Среди них особое внимание уделяется гематологическим, метаболическим и иммуновоспалительным нарушениям [80].
Гемоцитопения (анемия, тромбоцитопения, лейкопения, нейтропения) является одним из наиболее частых поздних осложнений, сохраняющимся в течение недель после инфузии. Она обусловлена как предварительной лимфодеплецией, так и воздействием цитокинов. Поддерживающая терапия включает назначение колониестимулирующих факторов (например, G-CSF) и компонентов крови.
Синдром лизиса опухоли (TLS) развивается преимущественно у пациентов с высокой опухолевой нагрузкой и характеризуется острыми метаболическими нарушениями, такими как гиперкалиемия, гиперурикемия и гиперфосфатемия. Профилактика и лечение предполагают агрессивную внутривенную гидратацию и применение урикозурических средств, таких как аллопуринол или расбуриказа.
ДВС-синдром и вторичный гемофагоцитарный лимфогистиоцитоз являются редкими, но потенциально жизнеугрожающими осложнениями, возникающими в результате массивного выброса провоспалительных цитокинов. Их развитие требует немедленной диагностики и интенсивной терапии с применением иммуномодуляторов и глюкокортикоидов.
Реакция «трансплантат против хозяина» может развиваться при применении аллогенных CAR-T-клеток и требует строгого мониторинга, особенно в рамках клинических испытаний универсальных или донорских платформ.
7.3.4 Рецидив
Рецидив злокачественного процесса после терапии CAR-T-клетками остается одной из ключевых нерешённых проблем, ограничивающих долговременную эффективность терапии. Согласно обобщённым данным, у 40–60 % пациентов с рецидивирующими/рефрактерными В-клеточными новообразованиями наблюдается возврат заболевания после начального достижения полной ремиссии с использованием CAR-T-клеток. У пациентов с R/R ОЛЛ рецидив отмечается у 30–60 %, при этом в 10–20 % случаев он носит CD19-негативный характер [40].
Выделяют два ключевых типа рецидива:
- CD19-негативный рецидив, обусловленный потерей или изменением целевого антигена;
- CD19-позитивный рецидив, связанный с дисфункцией или ограниченной персистенцией CAR-T-клеток in vivo.
Дополнительным фактором риска служит изначальная экспрессия антигена на низком уровне, что снижает эффективность начального распознавания и способствует выживанию остаточной опухолевой популяции. Исследования показывают, что устойчивость к терапии может быть вызвана также эпигенетическими изменениями и экспрессией иммунорегуляторных молекул опухоли (например, IDO, TGF-β).
8. Стоимость и доступность
CAR-T-клеточная терапия остаётся одной из самых дорогих форм лечения в онкологии: стоимость одного курса может превышать 400000–600000 долларов США. Такая цена обусловлена в первую очередь индивидуализированным процессом производства — каждая доза создаётся из собственных Т-клеток пациента, которые выделяются, модифицируются с помощью вирусных векторов (один только GMP-класс вируса может стоить до 100 000$), затем культивируются, криоконсервируются и возвращаются в клинику. Дополнительно расходы включают логистику, госпитализацию, лимфодеплеционную химиотерапию и лечение тяжёлых побочных эффектов, таких как CRS и ICANS, что может увеличить итоговую стоимость ещё на 160000$ и более. На сегодняшний день CAR-T-терапия одобрена и применяется в США, Китае, странах Европы (Германия, Франция, Великобритания и др.), а также в Израиле и Индии. США лидируют по числу одобренных продуктов и проведённых клинических исследований, в Китае активно развивается собственный рынок с более доступными по цене препаратами, а в Индии недавно был зарегистрирован первый национальный продукт NexCAR19, стоимость которого составляет около 50000$ — в разы дешевле западных аналогов. Однако в странах с низким и средним уровнем дохода доступ к терапии всё ещё крайне ограничен из-за дороговизны и отсутствия необходимой инфраструктуры. Чтобы изменить ситуацию, исследователи и биотехнологические компании разрабатывают новые технологические решения: автоматизированные производственные платформы (например, Cell Shuttle от компании Cellares), аллогенные («off-the-shelf») CAR-T-клетки, которые можно заготавливать заранее, in vivo модификации Т-клеток, позволяющие избежать стадий выделения и культивирования, а также децентрализованное производство прямо в больницах. Эти инновации направлены на то, чтобы сделать CAR-T-терапию не только эффективной, но и по-настоящему доступной — не только для пациентов в крупных центрах США, но и во всём мире.
9. Заключение
Химерные антигенные рецепторы на основе Т-клеток (CAR-T) становятся ключевым элементом трансформации подходов к лечению онкологических заболеваний. Благодаря способности преодолевать иммунную толерантность, устойчиво пролиферировать, мигрировать в опухолевые ниши, взаимодействовать с эндогенным иммунитетом и сохраняться in vivo в течение длительного времени, CAR-T-клетки обеспечивают глубокий и длительный противоопухолевый ответ. Это выгодно отличает их от традиционных моноклональных антител, которые, несмотря на доказанную эффективность, требуют повторного введения и редко приводят к полному излечению.
В ряде гематологических заболеваний применение CAR-T-клеток позволяет отказаться от аллогенной трансплантации гемопоэтических стволовых клеток — дорогостоящей и высокотоксичной процедуры, ранее считавшейся стандартом спасительной терапии. Потенциал технологии выходит за рамки CD19-позитивных В-клеточных опухолей: в настоящее время активно проводятся клинические испытания при других видах рака, включая солидные новообразования и аутоиммунные патологии.
Расширение возможностей CAR-T обусловлено развитием технологий клеточной инженерии, внедрением платформ точного редактирования генома (например, CRISPR/Cas9), совершенствованием логистики и автоматизацией производства. На этом фоне CAR-T-терапия постепенно переходит от экспериментального статуса к промышленной реальности. В обозримом будущем она может стать доступным, персонализированным и, главное, потенциально излечивающим методом лечения для широкого круга онкологических больных.
CAR-T-терапия в России: текущее состояние
В ноябре 2024 года Национальный медицинский исследовательский центр гематологии (НМИЦ гематологии) начал клинические испытания первого отечественного CAR-T препарата под названием «Утжефра» (МНН — гемагенлеклейцел), NCT03467256. Препарат предназначен для лечения агрессивных форм В-клеточных злокачественных новообразований, экспрессирующих антиген CD19, включая рецидивирующие и рефрактерные формы острых лимфобластных лейкозов и лимфом. Клиническое исследование рассчитано на 60 пациентов и продлится до конца 2025 года. «Утжефра» производится на собственной лицензированной площадке НМИЦ гематологии, что позволяет обеспечить полный цикл производства и контроля качества. После завершения клинических испытаний и прохождения всех этапов регистрации планируется масштабирование производства для обеспечения потребностей других медицинских учреждений России [81].
В настоящее время CAR-T-терапия в России находится на стадии клинических исследований, и коммерческое применение ограничено. Однако развитие отечественных препаратов, таких как «Утжефра», и создание производственных мощностей внутри страны могут существенно снизить стоимость лечения по сравнению с импортными аналогами, стоимость которых за рубежом может достигать 400000$–600000$.
Литература
1. Li C.-H. et al. Long-term outcomes of GD2-directed CAR-T cell therapy in patients with neuroblastoma // Nat Med. 2025. Vol. 31, № 4. P. 1125–1129.
2. Medawar P.B. THE BEHAVIOUR AND FATE OF SKIN AUTOGRAFTS AND SKIN HOMOGRAFTS IN RABBITS // A report to the War Wounds Committee of the Medical Research Council. 1944.
3. Quantitative studies on tissue transplantation immunity. II. The origin, strength and duration of actively and adoptively acquired immunity // Proc R Soc Lond B Biol Sci. 1954. Vol. 143, № 910. P. 58–80.
4. Mitchison N.A. STUDIES ON THE IMMUNOLOGICAL RESPONSE TO FOREIGN TUMOR TRANSPLANTS IN THE MOUSE // J Exp Med. 1955. Vol. 102, № 2. P. 157–177.
5. Gross G., Waks T., Eshhar Z. Expression of immunoglobulin-T-cell receptor chimeric molecules as functional receptors with antibody-type specificity // Proc Natl Acad Sci U S A. 1989. Vol. 86, № 24.
6. Dabas P., Danda A. Revolutionizing cancer treatment: a comprehensive review of CAR-T cell therapy // Medical Oncology. 2023. Vol. 40, № 9.
7. Brudno J.N., Maus M. V., Hinrichs C.S. CAR T Cells and T-Cell Therapies for Cancer // JAMA. 2024. Vol. 332, № 22. P. 1924.
8. Nair R., Westin J. CAR T-Cells. 2020. P. 215–233.
9. Chailyan A., Marcatili P., Tramontano A. The association of heavy and light chain variable domains in antibodies: Implications for antigen specificity // FEBS Journal. 2011. Vol. 278, № 16.
10. Sterner R.C., Sterner R.M. CAR-T cell therapy: current limitations and potential strategies // Blood Cancer Journal. 2021. Vol. 11, № 4.
11. Bridgeman J.S. et al. The Optimal Antigen Response of Chimeric Antigen Receptors Harboring the CD3ζ Transmembrane Domain Is Dependent upon Incorporation of the Receptor into the Endogenous TCR/CD3 Complex // The Journal of Immunology. 2010. Vol. 184, № 12. P. 6938–6949.
12. Zhang T., Wu M.-R., Sentman C.L. An NKp30-Based Chimeric Antigen Receptor Promotes T Cell Effector Functions and Antitumor Efficacy In Vivo // The Journal of Immunology. 2012. Vol. 189, № 5.
13. Guedan S. et al. Enhancing CAR T cell persistence through ICOS and 4-1BB costimulation // JCI Insight. 2018. Vol. 3, № 1.
14. Fujiwara K. et al. Hinge and Transmembrane Domains of Chimeric Antigen Receptor Regulate Receptor Expression and Signaling Threshold // Cells. 2020. Vol. 9, № 5. P. 1182.
15. Sadelain M., Brentjens R., Rivière I. The promise and potential pitfalls of chimeric antigen receptors // Current Opinion in Immunology. 2009. Vol. 21, № 2.
16. Maher J. et al. Human T-lymphocyte cytotoxicity and proliferation directed by a single chimeric TCRζ/CD28 receptor // Nat Biotechnol. 2002. Vol. 20, № 1.
17. Ramello M.C. et al. An immunoproteomic approach to characterize the CAR interactome and signalosome // Sci Signal. 2019. Vol. 12, № 568.
18. Morgan R.A. et al. Case report of a serious adverse event following the administration of t cells transduced with a chimeric antigen receptor recognizing ERBB2 // Molecular Therapy. 2010. Vol. 18, № 4.
19. Chmielewski M., Hombach A.A., Abken H. Of CARs and TRUCKs: Chimeric antigen receptor (CAR) T cells engineered with an inducible cytokine to modulate the tumor stroma // Immunol Rev. 2014. Vol. 257, № 1.
20. Asmamaw Dejenie T. et al. Current updates on generations, approvals, and clinical trials of CAR T-cell therapy // Human Vaccines and Immunotherapeutics. 2022. Vol. 18, № 6.
21. Steentoft C. et al. Glycan-directed CAR-T cells // Glycobiology. 2018. Vol. 28, № 9.
22. Mitra A. et al. From bench to bedside: the history and progress of CAR T cell therapy // Frontiers in Immunology. 2023. Vol. 14.
23. Stroncek D.F. et al. Myeloid cells in peripheral blood mononuclear cell concentrates inhibit the expansion of chimeric antigen receptor T cells // Cytotherapy. 2016. Vol. 18, № 7.
24. Ruella M. et al. Induction of resistance to chimeric antigen receptor T cell therapy by transduction of a single leukemic B cell // Nat Med. 2018. Vol. 24, № 10.
25. Scholler J. et al. Decade-long safety and function of retroviral-modified chimeric antigen receptor T cells // Sci Transl Med. 2012. Vol. 4, № 132.
26. Milone M.C., O’Doherty U. Clinical use of lentiviral vectors // Leukemia. 2018. Vol. 32, № 7.
27. Ottaviano G., Qasim W. Current landscape of vector safety and genotoxicity after hematopoietic stem or immune cell gene therapy // Leukemia. 2025.
28. Fraietta J.A. et al. Disruption of TET2 promotes the therapeutic efficacy of CD19-targeted T cells // Nature. 2018. Vol. 558, № 7709.
29. Feins S. et al. An introduction to chimeric antigen receptor (CAR) T-cell immunotherapy for human cancer // American Journal of Hematology. 2019. Vol. 94, № S1.
30. Canelo-Vilaseca M. et al. Lymphodepletion chemotherapy in chimeric antigen receptor-engineered T (CAR-T) cell therapy in lymphoma // Bone Marrow Transplant. 2025. Vol. 60, № 5. P. 559–567.
31. Kröger N. et al. The EBMT/EHA CAR-T cell handbook // The EBMT/EHA CAR-T Cell Handbook. 2022.
32. Rees J.H. Management of Immune Effector Cell-Associated Neurotoxicity Syndrome (ICANS) // The EBMT/EHA CAR-T Cell Handbook. 2022.
33. Jain M.D., Smith M., Shah N.N. How I treat refractory CRS and ICANS after CAR T-cell therapy // Blood. 2023. Vol. 141, № 20.
34. Fda. Long Term Follow-Up After Administration of Human Gene Therapy Products // Guidance for Industry. 2020.
35. Ploch W. et al. Advancement and Challenges in Monitoring of CAR-T Cell Therapy: A Comprehensive Review of Parameters and Markers in Hematological Malignancies // Cancers (Basel). 2024. Vol. 16, № 19. P. 3339.
36. Huang S. et al. Deciphering and advancing CAR T-cell therapy with single-cell sequencing technologies // Molecular Cancer. 2023. Vol. 22, № 1.
37. Abdo L., Batista-Silva L.R., Bonamino M.H. Cost-effective strategies for CAR-T cell therapy manufacturing // Molecular Therapy Oncology. 2025. Vol. 33, № 2. P. 200980.
38. Bhaskar S.T. et al. Overview of approved CAR-T products and utility in clinical practice // Clin Hematol Int. 2024. Vol. 6, № 4.
39. Sermer D. et al. Targeting CD19 for diffuse large B cell lymphoma in the era of CARs: Other modes of transportation // Blood Reviews. 2023. Vol. 57.
40. Maude S.L. et al. Tisagenlecleucel in Children and Young Adults with B-Cell Lymphoblastic Leukemia // New England Journal of Medicine. 2018. Vol. 378, № 5.
41. Locke F.L. et al. Long-term safety and activity of axicabtagene ciloleucel in refractory large B-cell lymphoma (ZUMA-1): a single-arm, multicentre, phase 1–2 trial // Lancet Oncol. 2019. Vol. 20, № 1.
42. Wang M. et al. KTE-X19 CAR T-Cell Therapy in Relapsed or Refractory Mantle-Cell Lymphoma // New England Journal of Medicine. 2020. Vol. 382, № 14.
43. Wang M. et al. Lisocabtagene Maraleucel in Relapsed/Refractory Mantle Cell Lymphoma: Primary Analysis of the Mantle Cell Lymphoma Cohort From TRANSCEND NHL 001, a Phase I Multicenter Seamless Design Study // Journal of Clinical Oncology. 2024. Vol. 42, № 10.
44. Munshi N.C. et al. Idecabtagene Vicleucel in Relapsed and Refractory Multiple Myeloma // New England Journal of Medicine. 2021. Vol. 384, № 8.
45. Berdeja J.G. et al. Ciltacabtagene autoleucel, a B-cell maturation antigen-directed chimeric antigen receptor T-cell therapy in patients with relapsed or refractory multiple myeloma (CARTITUDE-1): a phase 1b/2 open-label study // The Lancet. 2021. Vol. 398, № 10297.
46. Coiffier B. et al. Long-term outcome of patients in the LNH-98.5 trial, the first randomized study comparing rituximab-CHOP to standard CHOP chemotherapy in DLBCL patients: A study by the Groupe d’Etudes des Lymphomes de l’Adulte // Blood. 2010. Vol. 116, № 12.
47. Pandey P., Gogia A. Axicabtagene ciloleucel as second-line therapy for large B-cell lymphoma // Cancer Research, Statistics, and Treatment. 2022. Vol. 5, № 2.
48. Schuster S.J. et al. Tisagenlecleucel in Adult Relapsed or Refractory Diffuse Large B-Cell Lymphoma // New England Journal of Medicine. 2019. Vol. 380, № 1.
49. Kamdar M. et al. Lisocabtagene maraleucel versus standard of care with salvage chemotherapy followed by autologous stem cell transplantation as second-line treatment in patients with relapsed or refractory large B-cell lymphoma (TRANSFORM): results from an interim analysis of an open-label, randomised, phase 3 trial // The Lancet. 2022. Vol. 399, № 10343.
50. Gökbuget N. et al. Adult patients with acute lymphoblastic leukemia and molecular failure display a poor prognosis and are candidates for stem cell transplantation and targeted therapies // Blood. 2012. Vol. 120, № 9.
51. Maude S.L. et al. Chimeric Antigen Receptor T Cells for Sustained Remissions in Leukemia // New England Journal of Medicine. 2014. Vol. 371, № 16.
52. Shah B.D. et al. KTE-X19 for relapsed or refractory adult B-cell acute lymphoblastic leukaemia: phase 2 results of the single-arm, open-label, multicentre ZUMA-3 study // The Lancet. 2021. Vol. 398, № 10299.
53. Fry T.J. et al. CD22-targeted CAR T cells induce remission in B-ALL that is naive or resistant to CD19-targeted CAR immunotherapy // Nat Med. 2018. Vol. 24, № 1.
54. Tan Y. et al. Long-term follow-up of donor-derived CD7 CAR T-cell therapy in patients with T-cell acute lymphoblastic leukemia // J Hematol Oncol. 2023. Vol. 16, № 1.
55. San-Miguel J. et al. Cilta-cel or Standard Care in Lenalidomide-Refractory Multiple Myeloma // New England Journal of Medicine. 2023. Vol. 389, № 4.
56. Li C. et al. CT103A, a novel fully human BCMA-targeting CAR-T cells, in patients with relapsed/refractory multiple myeloma: Updated results of phase 1b/2 study (FUMANBA-1). // Journal of Clinical Oncology. 2023. Vol. 41, № 16_suppl.
57. Mei H. et al. A bispecific CAR-T cell therapy targeting BCMA and CD38 in relapsed or refractory multiple myeloma // J Hematol Oncol. 2021. Vol. 14, № 1.
58. O’Neal J. et al. CS1 CAR-T targeting the distal domain of CS1 (SLAMF7) shows efficacy in high tumor burden myeloma model despite fratricide of CD8+CS1 expressing CAR-T cells // Leukemia. 2022. Vol. 36, № 6.
59. Wang M. et al. Three-Year Follow-Up of KTE-X19 in Patients With Relapsed/Refractory Mantle Cell Lymphoma, Including High-Risk Subgroups, in the ZUMA-2 Study // Journal of Clinical Oncology. 2022. Vol. 94.
60. Fraietta J.A. et al. Determinants of response and resistance to CD19 chimeric antigen receptor (CAR) T cell therapy of chronic lymphocytic leukemia // Nat Med. 2018. Vol. 24, № 5.
61. Alizadeh D. et al. IL15 enhances CAR-T cell antitumor activity by reducing mTORC1 activity and preserving their stem cell memory phenotype // Cancer Immunol Res. 2019. Vol. 7, № 5.
62. Deng Q. et al. Characteristics of anti-CD19 CAR T cell infusion products associated with efficacy and toxicity in patients with large B cell lymphomas // Nat Med. 2020. Vol. 26, № 12.
63. Rossi J. et al. Preinfusion polyfunctional anti-CD19 chimeric antigen receptor T cells are associated with clinical outcomes in NHL // Blood. 2018. Vol. 132, № 8.
64. Turtle C.J. et al. CD19 CAR-T cells of defined CD4+:CD8+ composition in adult B cell ALL patients // Journal of Clinical Investigation. 2016. Vol. 126, № 6.
65. Shen L. et al. Metabolic reprogramming by ex vivo glutamine inhibition endows CAR-T cells with less-differentiated phenotype and persistent antitumor activity // Cancer Lett. 2022. Vol. 538.
66. Philip M. et al. Chromatin states define tumour-specific T cell dysfunction and reprogramming // Nature. 2017. Vol. 545, № 7655.
67. Ruella M., Maus M. V. Catch me if you can: Leukemia Escape after CD19-Directed T Cell Immunotherapies // Computational and Structural Biotechnology Journal. 2016. Vol. 14.
68. Sotillo E. et al. Convergence of acquired mutations and alternative splicing of CD19 enables resistance to CART-19 immunotherapy // Cancer Discov. 2015. Vol. 5, № 12.
69. Jacoby E. et al. CD19 CAR immune pressure induces B-precursor acute lymphoblastic leukaemia lineage switch exposing inherent leukaemic plasticity // Nat Commun. 2016. Vol. 7.
70. Orlando E.J. et al. Genetic mechanisms of target antigen loss in CAR19 therapy of acute lymphoblastic leukemia // Nat Med. 2018. Vol. 24, № 10.
71. Ghorashian S. et al. Enhanced CAR T cell expansion and prolonged persistence in pediatric patients with ALL treated with a low-affinity CD19 CAR // Nat Med. 2019. Vol. 25, № 9.
72. Cherkassky L. et al. Human CAR T cells with cell-intrinsic PD-1 checkpoint blockade resist tumor-mediated inhibition // Journal of Clinical Investigation. 2016. Vol. 126, № 8.
73. Cao Y. et al. Anti-CD19 chimeric antigen receptor T cells in combination with nivolumab are safe and effective against relapsed/refractory B-cell non-hodgkin lymphoma // Front Oncol. 2019. Vol. 9, № AUG.
74. Depil S. et al. ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges // Nature Reviews Drug Discovery. 2020. Vol. 19, № 3.
75. Lee D.W. et al. Current concepts in the diagnosis and management of cytokine release syndrome // Blood. 2014. Vol. 124, № 2.
76. Hay K.A. et al. Kinetics and biomarkers of severe cytokine release syndrome after CD19 chimeric antigen receptor–modified T-cell therapy // Blood. 2017. Vol. 130, № 21.
77. Lee D.W. et al. ASTCT Consensus Grading for Cytokine Release Syndrome and Neurologic Toxicity Associated with Immune Effector Cells // Biology of Blood and Marrow Transplantation. 2019. Vol. 25, № 4.
78. Jung S. et al. Fatal late-onset CAR T-cell–mediated encephalitis after axicabtagene-ciloleucel in a patient with large B-cell lymphoma // Blood Adv. 2021. Vol. 5, № 19.
79. Hill J.A. et al. Infectious complications of CD19-targeted chimeric antigen receptor-modified T-cell immunotherapy // Blood. 2018. Vol. 131, № 1.
80. Neelapu S.S. et al. Chimeric antigen receptor T-cell therapy-assessment and management of toxicities // Nature Reviews Clinical Oncology. 2018. Vol. 15, № 1.
81. The first clinical trial of a domestic CAR-T-cell drug has begun [Электронный ресурс] / Blood.ru. — 2025. — Режим доступа: https://blood.ru/en/about/news/the-first-clinical-trial-of-a-domestic-car-t-cell-drug-has-begun/ (дата обращения: 15.05.2025).
