Нейропротез для поддержания артериального давления после травмы спинного мозга
Неспособность поддерживать артериальное давление — инвалидизирующее последствие травмы спинного мозга. Эту проблему удалось обойти, искусственно воссоздав рефлекс, необходимый для стабилизации артериального давления.
Паралич и сенсорная недостаточность — наиболее очевидные последствия травмы спинного мозга (ТСМ). Но многие люди также испытывают ортостатическую гипотензию — невозможность поддержания артериального давления при переходе из положения лежа в положение сидя или стоя. В краткосрочной перспективе это состояние может препятствовать нормальному наполнению сердца кровью и вызывать помутнение сознания и головокружение. В долгосрочной — повторяющиеся эпизоды ортостатической гипотензии увеличивают частоту сердечных приступов и инсультов, которые являются основными причинами смерти у людей, перенесших ТСМ. В своей статье в «Nature» Squair с соавт. [2] сообщают о стратегии нейропротезирования, которая сводит к минимуму ортостатическую гипотензию, вызванную ТСМ. Устройство способствует восстановлению контроля артериального давления у грызунов, обезьян и людей.
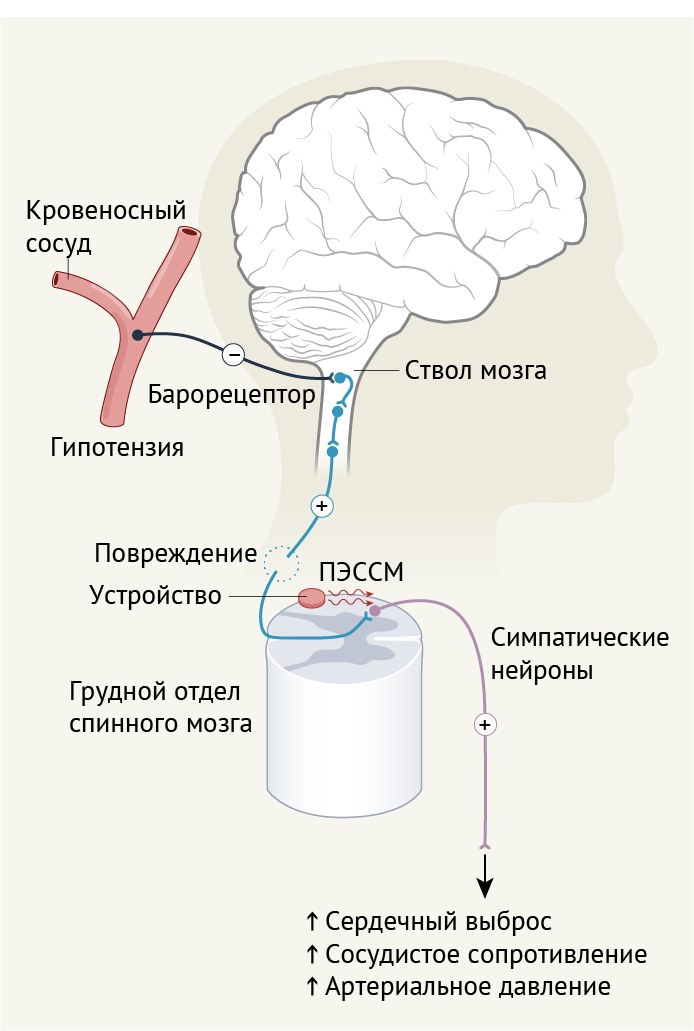
Когда мы сидим или стоим, сила тяжести заставляет кровь скапливаться в нижней части тела. Ортостатическая гипотензия возникает в основном из-за нарушения рефлексов, препятствующих этому накоплению крови. Наиболее важным из них является барорефлекс, который запускается с барорецепторов — нейронов, которые определяют («чувствуют») артериальное давление и степень заполнения крупных вен и камер сердца [3]. У млекопитающих эти сенсоры активны, когда тело находится в состоянии покоя. Снижение артериального давления или объема крови снижает активность барорецепторов. Это, в свою очередь, активирует симпатическую ветвь вегетативной нервной системы, восстанавливая давление в кровеносном русле за счет увеличения сопротивления сосудов и притока крови обратно к сердцу. ТСМ нарушает связь между нижней частью ствола мозга, который получает информацию от барорецепторов, и симпатическими нейронами, иннервирующими сердечно-сосудистую систему, которые берут начало в грудном и верхнем поясничном сегментах спинного мозга (рис. 1).
Ортостатическую гипотензию обычно лечат изменением образа жизни (использованием компрессионных повязок на ногах и сном в полувертикальном положении) и такими препаратами, как флудрокортизон (увеличивает объем циркулирующей крови) или мидодрин (активирует рецепторы, которые обычно опосредуют эффект симпатических нервов на сердце и мышечную стенку сосудов) [5, 6]. Однако у этих препаратов имеются и нежелательные эффекты. Другие методы включают электрическую стимуляцию скелетных мышц нижних конечностей, что способствует активации мышечного насоса и помогает наполнению сердца, а также использование поясов-корсетов на живот (для создания адекватного внутрибрюшного давления). Обе эти стратегии использовались в терапии данного состояния, но особой эффективности с их помощью достигнуть не удалось [6].
Могут ли нейропротезы оказаться лучшей альтернативой? Принцип их работы заключается в восстановлении функции путем электрической стимуляции нервных путей, которые перестали реагировать в результате ТСМ. В идеале стимуляция должна точно соответствовать тому режиму активности, который необходим для контроля целевой функции организма. Такой подход уже применялся для частичного восстановления передвижения у приматов [7]. Он также использовался для активации мышц ног для улучшения контроля артериального давления у людей с ТСМ, хотя причины успешного применения этой методики в этой ситуации оказались не ясны.
Squair с соавт. решили разработать более точный нейропротез для контроля артериального давления. Для начала исследователи смоделировали ТСМ на крысах. Анализ нейрональной активности в модели выявил, что артериальное давление и симпатические реакции у этих животных оказались нестабильны. Вследствие небольших размеров у крыс не наблюдалась ортостатическая гипотензия. Однако авторами использовалась камера отрицательного давления, чтобы уменьшить давление воздуха вокруг нижней части тела животного; это заставило кровь скапливаться в нижней части тела, подтверждая это явление.
Затем Squair с соавт. решили выяснить, где необходимо применить электрическую стимуляцию (называемую прицельной эпидуральной стимуляцией спинного мозга, ПЭССМ), чтобы вызвать симпатические реакции, которые изменяют артериальное давление. Они систематически стимулировали сегменты спинного мозга у травмированных крыс и обнаружили, что можно добиться существенного повышения артериального давления у животных, воздействуя электрическими импульсами вблизи задней стороны нижнего грудного отдела спинного мозга. Впечатляющая серия экспериментов — визуализационные методики и анатомический анализ в сочетании с компьютерным моделированием и манипуляциями для активации или ингибирования нейронов, функционирующих в этой области, — показала, что ПЭССМ способствует повышению артериального давления, активируя группу чувствительных афферентных нейронов (которые передают сигналы от кожи, мышц и внутренних органов к спинному мозгу). Эти афферентные нейроны косвенно возбуждают эфферентные симпатические нейроны, которые контролируют кровообращение во внутренних органах (кровеносные сосуды органов брюшной полости).
Следующим весьма оригинальным шагом исследователей было создание устройства биомиметического контроля, которое непрерывно регулирует частоту стимуляции ПЭССМ, чтобы предотвратить любое падение артериального давления у травмированных крыс. Затем им удалось успешно адаптировать концепцию «протезного барорефлекса» для макак-резусов. Они еще раз протестировали каждый сегмент позвоночника, чтобы определить, на какой необходимо воздействовать ПЭССМ, и провели масштабирование локации протеза, чтобы она соответствовала анатомии обезьяны. Наконец, что наиболее примечательно, ученым удалось показать, что протезный барорефлекс может восстановить стабильность артериального давления у человека, у которого возникла инвалидизирующая ортостатическая гипотензия после ТСМ.
Это «прикроватное» исследование беспрецедентно во многих отношениях и, как таковое, вызывает несколько вопросов. К примеру, точно не определено, на какие чувствительные нейроны воздействует протез, и неизвестны долгосрочные эффекты такой их стимуляции. После травмы позвоночника происходит перестройка кровоснабжения спинного мозга, и обостряются рефлексы, так что ранее безобидные стимулы могут вызывать приступы опасно высокого артериального давления. Только время и дальнейшие эксперименты покажут, будет ли хроническая активация этих афферентных нейронов смягчать или усугублять действие этих гиперактивных рефлексов. Действительно, в отличие от настоящего барорефлекса, протезный барорефлекс намного надежнее предотвращает приступы гипотонии, нежели чем смягчает проявления гипертонии.
Кроме того, нейропротез может оказать неблагоприятное воздействие на функции желудочно-кишечного тракта и почек, которые регулируются нижними грудными симпатическими нейронами. Наконец, для размещения эпидурального электрода в позвоночнике требуется инвазивная процедура, а срок работы устройства (в отдаленной перспективе) не ясен.
Тем не менее, это новейшая попытка по лечению инвалидизирующей артериальной гипотензии, развивающейся вследствие ТСМ, и она основана на большом количестве доклинических нейробиологических доказательств. На данный момент это самая сложная методика. Предполагается, что этот подход может заменить доступные в настоящее время методы лечения, хотя говорить об этом однозначно пока рано.
