Как ожирение влияет на почки?
Эпидемиология
За последние три десятилетия распространенность избыточного веса и ожирения среди взрослых во всем мире существенно увеличилась. В странах с низким и средним уровнем дохода в настоящее время наблюдаются признаки перехода от нормальной массы тела к избыточному весу и ожирению, как это произошло несколько десятилетий назад в некоторых частях Европы и США. Эта растущая распространенность ожирения имеет значение для сердечно-сосудистых заболеваний (ССЗ), а также для ХБП. Высокий ИМТ является одним из важных факторов риска развития ХБП.
▶ Читайте также: Хроническая болезнь почек: главное из исследований
Механизмы повреждения почек при ожирении
Ожирение вызывает гломерулярные заболевания с фенотипом фокально-сегментарного гломерулосклероза (ФСГС), которые обычно называют гломерулопатия, связанная с ожирением (ГСЖ).
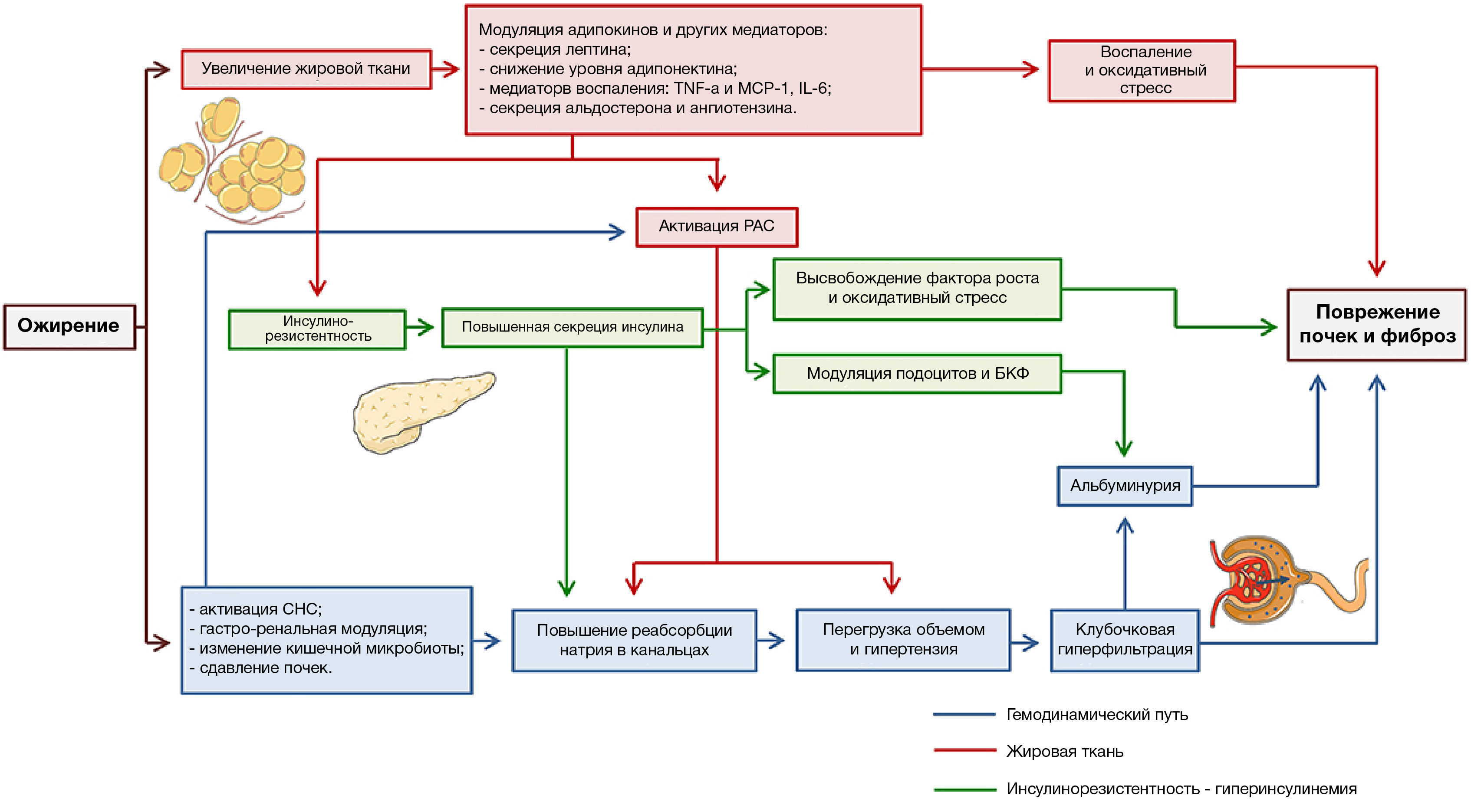
Рисунок 1 | Пути, участвующие в заболевании почек, связанном с ожирением
García-Carro, Clara, et al. "A nephrologist perspective on obesity: from kidney injury to clinical management." Frontiers in Medicine 8 (2021): 655871.
Три ключевых пути (гемодинамический, связанный с жировой тканью и инсулинорезистентности-гиперинсулинемии) различаются по цвету (см. схему выше). Совместное взаимодействие этих трех путей способствует повреждению почек.
Гемодинамический путь
Ожирение повышает реабсорбцию натрия в канальцах, что вызывает перегрузку объемом и развитие артериальной гипертензии, способствующей гиперфильтрации и микрососудистому поражению почек. Активация ренин-ангиотензиновой системы (РАС) также была обнаружена у пациентов с ожирением и на животных моделях. В некоторых исследованиях указано, что при ожирении реабсорбция натрия изначально происходит в начальных сегментах канальцев, в частности в проксимальных канальцах и восходящей петле Генле. Это приводит к уменьшению доставки натрия к дистальным сегментам канальцев, что воспринимается клетками macula densa, активируя тубулогломерулярную обратную связь и вызывая секрецию ренина юкстагломерулярным аппаратом. Данный механизм сходен с механизмом, способствующим гиперфильтрации при диабетической нефропатии.
Путь, связанный с жировой тканью
Адипоциты — активные клетки, вырабатывающие цитокины, известные как адипокины. В почечных заболеваниях, связанных с ожирением, задействованы адипокины, такие как лептин, адипонектин, фактор некроза опухоли α (TNF-α) и интерлейкин 6 (IL-6). Секреция лептина увеличивается у лиц с ожирением и связана с активацией симпатической нервной системы, что способствует гипертонии, а инфузия лептина у крыс повышает среднее артериальное давление. Лептин также усиливает окисление жирных кислот, окислительный стресс и выработку провоспалительных цитокинов, вроде хемоаттрактантного белка моноцитов 1 (MCP-1). В то время как уровни адипонектина снижаются у пациентов с ожирением. У мышей с низким уровнем адипонектина было обнаружено сглаживание стопы подоцита, что ведет к увеличению альбуминурии, а альбуминурия частично устраняется при введении экзогенного адипонектина. Жировая ткань также регулирует РАС. В адипоцитах обнаружена секреция альдостерона и ангиотензиногена. Альдостерон, вырабатываемый жировой тканью, участвует в дифференцировке адипоцитов и связан с гипертонией, вызванной ожирением.
Инсулинорезистентность
Еще один путь — инсулинорезистентность. Она способствует компенсаторной секреции инсулина, который воздействует на почки разными способами. Инсулин влияет на подоциты через инсулиновые рецепторы. Внутриклеточный путь AKT/mTOR или переносчик глюкозы 4 (GLUT4) связаны с передачей его сигналов. Инсулин участвует в функционировании подоцитов и регулировании актинового цитоскелета. Таким образом, повышенная секреция инсулина влияет на селективность барьера клубочковой фильтрации, что приводит к протеинурии. В экспериментах на крысах и культивированных подоцитах введение инсулина увеличивает проницаемость для альбумина. Кроме того, инсулин способствует окислительному стрессу в подоцитах через активацию NADPH-оксидазы. Инсулин также воздействует на канальцы и в культивированных клетках проксимальных канальцев почек, где он стимулирует образование TGF-β и коллагена IV, что в конечном итоге приводит к тубулоинтерстициальному фиброзу. Помимо этого, ожирение является важным фактором риска развития диабета, который представляет собой наиболее распространенную причину хронической болезни почек во всем мире.
Связь ожирения и ХБП
Связь между ожирением и хронической болезнью почек (ХБП) была впервые обнаружена в 1974 году. Увеличение ИМТ на одну единицу повышает риск развития ХБП на 20 % в течение 20 лет. Как отмечалось ранее, абдоминальный жир и центральное ожирение тесно связаны с началом и тяжестью метаболического синдрома, который является важным фактором риска развития ХБП в общей популяции.
Связь ожирения с почечными осложнениями без ХБП
Ожирение также связано с почечными осложнениями у лиц без ХБП. Более высокий ИМТ коррелирует с наличием и прогрессированием протеинурии у лиц без заболеваний почек. Кроме того, в ряде крупных исследований населения более высокий ИМТ ассоциирован с наличием и развитием низкой расчетной скорости клубочковой фильтрации (СКФ) и с более быстрой потерей расчетной СКФ со временем.
Как ожирение влияет на диагноз ХБП
Ожирение влияет на диагноз и прогрессирование ХБП. Повышенный ИМТ и ожирение II степени и выше ассоциированы с более быстрым прогрессированием ХБП, если она уже есть у пациента. Ожирение также является сильным предиктором прогрессирования потери функции почек при ХБП. Например, при IgA-нефропатии ожирение увеличивает частоту гипертензии, протеинурии, тяжелых гистологических изменений и риск развития терминальной стадии почечной недостаточности. С другой стороны, недавнее когортное исследование 1940 пациентов, наблюдаемых в течение более 3 лет, показало, что как метаболические нарушения, так и ожирение независимо связаны со значительно повышенным риском прогрессирования ХБП, а пациенты с ожирением без метаболических нарушений также имеют повышенный риск прогрессирования ХБП. Таким образом, ожирение, вероятно, оказывает как прямое, так и косвенное (через сопутствующие метаболические нарушения) неблагоприятное влияние на скорость прогрессирования ХБП.
Ожирение и трансплантация почек
В соответствии с большинством рекомендаций по клиническому управлению, ожирение не является абсолютным противопоказанием для пересадки почки. Тем не менее на практике многие трансплантационные центры предпочитают избегать пересадки почек пациентам с ожирением, считая ИМТ > 35 кг/м² относительным противопоказанием для данной процедуры. В большом популяционном исследовании, основанном на данных от United Network for Organ Sharing (UNOS), включавшем 132 353 пациента из списка ожидания, обнаружено, что вероятность получения операции по пересадке почки снижается с увеличением ИМТ. Кроме того, среди лиц, прошедших аллотрансплантацию, пациенты с ожирением чаще исключались из исследования по мере роста ИМТ.
Важно подчеркнуть, что исследования показывают, что пересадка почек у пациентов с ожирением обеспечивает более высокую выживаемость, чем продолжение диализа. В регистрационном исследовании, проведенном с использованием данных из Системы почечных данных США (USRDS) и включавшем 7443 пациентов с ожирением, смертность среди тех, кто прошел пересадку почки, была в два раза ниже, чем среди тех, кто оставался в списке ожидания (3,3 случая смерти против 6,6 случаев смерти на 100 пациентов в год), причем смертность была еще ниже в подгруппе пациентов, получивших трансплантат от живого донора. Однако данное преимущество в выживаемости не достигалось у пациентов с ИМТ ≥40 кг/м².
Существуют противоречивые данные касательно связи между выживаемостью пациентов, трансплантатов и ожирением. Некоторые исследования выявили отрицательное воздействие ожирения на выживаемость пациентов и трансплантатов, в то время как другие не обнаружили такой связи. В систематическом обзоре и мета-анализе, включающем 138081 реципиента донорской почки, ожирение ассоциировалось с повышенной недостаточностью трансплантата, однако различий в выживаемости между пациентами с ожирением и без него не обнаружено. В крупном регистровом исследовании с более чем 50000 пациентов были зафиксированы худшие результаты для трансплантата и пациентов с крайне низким и крайне высоким ИМТ. Недавний систематический обзор, включающий данные свыше 200000 получателей почечных трансплантатов, выявил худшую выживаемость пациентов и трансплантатов через один, два и три года после пересадки среди пациентов с ожирением по сравнению с таковыми без ожирения. В то же время, исследование, основанное на регистре ANZDATA (n = 5864), не показало независимой связи между ожирением и выживаемостью пациента или трансплантата, хотя у пациентов с ожирением чаще наблюдалась задержанная функция трансплантата и острое отторжение. Другие одноцентровые ретроспективные исследования не выявили влияния ожирения на выживаемость пациентов или потерю трансплантата при сравнении результатов в случае ожирения и без него. Интересно, что в одном ретроспективном одноцентровом исследовании выживаемость пациентов и трансплантатов у лиц с ожирением была сравнима с пациентами без ожирения, когда из анализа были исключены испытуемые, столкнувшиеся с осложнениями хирургического профиля.
Заключение
Глобальная эпидемия ожирения оказывает влияние на население планеты во множестве аспектов. Заболевания почек, такие как ХБП, нефролитиаз и рак, являются одними из самых коварных последствий ожирения. Они вызывают масштабные негативные последствия, приводя к значительному росту заболеваемости, смертности и чрезмерным расходам для отдельных людей и системы здравоохранения. Популяционные меры по борьбе с ожирением могут способствовать предупреждению развития или замедлению прогрессии ХБП. Медицинскому сообществу необходимо разработать долгосрочные стратегии для улучшения понимания взаимосвязи между ожирением и заболеваниями почек, а также определить наилучшие подходы для противодействия этой тенденции.
