Катаболизм и биоэнергетика

Глава 1 | Метаболизм азотистых оснований
Глава 2 | Биосинтез макромолекул
Речь пойдет о распаде макромолекул — преимущественно липидов и сахаров — до мономеров и воды с пеплом. А также обо всем, что с этими путями связано (а связано очень много). Тема важная. Тема интересная. Порою ее понимание дает ответы на ряд вопросов и вскрывает тайны происхождения ужасных картин, которые ты можешь наблюдать в стационаре и в жизни, дает адекватное понимание диететики и в целом делает тебя адекватнее. В этот раз ты узнаешь, как и почему вафли со сгущенкой и шоколадом не сделают тебя сладкой конфеткой, а приведут к отложению ненужного жира в боках. Как выживает мозг, когда у тебя пять пар. А если серьезно, то осилив этот раздел, ты поймешь, почему бессмысленна безуглеводная диета, почему развивается ацидоз и к каким последствиям это может привести. Мы коснемся базы, необходимой для понимания множества клинических проблем. Отрывки, объясняющие процессы распада углеводов и липидов, местами могут показаться нудными; если знаешь их, пропусти (только попробуй).
Судьба углеводов в суровом организме: в главной роли — глюкоза
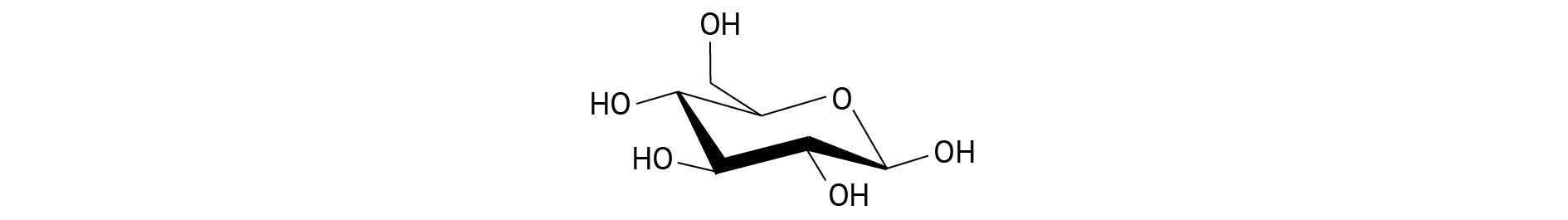
Взгляни на эту красоту. На это настоящее чудо биохимии, на одну из самых активных молекул нашего организма. По количеству реакций, в которых она фигурирует, можно поначалу подумать, что наша жизнь есть способ существования глюкозы [1].
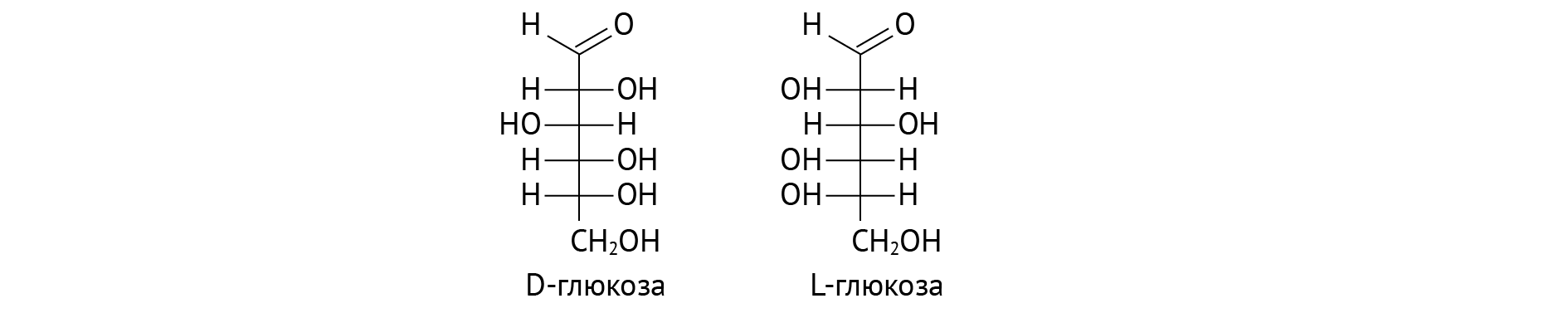
Мы имеем дело гидроксиальдегидом на основе шести атомов углерода и имеющим пять гидроксильных групп. Это делает глюкозу чрезвычайно водолюбивой и открывает просторы для биохимического синтеза. В нашем организме функционирует D-форма глюкозы, и только такая форма способна участвовать в ферментативных реакциях.
Внешний обмен углеводов
О пищевых источниках глюкозы тебе хорошо известно. Это различные овощи и фрукты, оциллококцинум, сладости, пряности и прочее. Гораздо интереснее, что с ней происходит при приеме через рот [3].
Глюкоза попадает в организм в виде полимеров — крахмала, целлюлозы, гликогена. Но не из всех них можно с одинаковой эффективностью вылущить глюкозу. Крахмал и гликоген начинает расщепляться ещё в ротовой полости благодаря α-амилазе из слюнных желез. Происходит разрушение α-1,4-гликозидных связей (связей между первым атомом углерода одной молекулы и четвертым атомом соседней молекулы углевода). К слову, в организме расщепляются только такие связи.
Процесс продолжается в кишечнике (просвете двенадцатиперстной кишки), где под действием α-амилазы поджелудочной железы происходит образование углеводных мономеров и димеров. В качестве мономеров не обязательно получается только глюкоза. Это может быть и фруктоза, и галактоза, но, как мы увидим дальше, все они имеют одинаковую судьбу. Далее начинается их абсорбция [1, 3].
В абсорбции молекул моносахаров в кишечнике важную роль играет вторичный активный транспорт.
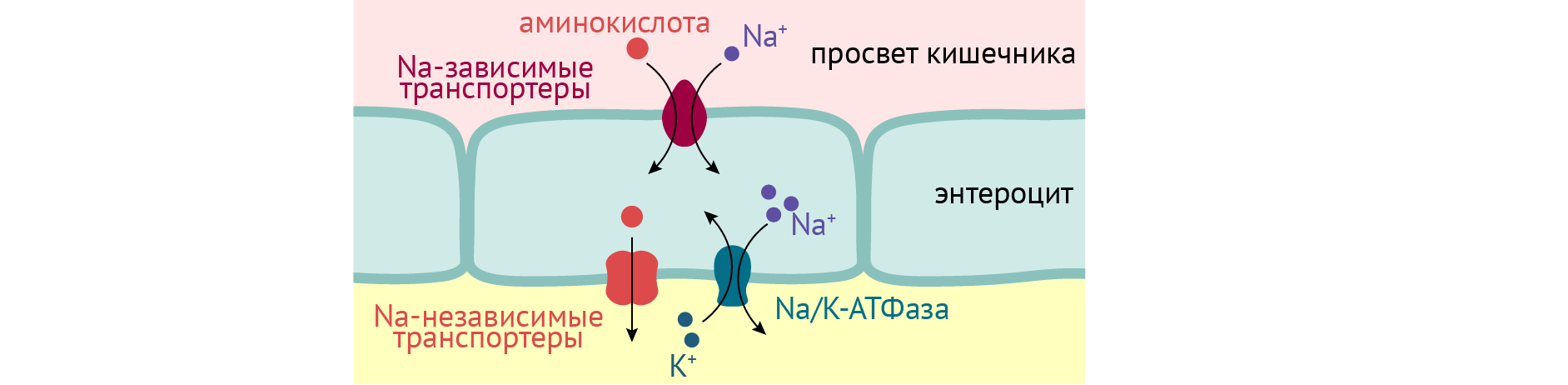
Здесь все максимально просто. Глюкоза (как и другие мономеры) нагло использует натрий. Увидев в нем внутренний потенциал в виде электрохимического градиента, она заманивает его на специальный белковый переносчик в мембране энтероцита. Тут то она и берет его в оборот, заставляя оборачиваться вокруг своей оси еще и белок-переносчик. Это происходит в результате изменения его конформации — взаимной пространственной ориентации компонентов этой большой молекулы. В итоге и глюкоза, и натрий оказываются внутри клетки. Поскольку натрий двигается по своему градиенту, освобождаясь от белка-переносчика, он выделяет малое количество энергии. Но этого количества достаточно, чтобы глюкоза расплатилась с переносчиком за такси через клеточную мембрану и спокойно ушла вглубь энтероцита. Увидев большой город в виде цитоплазмы энтероцита, глюкоза имеет два пути: остаться здесь (потом расскажу, что произойдет) или же двигаться дальше к своей мечте, для чего она прыгает в кровь. И тут начинаются высокие материи [2].
Путешествия глюкозы
Существует гомеостатический механизм, обеспечивающий поддержание физиологического уровня глюкозы в крови, и он сложнее, чем кажется на первый взгляд. Главным его компонентом и сигналом, — хэдлайнером — является глюкоза. А один из основных датчиков — «подчиняющихся» элементов этой игры — В-клетки поджелудочной железы. С них и начнем [1–3, 4].
Шаг 1. Попадание глюкозы в клетку. В-клетки поджелудочной активно экспрессируют ГЛЮТ2 — переносчик глюкозы. Попадая в В-клетки, глюкоза подвергается фосфорилированию (активации):
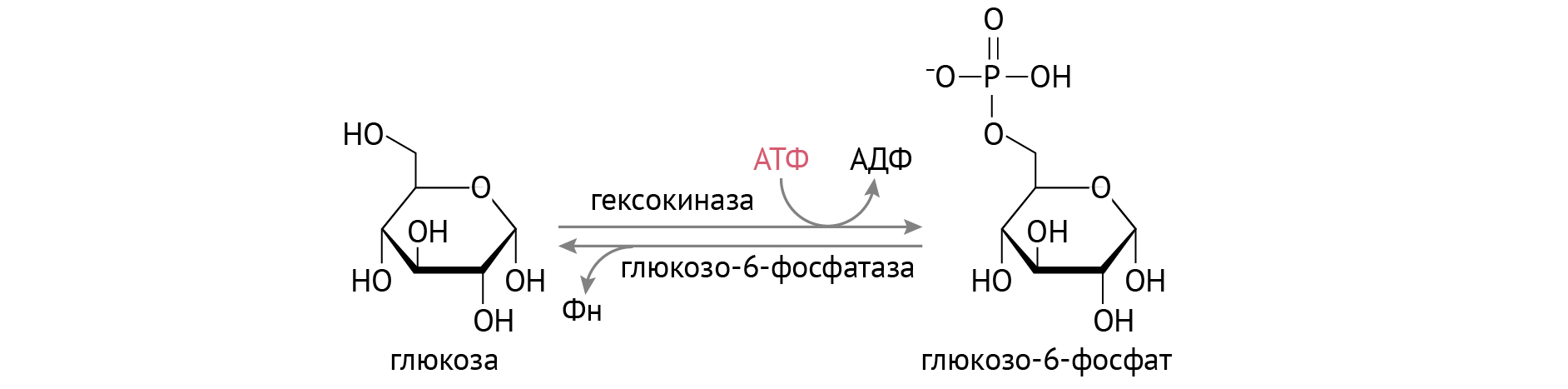
Данная реакция необходима по нескольким причинам:
- Глюкозо-6-фосфат (Г6Ф) — это активная форма глюкозы, необходимая для осуществления реакций в клетке с ее участием.
- Образование Г6Ф нужно для постоянного притока глюкозы в клетку. (Глюкоза и Г6Ф — разные молекулы, что имеет значение для диффузии глюкозы в клетку и поддержания концентрационного градиента.)
В печени и В-клетках поджелудочной железы работает гексокиназа 4, или глюкокиназа. Этот фермент характеризуется тем, что не ингибируется конечным продуктом реакции — Г6Ф. Это значит, что образование Г6Ф будет пропорциональным количеству глюкозы. Отсюда вытекают и иные особенности, о которых мы скажем позже. Примечательно, что образование Г6Ф невозможно без магния [2].
Попадая в В-клетки, Г6Ф вовлекается в гликолиз и активно включается в цикл трикарбоновых кислот (ЦТК). Чуть позже мы разберем их более детально. Главное, на что здесь надо обратить внимание, — это результат ЦТК в В-клетках. Ты наверняка где-то слышал о том, что ЦТК сопряжен с митохондриальным дыханием, то есть с синтезом АТФ — главного источника энергии в клетки. При резком повышении глюкозы в В-клетке растет интенсивность ЦТК, что приводит к повышению концентрации АТФ и увеличению соотношения АТФ/АДФ [4].
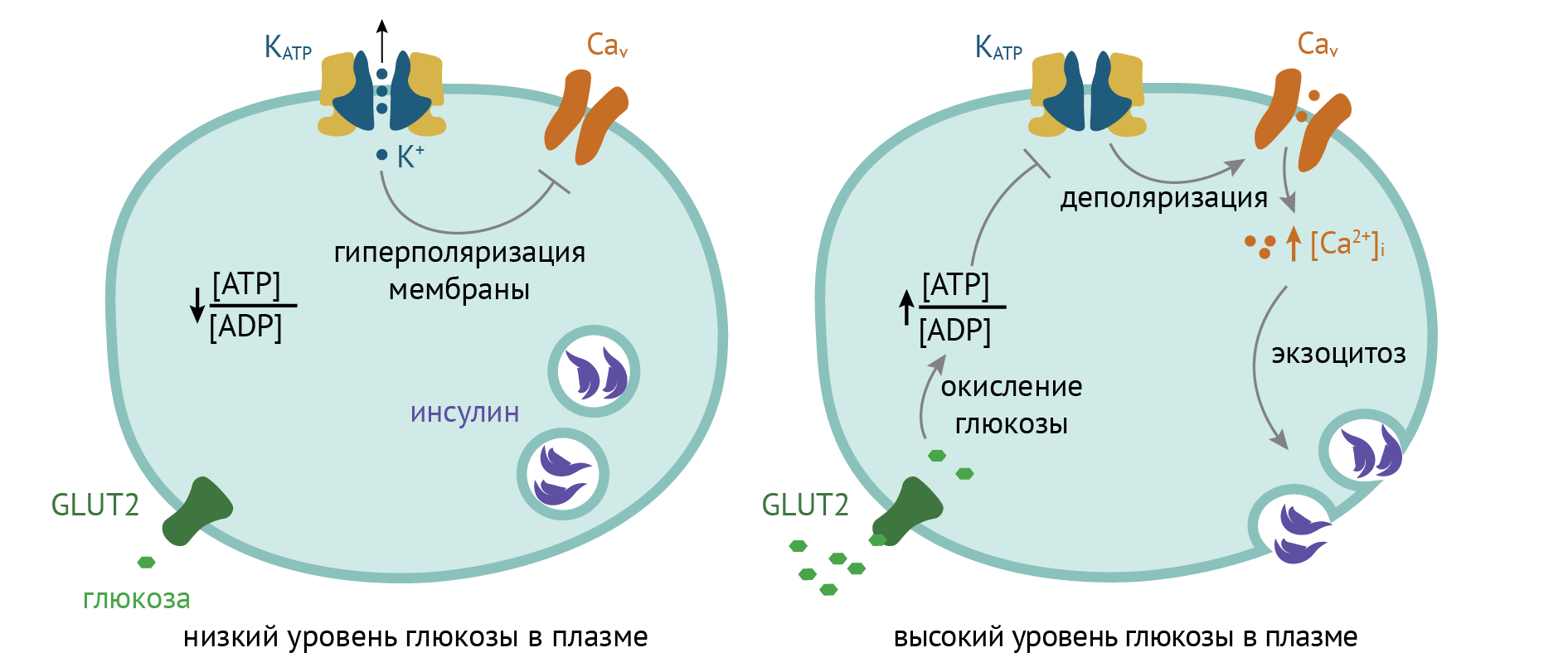
Шаг 2. Секреция инсулина. Сдвиг соотношения АТФ/АДФ снижает активность мембранных калиевых каналов (тем самым их закрывая). Эти каналы очень интересны в силу наличия в них множества рецепторных мишеней (см. далее) [2, 4].
В результате возникает деполяризация мембраны. Это становится пинком для открытия кальциевых каналов L-типа. Кальций, универсальный посредник экзоцитоза, индуцирует экзоцитоз и здесь: повышение его концентрации истерически провоцирует выброс инсулина.
Резюмируя, проследим цепь реакций: попадание глюкозы в кровь 🡪 попадание глюкозы в В-клетки поджелудочной железы 🡪 интенсификация ЦТК и рост АТФ 🡪 аллостерическое ингибирование калиевых каналов молекулами АТФ 🡪 деполяризация мембраны🡪 рост концентрации кальция в клетке (его выход из внутриклеточных депо) 🡪 экзоцитоз инсулина [4].
Шаг 2.1. Другой регуляторный механизм. Секреция инсулина зависит и от концентрации в В-клетках цАМФ. цАМФ участвует в фосфорилировании белков, ответственных за секрецию инсулина (иными словами, чем больше цАМФ в клетке, тем активнее белки-участники экзоцитоза и тем выше секреция инсулина). Это относительно новые данные: не удивляйся, что их нет в библиотечных учебниках. Зато теперь ты знаешь, что секреция инсулина может усиливаться через изменение концентрации цАМФ. А увеличивается она при действии кишечных гормонов на В-клетки. К ним относится инкретины. Они воздействуют на свои рецепторы, что приводит к увеличению содержания цАМФ [4].
Инкретины — класс гормонов, продукция которых организмом начинается после приема пищи и которые являются стимуляторами секреции инсулина. К инкретинам относятся пептидные гормоны: глюкозозависимый инсулинотропный полипептид (ГИП) и энтероглюкагон (он же — глюкагоноподобный пептид-1; ГПП-1).
Инкретины вырабатываются в кишечнике в ответ на прием пищи. До 70 % секреции инсулина после приема пищи у здоровых людей обусловлено именно эффектом инкретинов. У больных сахарным диабетом 2-го типа этот эффект значительно снижен.
Куда стекает кровь от кишечника? Надеюсь, для тебя не будет открытием, что в воротную вену печени — в эту биохимическую лабораторию, которая способна не только эффективно перерабатывать этанол и ибупрофен при месячных, но и осуществлять кучу других функций. Одной из них является контроль уровня глюкозы в крови путем высвобождения глюкозы из гликогена. Впрочем, печень не единственная, кто получает лакомый кусок. Глюкозы обычно хватает на все клетки. А вот что с ней происходит дальше, мы сейчас и посмотрим [3, 4].
Превращения глюкозы в клетке
Попадая в клетку, как мы и обсуждали ранее, глюкоза претерпевает превращение в Г6Ф. Это делает ее молекулой легкого поведения, которая вступает в самые разные, подчас поражающие своей извращенностью, реакции [1].
Первая группа реакций — синтетические:
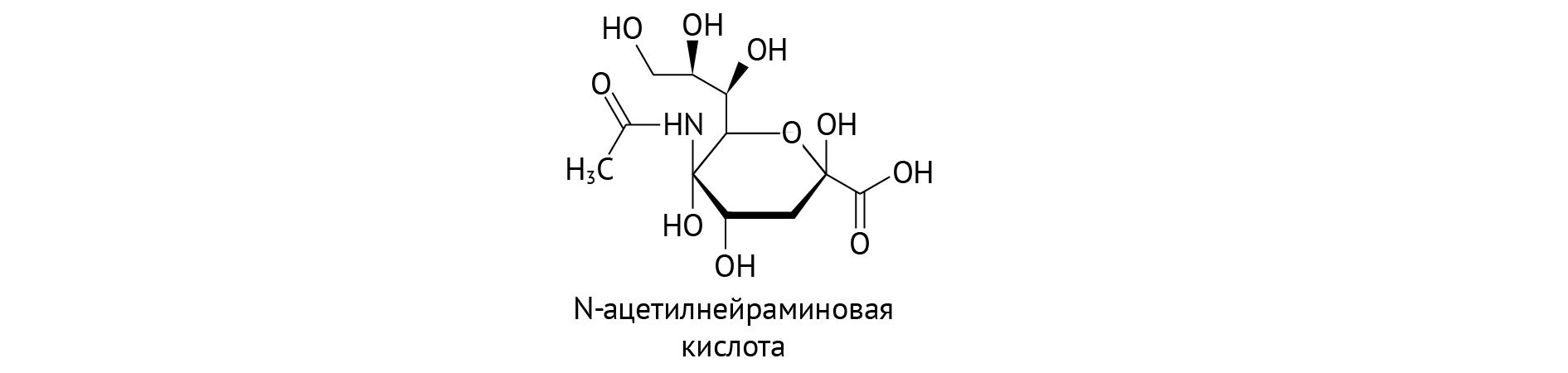
- Глюкоза — субстрат пентозофосфатного пути —источника рибозо-5-фосфата (для синтеза нуклеотидов) и НАДФН (восстановительного эквивалента, участвующего в целой серии синтетических реакций)
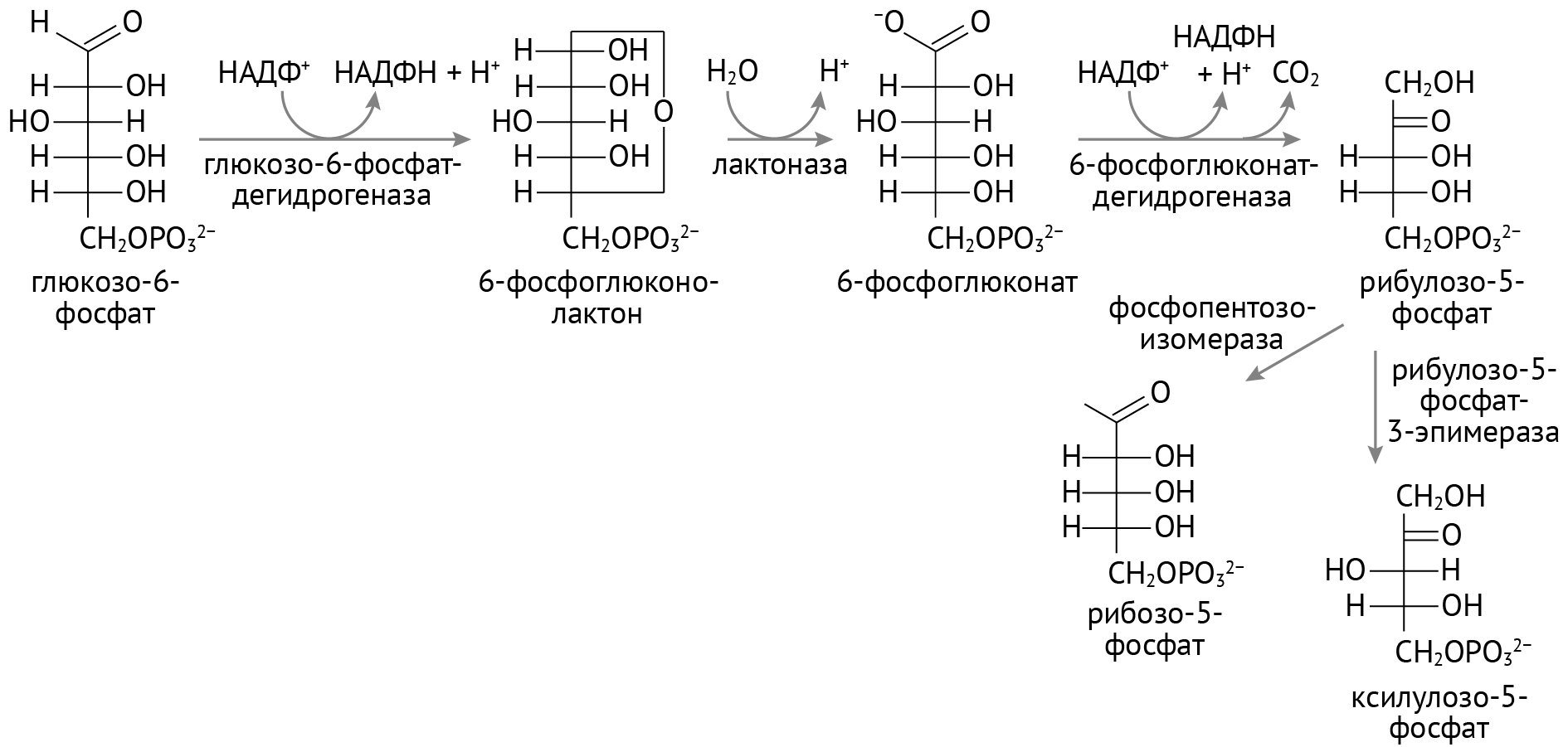
- Сахара могут быть элементом гликокаликса и частью некоторых поверхностных рецепторов в клетке. В процесс синтеза таких рецепторов глюкоза вписывается уже будучи производной самой себя — например, N-ацетилсиаловой кислотой. Сиаловая кислота включается в процесс на стадии посттрансляционной модификации протеинов (когда к белку в комплексе Гольджи после трансляции на рибосомах присоединяется небелковый компонент). Пример таких рецепторов — вирусные рецепторы (рецепторы к нейраминидазе вируса гриппа). Это тот самый рецептор клеток мерцательного эпителия дыхательных путей, который позволяет вирусу гриппа проникать в клетку и реализовать свой пролиферативный потенциал.
- Синтез в печени и мышцах гликогена — запасающей формы глюкозы. Данный процесс осуществляется следующим образом [1, 4];
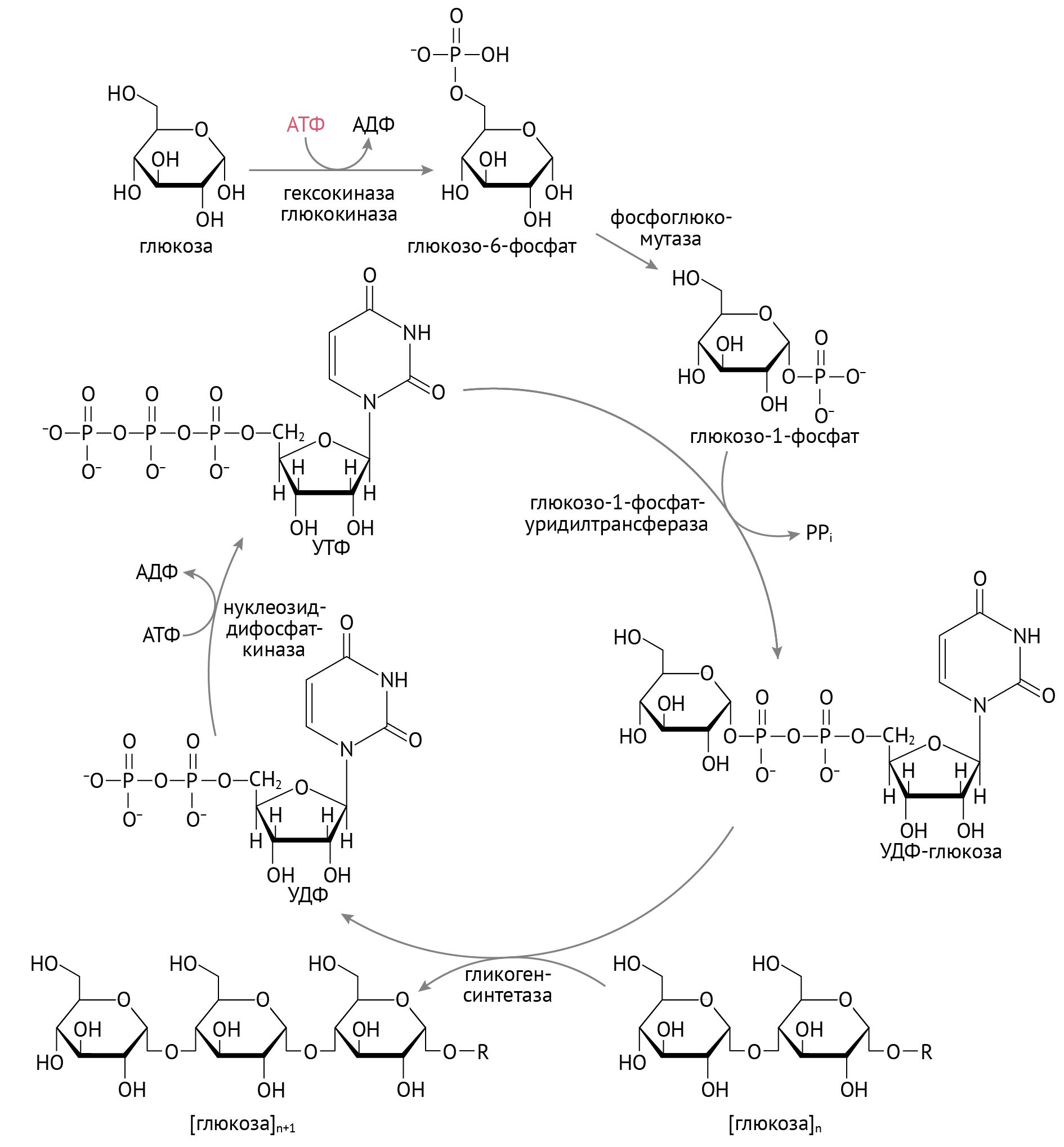
Здесь присутствует знакомый нам по предыдущей лекции УДФ-глюкуронид (УДФ-ГЛК) (глава 1). Примечательно, что исходным субстратом для синтеза этого кофермента служит сама глюкоза (глюкоза 🡪 рибозо-1-фосфат 🡪 УТФ 🡪 УДФ 🡪 УДФ-глюкоза). Все переплетено [1]...
Вторая группа реакций — катаболические.
Но основное предназначение глюкозы — светить другим, сгорая самой. Получается это у нее неплохо, поэтому мы получаем просто нескончаемый поток энергии. Поговорим, как это происходит.
Гликолиз
Схема проста, смысл — тоже: из одной молекулы глюкозы должно получиться две молекулы пировиноградной кислоты. Это ты знаешь еще с пятого класса своей коррекционной школы:
Глюкоза🡪 2 ПВК + 2 АТФ
Гликолиз включает в себя два этапа [1, 3]:
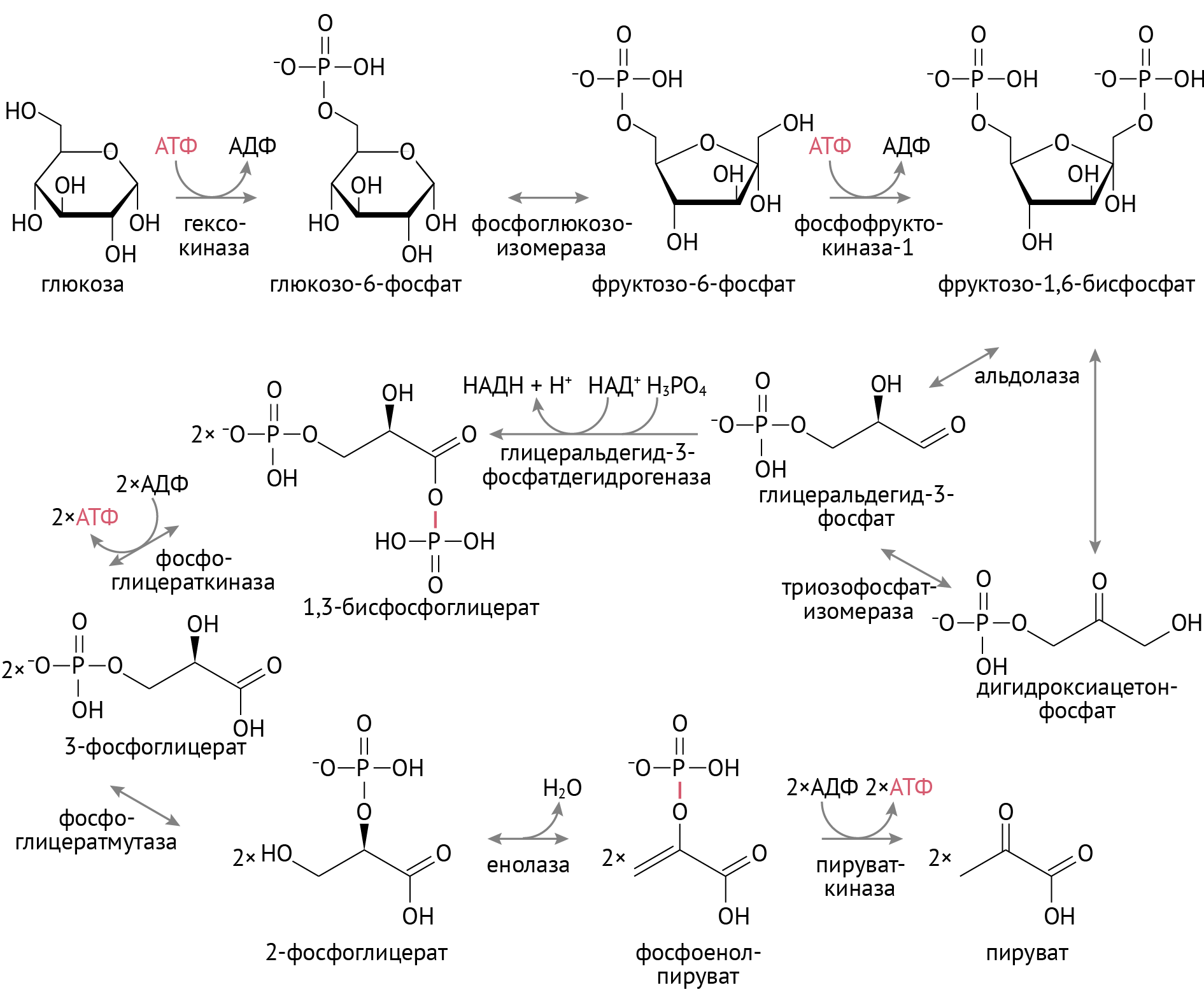
Реакции просты для запоминания (просто прописывай их в перерывах между отработками), дам пару комментариев.
- Фосфофруктокиназная реакция здесь — главная реакция. Она является лимитирующей, и ее скорость определяет скорость гликолиза. Это настолько важная реакция, что на нее даже расходуется АТФ.
- Первый этап заканчивается раздроблением сахара на два триуглеродных (С3) фрагмента: глицеральдегид-3-фосфат и дифосфоглицерат. Они взаимно превращаются друг в друга. 95 % продуктов реакции составляет глицеральдегид.
По мере истощения пула кетона дифосфоглицерата глицеральдегид любезно и по-джентельменски превращается в указанное соединение.
Глицеральдегид-3-фосфат служит мостиком между углеводным и липидным обменом, а также мостиком к твоим бокам. Глицеральдегид — субстрат для синтеза глицерола, а тот — для синтеза триацилглицеридов — основной запасающей формы жиров. Так что возьми с полки еще одну шоколадку и продолжаем [1–3].
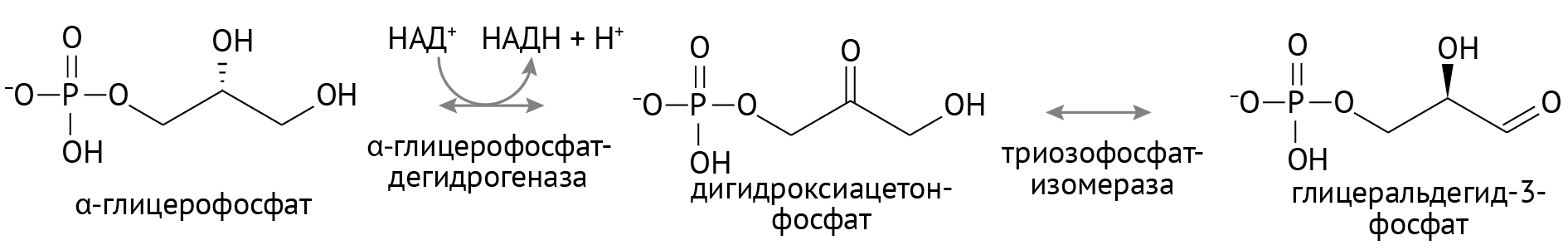
Для экзамена тебе нужно знать, в каких реакциях образуются АТФ и НАДН, а в каких они используется, и при каких обстоятельствах. Взгляни, всмотрись в схему и перепиши ее пару раз.
Интересен фермент енолаза. В клетках нервной ткани и диффузной нейроэндокринной системы обнаружили ее особую форму — нейро-специфическую енолазу (НСЕ). Существуют работы, где НСЕ пытались оценить как онкомаркер для мелкоклеточного рака легкого, несмотря на то, что НСЕ не является строго специфичной для данного заболевания. Также были попытки использовать ее для оценки повреждения ЦНС при черепно-мозговой травме.
Фосфоенолпируват — один из промежуточных соединений глюконеогенеза — синтеза глюкозы из неуглеводных предшественников через ПВК. После фосфоенолпирувата глюконеогенез становится повторением реакции гликолиза, только в обратном направлении (за исключением фосфофруктокиназной реакции — она неповторима и незаменима).
Гликолиз бывает аэробным — осуществляемым в присутствии кислорода и способствующим образованию ПВК. А может быть анаэробным — физиологическим (в эритроцитах, в скелетных мышцах после работы) и патологическим (гипоксия различного генеза).
Разница в исходе гликолиза следующая. Если есть кислород, гликолиз закончится на образовании пировиноградной кислоты, которая станет ацетил-КоА и даст много-много энергии. А если у нас гипоксия, то будет работать лактатдегидрогеназа, и из ПВК получится лактат (молочная кислота). Этот фермент имеет колоссальное значение, а реакция важна с точки зрения развития многих патологических процессов.
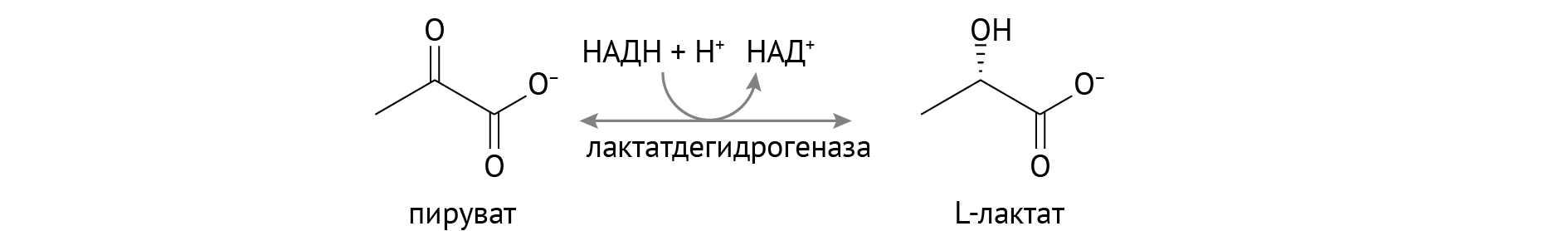
Промежуточный этап метаболизма глюкозы
Мы коснемся промежуточного этапа на пути к образованию конечных метаболитов и к твоему отчислению. Здесь мы имеем дело с пируватдегидрогеназным комплексом. Это конгломерат пяти ферментов, которые последовательно превращают ПВК в ацетил-КоА — субстрат для цикла Кребса (ЦТК) [1–3].
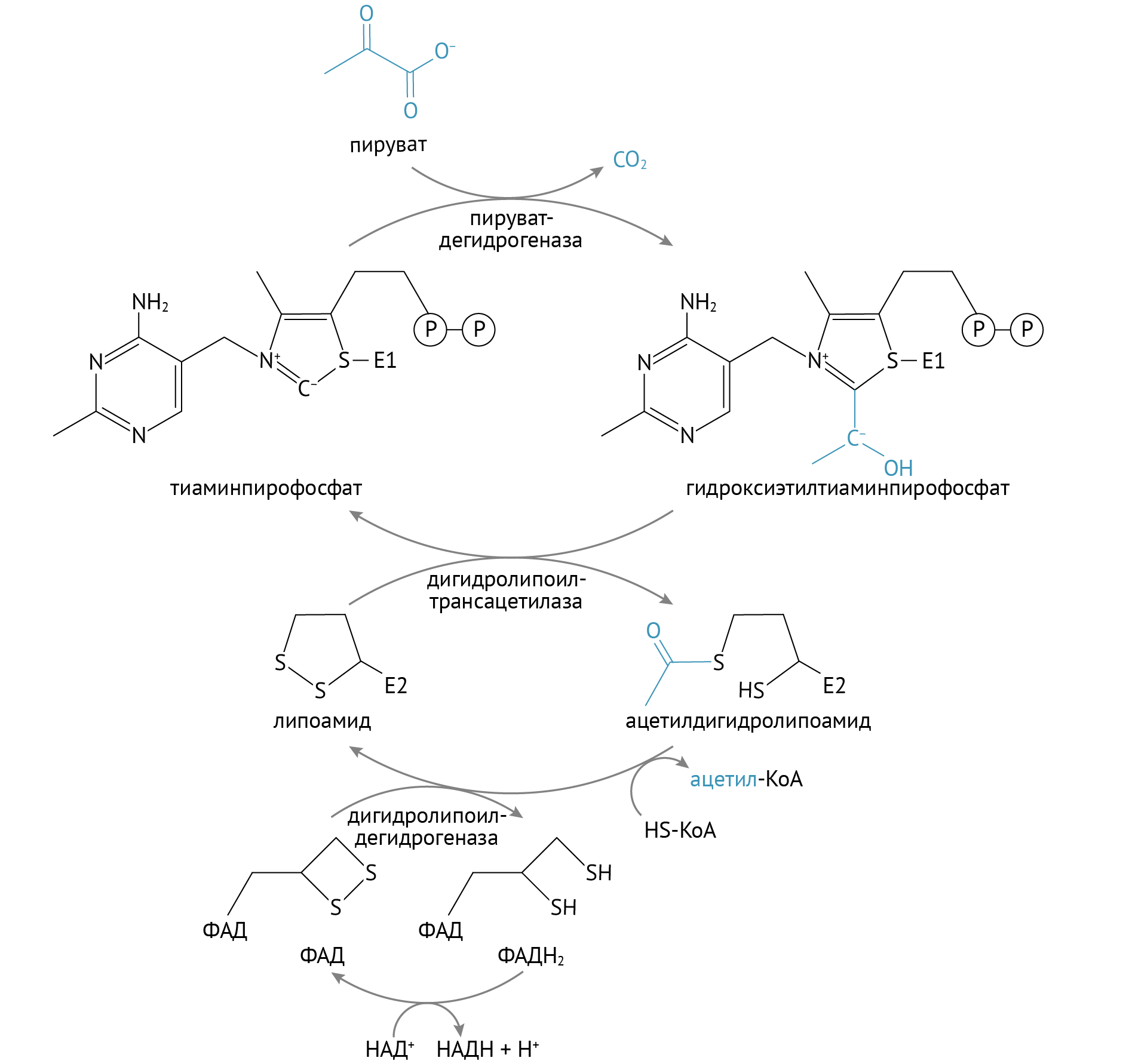
Сможешь ли ты это выучить? Мне все равно, я лишь хочу акцентировать внимание на том, что здесь активно участвует тиамин (В1). Сладкоежкам и алкоголикам рекомендуют получать дополнительную дотацию витамина В1 в силу того, что при указанных поведенческих особенностях биоэнергетика может несколько страдать: в первом случае часть глюкозы уйдет в бока, а во втором — глюкоза в принципе не нужна для ЦТК (и тоже уйдет в бока, если ты выпиваешь в прикуску с чем-то сладким и жирным). (Уровень доказательности — мнение отдельных экспертов).
И мы подошли к самому главному и любимому всеми студентами (даже троечниками) — к циклу трикарбоновых кислот.
Цикл трикарбоновых кислот
Его суть проста: пока ацетил-КоА сгорает в серии реакций, в некоторых из них высвобождаются восстановительные эквиваленты — 2 НАДН и ФАДН2. Они являются донорами электронов для электрон-транспортной цепи. Электрон-транспортная цепь, в свою очередь, служит базой формирования энергии АТФ. Не надо говорить на экзамене, что смысл ЦТК — сжечь ацетил-КоА до воды и углекислоты. Углекислота — это побочный продукт ЦТК. Но имеющий для клинической практики важное значение.
▶ Читать по теме: Цикл трикарбоновых кислот (доступно в PDF)
Также хочу акцентировать внимание на том, что ЦТК является множественным по значению циклом: здесь можно найти молекулы, активно участвующие в различных анаболических процессах. (Например, сукцинат служит субстратом для синтеза гема; ацетил-КоА — для синтеза жирных кислот, кетоновых тел и холестерола; α-кетоглутарат — для синтеза глутамата и реакций трансаминирования [1–3]).
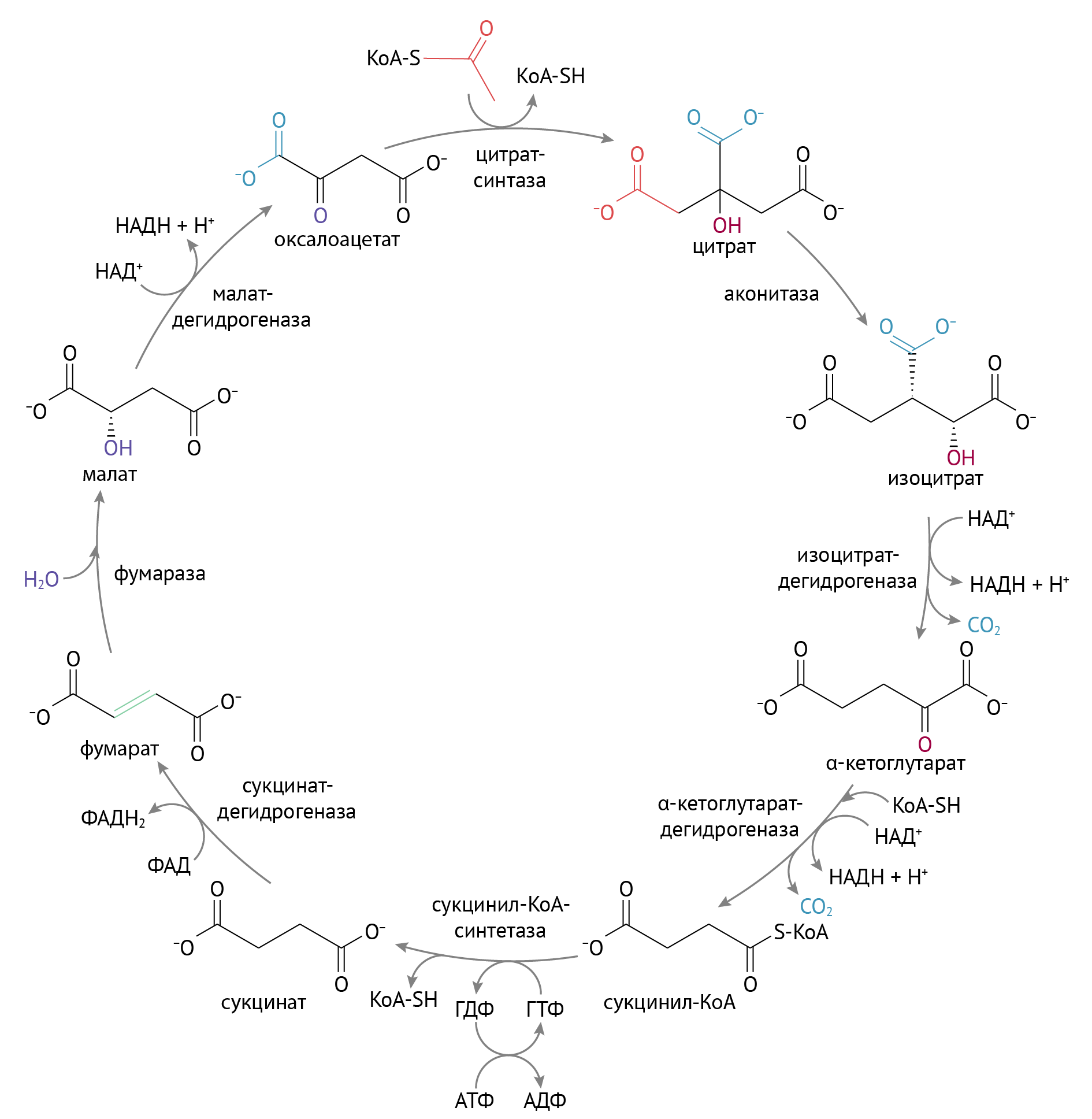
Комментарии к ЦТК, которые пригодятся на экзамене и по жизни:
- ЦТК — это вечеринка для молекул из самых разных серий метаболизма. Здесь можно найти субстрат для ряда анаболических реакций:
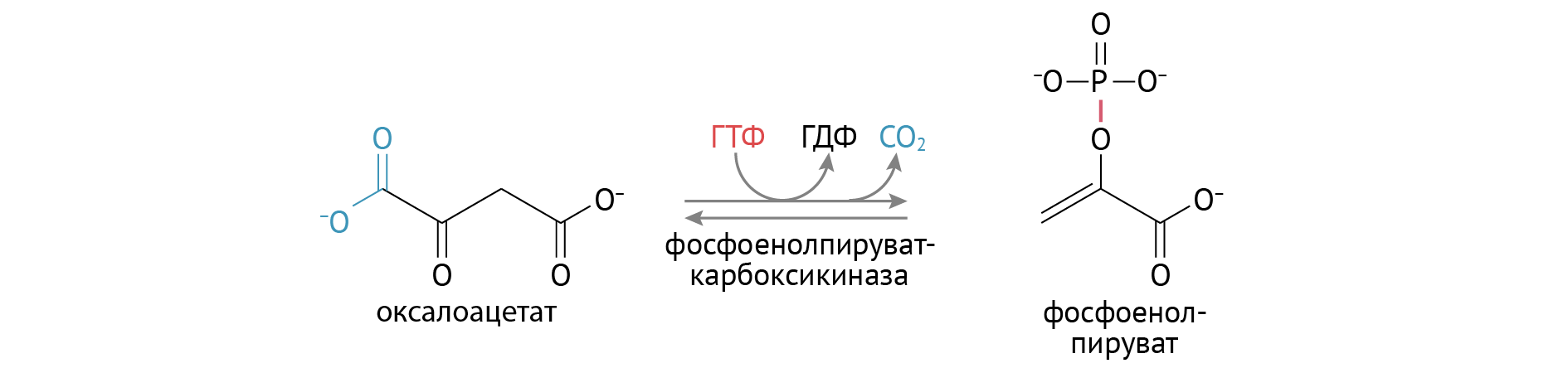
(Глюконеогенез)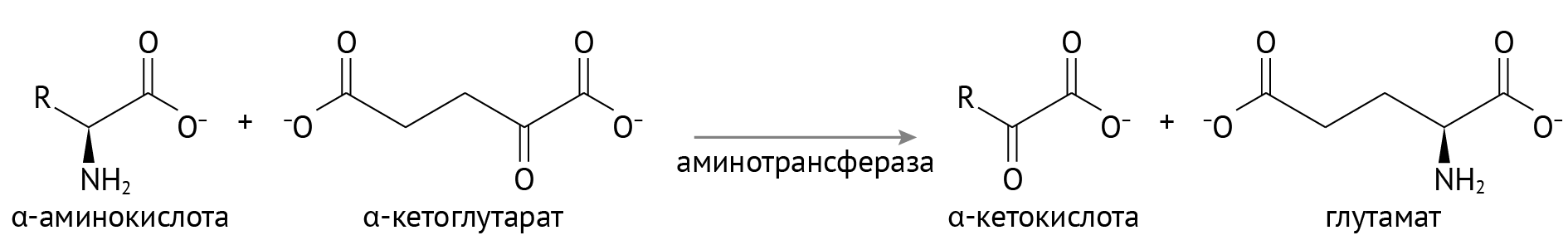
(Синтез самых разных кетокислот из соответствующих аминокислот) - Глутамат можно превратить в глутамин и тем самым утилизировать азот, образующийся в клетках и являющийся токсичным в больших концентрациях (см. главу 5).
- Оксалоацетат можно превратить в аспартат. Аспартат участвует в цикле мочевины (процесс превращения азота в нечто безопасное и растворимое) и в синтезе пуриновых колец (пиримидиновых вроде тоже).
Здесь можно найти продукты метаболизма ряда веществ. - Фумарат является одним из продуктов метаболизма тирозина, а также обмена пиримидиновых нуклеотидов.
- Сукцинил КоА — продукт β-окисления жирных кислот с нечетным числом углеродных атомов.
- α-кетоглутарат — это продукт реакций трансаминирования.
Обрати внимание на то, что одним из субстратов является оксалоацетат. Ему тоже нужно откуда-то браться. Есть чудесный фермент — аспартатаминотрансфераза (АсТ). Это органоспецифичный фермент, обнаруживающийся преимущественно в печени и в сердце и имеющий колоссальное значение для биоэнергетики: без него ЦТК не «заработает», потому как ЦТК надо запустить двумя субстратами: ацетил-КоА и оксалоацетатом.
Если ацетил-КоА будет слишком много (кетонемия при сахарном диабете, массивное поступление жиров, алкогольная атака), он будет расходоваться на синтетические процессы. Это может быть синтез холестерола или кетоновых тел. Ничто в нашем организме не пропадает без дела — кроме жира на боках, естественно…
Глава 4 | Катаболизм липидов
Источники:
- Тимин О. А. Основы биологической химии, 2018 г., с. 181–220.
- Портал «Биохимия для студента», раздел «Обмен углеводов».
- Я. Кольман, К.-Г. Рём. Наглядная биохимия, 5-е издание, 2018 г., с. 38–44, 138–152.
- А. Д. Таганович, Э. И. Олецкий, И. Л. Котович. Патологическая биохимия, 2015 г., c. 44–47.
